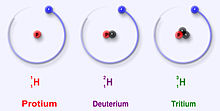
Vedyllä on kolme pääisotooppia: protium (1H), deuterium (2H) ja tritium (3H). Nämä isotoopit muodostuvat luonnossa. Protium on yleisin ja koostuu yhdestä protonista ilman neutronia. Deuterium sisältää yhden neutronin, ja se on stabiili. Tritium on radioaktiivinen ja hajoaa beetahajoamisella helium-3:ksi; sen puoliintumisaika on noin 12,32 vuotta. Tutkijat ovat lisäksi luoneet laboratorio-oloissa lyhytikäisiä vedyn isotooppeja, kuten 4H–7H, mutta ne ovat erittäin epävakaita eikä niitä esiinny merkittävästi luonnossa.
Määritelmä ja perusominaisuudet
Isotoopit ovat saman alkuaineen atomeja, joilla on sama määrä protoneja mutta eri määrä neutroneja. Vedyn tapauksessa protonien määrä on aina yksi, joten isotooppien ero tulee neutroneista. Tästä johtuen vedyllä on poikkeuksellisen yksinkertaiset ja helposti tunnistettavat isotoopit:
- Protium (1H): yksi protoni, ei neutronia. Suurin osa vedystä on tätä isotooppia.
- Deuterium (2H, myös D): yksi protoni ja yksi neutroni. Stabiili, suhteellisen harvinainen luonnossa mutta helposti erotettavissa ja hyödyllinen monissa sovelluksissa.
- Tritium (3H, myös T): yksi protoni ja kaksi neutronia. Radioaktiivinen ja harvinainen luonnossa; syntyy esimerkiksi kosmisten säteiden vaikutuksesta ilmakehässä ja ydinreaktoreissa.
Luonnollinen esiintyminen ja runsaus
Protium muodostaa lähes kaiken luonnollisen vedyn: sen osuudet luonnollisessa vedessä ovat noin 99,98 %. Deuteriumin luonnollinen runsaus on noin 0,0156 % (noin 156 ppm), mikä riittää esimerkiksi raskaan veden (D2O) valmistukseen teollisesti erotusmenetelmillä kuten elektrolyysillä, kemiallisilla vaihtoprosesseilla tai fraktioimisella. Tritiumia esiintyy luonnossa vain hyvin pieniä määriä, mutta sitä syntyy myös ihmisen toiminnan seurauksena ydinreaktoreissa ja ydinasekokeissa.
Fysikaaliset ja kemialliset erot
Deuteriumin ja protiumin välillä on merkittävä massiero: deuteriumin atomin massa on noin kaksinkertainen verrattuna protiumiin, ja tritium on vielä raskaampi. Tämä johtaa useisiin havaittaviin eroihin:
- Fysikaaliset ominaisuudet: D2O:n sulamis- ja kiehumispisteet ovat hieman korkeammat kuin H2O:n; esimerkiksi raskaan veden tiheys on suurempi. Massan erot vaikuttavat myös esimerkiksi lämpökapasiteettiin ja diffuusiokertoimiin.
- Kemialliset reaktiot ja isotooppiefekti: Kevyemmän ja raskaamman vedyn väliset massat vaikuttavat reaktioiden nopeuksiin (kineettinen isotooppiefekti). Tämä tarkoittaa, että kemiallisissa reaktioissa, joissa vedyn sidokset katkeavat tai muodostuvat, deuteriumin sisältämät molekyylit reagoivat usein hitaammin kuin protiumia sisältävät.
- Radioaktiivisuus: Tritium tuottaa matalaenergistä beetasäteilyä, joka ei läpäise ihoa syvälle, mutta tritium on vaarallisin, jos sitä pääsee elimistöön hengityksen, ruuan tai veden mukana.
Käyttö ja sovellukset
Vedyn isotoopeilla on monia tärkeitä sovelluksia:
- Deuterium (D): käytetään raskaan veden muodossa neutronien hidastimena joissakin ydinreaktoreissa (esim. CANDU), ja deuteriumia käytetään myös isotooppileimauksessa, NMR-spektroskopiassa (D2O-liuos kantajana) sekä tutkimuksissa, joissa halutaan seurata veden liikettä tai reaktiomekanismeja.
- Tritium (T): käytetään joskus valoa tuottavissa laitteissa (esim. tritium-valomerkit), ydinfuusion polttoaineena kokeellisissa laitteissa (yhdessä deuteriumin kanssa), sekä tutkimukseen käytettävänä radioisotooppina ja seurantamerkkinä hydrologiassa ja ympäristötutkimuksissa. Tritiumin radioaktiivisuus tekee siitä käyttökelpoisen merkkiaineen, mutta sama ominaisuus aiheuttaa turvallisuus- ja hävittämishaasteita.
- Isotooppileimaukset: Deuteriumia ja tritiumia käytetään laajasti biokemiallisissa ja lääketieteellisissä merkintätutkimuksissa seurantamolekyyleinä.
Tuotanto ja erotus
Deuterium erotetaan luonnollisesta vedestä useilla menetelmillä, kuten elektrolyysillä, fraktioivalla tislauksella ja kemiallisella vaihtotekniikalla. Tritiumia tuotetaan pääasiassa ydinreaktoreissa neutronisäteilyn vaikutuksesta litium- tai booriyhdisteissä, tai se syntyy myös kosmisten säteiden aiheuttamina reaktioina ilmakehässä.
Turvallisuus ja ympäristö
Tritiumin radioaktiivisuus vaatii erityistä käsittelyä: vaikka sen beetasäteily on matalaenergiaista, sisäinen altistus (hengitys, nieleminen) voi aiheuttaa säteilyannoksen kudoksille. Tritiumia sisältävät jätteet täytyy käsitellä ja varastoida asianmukaisesti. Deuterium ja protium ovat kemiallisesti turvallisia normaaleissa olosuhteissa; raskaan veden pitkäaikainen käyttö voi kuitenkin vaikuttaa biologisiin prosesseihin, jos se korvaa merkittävästi normaalia vettä eliöiden elimistössä.
Nimet ja tunnukset
Vedyn pääisotoopit ovat poikkeuksellisia myös nimien puolesta: ne ovat ainoat isotoopit, joilla on vakiintuneet nimet (protium, deuterium, tritium). Deuteriumia ja tritiumia merkitään usein lyhenteillä D ja T. Kansainvälinen puhtaan ja soveltavan kemian liitto suhtautuu näihin nimityksiin varauksellisesti, mutta käytännössä D- ja T-merkinnät ovat laajasti käytössä tieteessä ja tekniikassa.
Yhteenvetona: vedyllä on yksinkertaiset mutta biologisesti ja teknisesti merkitykselliset isotoopit. Protium on yleisin ja kemiallisesti perusedullinen, deuterium tarjoaa mahdollisuuden tutkimukseen ja teollisiin sovelluksiin raskaan veden muodossa, ja tritium on tärkeä radioaktiivinen merkkiaine ja fuusiopolttoaineen komponentti, jonka käsittely vaatii huolellisuutta.