Termodynamiikan toinen laki sanoo, että kun energia muuttuu muodosta toiseen tai kun aine liikkuu vapaasti, entropia (epäjärjestys tai energian hajaantuminen) kasvaa suljetussa järjestelmässä. Käytännössä tämä merkitsee, että mikään prosessi ei voi muuttaa kaiken saatavilla olevan lämmön kokonaan työksi ilman muita muutoksia ympäristössä.
Lämpötila-, paine- ja tiheyserot tasoittuvat yleensä jonkin ajan kuluttua vaakasuunnassa, kun aine ja energia pääsevät kulkeutumaan vapaasti. Painovoiman vuoksi tiheys ja paine eivät tasaannu täysin pystysuunnassa: hydrostaattisessa tasapainossa paine ja tiheys ovat alhaalla suuremmat kuin ylhäällä johtuen gravitaatiopotentiaalista, vaikka paikallinen lämpötila voi olla sama. Tämä ei riko toista lakia, vaan on esimerkki siitä, miten ulkoiset kentät (kuten painovoima) vaikuttavat tasapainotilaan.
Entropia mittaa aineen ja energian leviämistä kaikkialle, minne ne pääsevät. Etenkin termodynamiikassa entropia kertoo, kuinka paljon energiaa on “säätelemättömässä” muodossa eli kuinka vähän siitä voidaan muuntaa hyödylliseksi työksi ilman lisämuutoksia ympäristössä.
Clausiusin ja Kelvinin lausunnot sekä matemaattinen muoto
Yleisin termodynamiikan toisen lain sanamuoto on pääosin Rudolf Clausiuksen ansiota. Clausius esitti sekä kvalitatiivisia lausuntoja että matemaattisen muodon, josta merkittävin on Clausiusin epätasa-arvo (Clausius inequality):
- Suljetulle (tai eristetyllä) systeemille: ΔS ≥ 0 — eli entropia ei pienene.
- Yleisemmin syklistä prosessia varten: ∮ δQ / T ≤ 0, missä δQ on systeemin vastaanottama lämmönmäärä ja T sen lämpötila.
Toisin sanoen reversiibelissä (täydellisesti palautuvassa) prosessissa entropian muutos ΔS = ∫ δQ / T, ja irreversiibelissä prosessissa ΔS > ∫ δQ / T. Reversiibeli prosessi on ideaalitapaus; todellisuudessa kaikki luonnolliset prosessit sisältävät irreversibiliteetteja ja siten entropian kasvua.
Toisesta laista on olemassa monia lausumia, joissa käytetään eri termejä, mutta kaikki tarkoittavat samaa asiaa. Toinen Clausiuksen lausuma on:
Lämpö ei voi itsestään siirtyä kylmemmästä kappaleesta kuumempaan.
Lordi Kelvinin vastaava lausunto on:
Muunnos, jonka ainoa lopputulos on vakiolämpötilassa olevasta lähteestä otetun lämmön muuttaminen työksi, on mahdoton.
Nämä Clausiusin ja Kelvinin lausunnot ovat keskenään yhtäpitäviä: molemmat ilmaisevat toisen lain perusrajoituksen lämmön ja työn muuttamiselle. Niistä seuraa myös Carnot'n teoreema, joka asettaa ylärajan lämpömoottorin hyötysuhteelle:
- Carnot-hyötysuhde: η_max = 1 − T_c / T_h, missä T_h on kuuman lähteen ja T_c kylmän lähteen absoluuttinen lämpötila.
Tilastollinen tulkinta ja pienet järjestelmät
Toinen laki on periaatteessa tilastollinen laki: mikrotason dynamiikka (esim. atomien törmäykset) on usein aika-symmetrinen, mutta suurten hiukkumäärien kokonaistodennäköisyydet johtavat siihen, että entropian kasvu on äärimmäisen todennäköinen. Boltzmannin kaava antaa yhteyden mikrotason tilojen lukumäärän W ja makrotason entropian S välillä:
- S = k_B ln W, missä k_B on Boltzmannin vakio.
Tämän vuoksi hyvin pienissä järjestelmissä tai lyhyillä aikaskaaloilla voivat esiintyä tilapäisiä entropian laskuja (fluktuatiot), mutta suurissa sistemaattisissa kokoonpanoissa entropian kasvu dominoi ja toinen laki pitää käytännössä aina paikkansa.
Seuraukset ja käytännön esimerkkejä
- Arkipäivässä lämpö virtaa kuumasta kylmään; esimerkiksi kuuma kahvikuppi jäähtyy huoneenlämpöön, eikä se itsestään kuumene takaisin.
- Sekoitusilmiöt: kaksi erilaista kaasua sekoittuvat spontaanisti, ja niiden erottaminen takaisin alkuperäiseen tilaan vaatii työpanosta (esim. suodattaminen tai erotuskenttä).
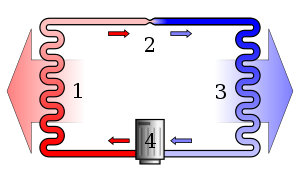
- Lämpövoimakoneet ja jääkaapit: koneet voivat muuntaa lämpöä työksi, mutta eivät täydellä hyötysuhteella; jääkaapit siirtävät lämpöä kylmästä tilasta kuumaan, mutta se vaatii ulkoista työtä.
- Eksergia: toisen lain seurauksena energian laadullinen arvo heikkenee — vaikka kokonaisenergia säilyy, energian käyttökelpoisuus työksi (eksergia) pienenee entropian kasvaessa.
Soveltamisalue ja rajoitukset
Toista lakia sovelletaan parhaiten suuriin, monen hiukkasen vaikutuspiirissä oleviin järjestelmiin ja siksi se on tilastollinen laki. Jos järjestelmä ei ole eristetty (energiaa tai ainetta pääsee sisään tai ulos), entropian kokonaismuutos riippuu vaihdosta ympäristön kanssa — mutta koko eristetyn systeemi+ympäristö -kokonaisuuden entropia ei pienene. Lisäksi ulkoiset kentät (kuten painovoima) ja muut konstraintit voivat johtaa tiloihin, joissa muuttujat (esim. paine, tiheys) eivät ole homogeenisia, vaikka järjestelmä olisi tasapainossa.
Yhteenvetona: toinen termodynamiikan laki kertoo, että energia pyrkii leviämään ja homogenisoitumaan niin että käyttökelpoinen energia vähenee, ja tämä prosessi on todennäköisyyspohjainen — lähes aina havaittava ja sovellettava suurissa systeemeissä, mutta mikroskooppisilla mittakaavoilla esiintyy satunnaisia poikkeamia.