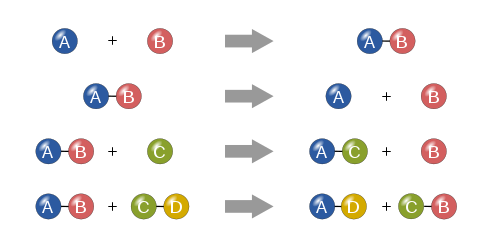
Kemiallinen reaktio tapahtuu, kun yksi tai useampi kemikaali muuttuu yhdeksi tai useammaksi muuksi kemikaaliksi. Reaktiossa atomien järjestys ja elektronien sitoutuminen muuttuvat, mutta atomien lukumäärä pysyy samana (massan säilymislaki). Esimerkkejä:
- Rauta ja happi muodostavat yhdessä ruostetta
- etikka ja ruokasooda yhdistyvät natriumasetaatiksi, hiilidioksidiksi ja vedeksi.
- palavat tai räjähtävät esineet
- monia reaktioita, jotka tapahtuvat elävien olentojen sisällä
- sähkökemialliset reaktiot akkuja purettaessa tai ladattaessa
Jotkut reaktiot ovat hyvin nopeita, toiset hitaita. Reaktioiden nopeuteen (reaktiokinetic) vaikuttavat muun muassa lämpötila, aineiden konsentraatio, pinta-ala ja katalyytit. Monet reaktiot muuttuvat nopeammin korkeammassa lämpötilassa: esimerkiksi puu ei reagoi ilman kanssa, kun se on kylmää, mutta jos se kuumennetaan tarpeeksi, se alkaa palaa. Reaktioilla on myös oma aktivaatiokykynsä — energiamäärä, joka tarvitaan, jotta reaktio voi alkaa.
Energian muutokset
Joistakin reaktioista vapautuu energiaa. Nämä ovat eksotermisiä reaktioita: reaktion tuotteissa on vähemmän sisäenergiaa kuin lähtöaineissa, ja ylimääräinen energia vapautuu usein lämmöksi tai valona. Toisissa reaktioissa energiaa otetaan sisään; nämä ovat endotermisiä reaktioita. Energian muutokset mitataan tavallisesti jouleina tai kilojouleina per mooli (kJ/mol) ja liittyvät termodynamiikan suureisiin, kuten entalpian muutokseen (ΔH).
Reaktioiden kulkua kuvataan usein energiaprofiililla (reaktiokoordinaattidiagrammi), jossa näkyy lähtöaineiden ja tuotteiden energiat sekä aktivaatioenergia. Katalyytit voivat alentaa aktivaatioenergiaa ja siten nopeuttaa reaktiota ilman, että ne muuttuvat pysyvästi itse reaktiossa.
Tasapaino ja kemiallisen yhtälön tasapainottaminen
Monet reaktiot ovat käänteisiä: tuotteet voivat reagoida muodostaakseen lähtöaineita. Tällöin järjestelmä voi saavuttaa kemiallisen tasapainon, jossa etenevän ja palautuvan reaktion nopeudet ovat yhtä suuret. Kemialliset reaktiot ilmaistaan reaktioyhtälöillä, jotka on tasapainotettava niin, että atomien lukumäärä on molemmilla puolilla sama (massan säilyminen). Tasapainotuksessa käytetään stoikiometriaa, joka kertoo kuinka monta moolia kukin aine kuluttaa ja muodostaa.
Reaktiomekanismit ja biologiset reaktiot
Yksinkertaisissa reaktioissa kaikki tapahtuu yhden askeleen kautta, monissa tapahtuu useita välivaiheita ja välituotteita — tätä kutsutaan reaktiomekanismiksi. Elävissä soluissa tapahtuvat reaktiot (metabolia) koostuvat usein monimutkaisista, usean vaiheen entsyymien katalysoimista reitistöistä. Nämä reaktiot ovat välttämättömiä elintoiminnoille, kuten energian tuotannolle ja solukomponenttien rakentamiselle.
Kemialliset vs. ydinreaktiot
Ydinreaktiot eivät ole kemiallisia reaktioita. Kemiallisissa reaktioissa muutoksissa ovat mukana atomien uloimmat elektronit ja niiden sidokset; ydinreaktioissa tapahtuu muutoksia atomiytimissä olevissa protoneissa ja neutroneissa, ja niihin liittyy yleensä paljon suurempia energiamääriä.
Käytännön merkitys ja turvallisuus
Kemiallisilla reaktioilla on valtava merkitys teollisuudessa, energiantuotannossa, lääketieteessä ja arjessa. Esimerkiksi polttoaineiden palaminen, lannoitteiden ja lääkkeiden valmistus, elintarvikkeiden happamuuden säätö ja akut toimivat kemiallisten reaktioiden avulla. Monet reaktiot voivat olla vaarallisia (palovaarat, myrkylliset kaasut, räjähdykset), joten reaktioiden käsittelyssä on noudatettava asianmukaisia turvallisuusohjeita.
Yhteenvetona: kemiallinen reaktio muuttaa aineiden sidoksia ja elektronijärjestystä tuottaen uusia aineita, noudattaa massan säilymistä, voi luovuttaa tai sitoa energiaa ja sen nopeuteen ja kulkuun vaikuttavat monet kemialliset ja fysikaaliset tekijät.