Elektroni on hyvin pieni kappale ainetta. Sen symboli on e− ja sen löysi J. J. Thomson vuonna 1897. Elektroni on perusosa, joka esiintyy sekä atomeissa että vapaana hiukkasena, ja se kantaa aina negatiivista sähkövarausta.
Elektroni on subatominen hiukkanen. Jokainen atomi koostuu ytimessä olevista protoneista ja neutroneista sekä atomin ydintä ympäröivistä elektroneista. Elektroni voi olla myös erillään mistä tahansa atomista; tällöin sitä kutsutaan vapaaksi elektroniksi. Elektronia pidetään alkeishiukkasena siinä mielessä, että sille ei ole todettu sisäistä rakennetta tai mahdollisuutta jakautua pienempiin osiin tunnetun fysiikan puitteissa. Sen sähkövaraus on negatiivinen ja vakio: yhden elektronin varauksen suuruus on noin −1,602176634×10^−19 coulombia (elementtärinen varaus).
Perusominaisuudet
- Varaukseen liittyvä arvo: −1,602176634×10^−19 C (elementtärinen varaus).
- Massa: hyvin pieni. Lepomassa on noin 9,10938356×10^−31 kg, eli elektronit ovat atomien massasta yleensä lähes mitättömiä.
- Spin: elektroni on fermioni, jolla on spin 1/2 — tämä tarkoittaa, että elektronit noudattavat Pauli-poissulkusääntöä ja Fermi–Dirac-tilastojakaumaa.
- Luonne: elektronit käyttäytyvät sekä hiukkasina että aaltomaisesti. Niitä kuvataan kvanttimekaniikassa aaltofunktiolla, ja niiden paikkaa ja liikemäärää koskee Heisenbergin epävarmuusperiaate.
- Ei-hajotettavuus: toistaiseksi elektronia ei ole havaittu koostuvan pienemmistä osista.
Nopeus ja liike
Elektronien massa on hyvin pieni, joten niihin kohdistuvilla kentillä ne voivat saada suuria nopeuksia. Vapaana olevat elektronit voivat liikkua lähes valon nopeudella esimerkiksi beetahiukkasina tai raskaiden alkuaineiden sisäisissä elektronikuorissa, joilla on suuri atomiluku. Kun elektronit liikkuvat johtimissa, ne muodostavat sähkövirran ja siten tuottavat käytännön sähkölaitteiden toiminnan.
Vuorovaikutukset ja kentät
Elektronit osallistuvat useisiin perusvuorovaikutuksiin: gravitaatio-, sähkömagneettiseen ja heikkoon vuorovaikutukseen. Näistä sähkömagneettinen vuorovaikutus on arkipäivän olosuhteissa merkittävin: elektronit hylkivät toisiaan johtuen samanmerkkisestä sähkövarauksesta ja vetäytyvät positiivisesti varautuneiden hiukkasten, kuten protonien, puoleen. Elektronin ympärillä on sähkökenttä, joka kuvaa tätä vetovoimaa ja hylkimistä.
Rooli atomeissa ja kemiassa
Atomien kemialliset ominaisuudet määräytyvät pitkälti niiden ulkokuoren elektroneista. Valenssielektronit osallistuvat kemiallisiin sidoksiin: ne voivat siirtyä atomista toiseen (ionisidoksessa), jakautua kahden atomin kesken (kovalenttinen sidos) tai muodostaa delokalisoituneita elektronipilviä (esim. metallisidos). Elektronin irrottaminen atomista vaatii ionisaatioenergiaksi kutsutun määrän, ja elektroneja vastaanottava atomi osoittaa elektronin affiniteettia.
Sähkö, johtuminen ja elektronit
Monet sähköiset ilmiöt perustuvat elektronien liikkeeseen. Tavallinen sähkö on käytännössä suuri joukko elektroneja, jotka liikkuvat johtimissa tai muissa johtimien kaltaisissa materiaaleissa. Hyvät johtimet, kuten metallit, sisältävät vapaita elektroneja, jotka liikkuvat helposti; eristeissä vapaita elektroneja on hyvin vähän. Puolijohteet mahdollistavat elektronien ja aukkojen määrän ja liikkuvuuden säätelyn, mikä on modernin elektroniikan perusta (transistorit, diodit).
Kvanttifysiikka ja sovellukset
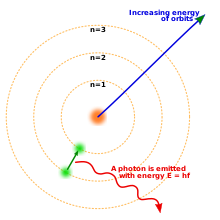
Elektronien käyttäytymistä selittää kvanttimekaniikka: elektronien tiloja kuvaavat orbitaalit, energiatason kvantittuminen määrää spektrejä ja fotonien kanssa tapahtuvat vuorovaikutukset (esim. fotoelektrinen ilmiö) ovat keskeisiä. Elektroneja hyödynnetään laajasti tekniikassa ja tutkimuksessa: elektronimikroskoopit hyödyntävät elektronien lyhyttä aallonpituutta korkearesoluutioiseen kuvantamiseen, putkissa ja näyttötekniikoissa käytetään katodipurkauksia, ja elektroniikka perustuu elektronien ohjattuun liikkeeseen puolijohdelaitteissa.
Lisätietoa ja huomioita
- Elektronin antipartikkeli on positroni (e+); kohtaaminen positronin kanssa johtaa annihilaatioon ja fotonien syntyyn.
- Beetahajoamisessa (β-hajoaminen) yksi syntyvistä hiukkasista voi olla elektroni tai positroni, ja prosessit liittyvät heikkoon vuorovaikutukseen.
- Elektronin energiaa mitataan usein elektronivoltteina (eV), mikä on kätevä yksikkö atomifysiikassa ja sovelluksissa.
Elektroni on siis keskeinen hiukkanen sekä atomien sisäisessä rakenteessa että käytännön teknologioissa. Sen pieni massa, varaus ja kvanttiluonne tekevät siitä avaintekijän sekä kemiallisissa sidoksissa että sähkötekniikan ilmiöissä.