Nitriitti on ioni. Sen kemiallinen kaava on NO2– . Se sisältää typpeä hapetusasteessa +3. Nitriitit ovat yleensä voimakkaita hapettimia. Useimmat niistä ovat värittömiä kiteisiä yhdisteitä. Natriumnitriitti on yleinen nitriitti. Ne ovat myös heikkoja pelkistimiä, jotka hapettuvat nitraateiksi (NO3– ).
Rakenne ja elektronijakauma
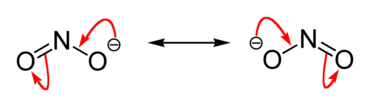
Nitriitti-ioni NO2– on epälineaarinen (V-muotoinen) molekyyli, jossa typpi on sidoksissa kahteen happiatomiin. Ionissa on resonanssirakenteita, mikä merkitsee, että typpi–happi-sidosten pituudet ovat keskimääräisiä yksittäis- ja kaksoissidosten välillä. Resonanssi selittää myös ioniin liittyvän varauksen jakaantumisen happiatomien ja typen kesken.
Kemialliset ominaisuudet
- Happamuus/emäksisyys: Nitriitti toimii emäksisenä ionina vesiliuoksissa; se voi reagoida protoneja vastaanottaen muodostuen nitriittihaposta (HNO2), joka on heikko happo ja epävakaa.
- Redox-ominaisuudet: Nitriitit voivat toimia sekä pelkistiminä että hapettimina olosuhteista riippuen. Tyypillinen suunta on nitriitin hapettuminen nitraatiksi (NO3–) tai sen pelkistyminen erilaisiksi typpiyhdisteiksi (esim. typpioksiduuli NO, typpioksiduuli N2O, typpi N2 tai ammonium NH4+) biologisissa tai kemiallisissa prosesseissa.
- Liukoisuus ja olomuoto: Useimmat nitriittisuolat ovat vesiliukoisia ja värittömiä kiteisiä aineita. Esimerkiksi natriumin- ja kaliumnitriitit muodostavat helposti vesiliuoksia.
Valmistus ja esiintyminen
Nitriittejä syntyy teollisesti ja luonnossa. Teollisesti nitriittisuoloja valmistetaan usein reduktioreaktiolla nitraateista tai suoraan natrium- tai kaliumnitraateista saatavilla prosesseilla. Luonnossa nitriitti on välituote typen kierrossa: mikro-organismit voivat pelkistää nitraatteja nitriitiksi (nitrate → nitrite) sekä toisaalta nitriitti voi pelkistyä edelleen typpikaasuksi denitrifikaation yhteydessä tai hapettua takaisin nitraatiksi. Nitriittejä esiintyy maaperässä, pohjavedessä ja jätteenkäsittelyvesissä.
Käyttö ja esimerkkiyhdisteet
- Natriumnitriitti (NaNO2) — laajasti käytetty elintarvikkeiden säilöntäaineena erityisesti lihavalmisteissa, korroosionestoaineena ja kemianteollisuuden raaka-aineena.
- Kaliumnitriitti (KNO2) — vastaava käyttöalue kuin natriumnitriitillä, käytetään mm. laboratorioissa ja joissain teknisissä sovelluksissa.
- Kalsiumnitriitti — käytetään korroosionestoaineissa ja betonin lisäaineissa tilanteissa, joissa halutaan hidastaa raudan korroosiota.
Terveyteen ja ympäristöön liittyvät näkökohdat
Nitriiteillä on sekä hyödyllisiä että haitallisia vaikutuksia. Elintarvikesäilöntänä nitriitit estävät Clostridium botulinumin kaltaisten patogeenien kasvua ja antavat rakenteelle ja maulle tyypillisen punertavan värin. Toisaalta nitriitit voivat reagoida sekundaaristen amiiniyhdisteiden kanssa muodostaen nitrosamiineja, jotka ovat osoittautuneet karsinogeenisiksi eläinkokeissa. Tämän vuoksi elintarvikkeisiin lisättävien nitriittien määrää valvotaan tiukasti.
Lisäksi nitriitti voi hapettaa hemoglobiinin muotoon methemoglobiinia, joka heikentää hapen kuljetusta veressä — erityisesti imeväisillä ja pienillä lapsilla riski methemoglobinemialle on korostunut, jos juomavedessä on runsaasti nitriittejä.
Analytiikka ja tunnistaminen
Yleinen laboratoriomenetelmä nitriitin määrittämiseen on Griessin reaktio, jossa nitriitti reagoi typpiyhdisteiden kanssa muodostaen värjäytyvän azo-yhdisteen. Myös kromatografisia ja spektrometrisia menetelmiä käytetään tarkempaan analyysiin ympäristö- ja elintarvikenäytteissä.
Turvallisuus ja säilytys
- Monet nitriittisuolat ovat oksidoivia aineita, joten niitä tulee säilyttää poissa helposti syttyvistä tai orgaanisista aineista.
- Varastointi kuivissa, viileissä ja hyvin ilmastoiduissa tiloissa vähentää hajoamis- ja reaktiovaaraa.
- Käsiteltäessä nitriittejä on noudatettava kummankin aineen käyttöturvallisuustietoja: käytettävä suojavarusteita ja välttävä pölyn hengittämistä tai suoraa ihokosketusta.
Yhteenveto
Nitriitti (NO2–) on kemiallisesti monipuolinen ioni, jonka kemiallinen käyttäytyminen vaihtelee olosuhteista riippuen — se voi toimia sekä hapettimena että pelkistimenä. Nitriitit ovat tärkeitä teollisuudessa, elintarviketeollisuudessa ja luonnon typen kiertokulussa, mutta niiden käyttöön liittyy terveys- ja ympäristöriskejä, jotka vaativat sääntelyä ja asianmukaista käsittelyä.