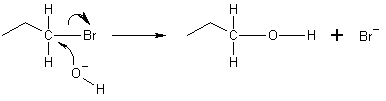
Nukleofiili on laji, joka luovuttaa elektroniparin elektrofiilille muodostaakseen kemiallisen sidoksen reaktiossa. Kaikki molekyylit tai ionit, joilla on vapaa elektronipari, voivat käyttäytyä nukleofiileinä; tätä elektroniparia kutsutaan yksinäiseksi elektronipariksi. Koska nukleofiilit luovuttavat elektroneja, ne sopivat Lewisin emästen määritelmään. Nukleofiilit voivat reagoida monin tavoin: ne voivat korvata toisen ryhmän orgaanisissa yhdisteissä, addetoitua kaksinkertaisiin sidoksiin tai hyökkää sähköisesti varattuihin keskuksiin (esim. karbokationeihin tai karbonyyliryhmiin).
Nukleofiilisyys — mitä se tarkoittaa
Nukleofiilinen kuvaa nukleofiilin vetovoimaa positiivisesti tai osittain positiivisesti varattuihin atomeihin (ytimiin). Termillä nukleofiilisyys, jota joskus kutsutaan myös nukleofiilin voimakkuudeksi, tarkoitetaan aineen kykyä luovuttaa elektronipari ja reagoida elektrofiilin kanssa. Nukleofiilisyys on suhteellinen ominaisuus: samaan aikaan se voi riippua sekä reagenssista itsestään että reaktioolosuhteista (liuotin, lämpötila, konsentraatio).
Tekijät, jotka vaikuttavat nukleofiiliseen käyttäytymiseen
- Varauksen suuruus: negatiivisesti varautuneet ionit (esim. OH−, RO−) ovat yleensä neutraaleja molekyylejä vahvempia nukleofiilejä.
- Elektronegatiivisuus: vähemmän elektronegatiiviset atomit luovuttavat elektronejaan helpommin ja ovat usein vahvempia nukleofiilejä.
- Polarisoituvuus: suuremmat, helposti polarisoituvat ionit (esim. I−, Br−) voivat olla hyviä nukleofiilejä etenkin protisissa liuottimissa, koska ne stabiloivat varausta tehokkaasti.
- Steroottinen este: suurikokoiset tai tukkoiset ryhmät ympärillä vähentävät pääsyä reaktiokeskittymään ja heikentävät nukleofiilisuutta.
- Resonanssi: resonanssin kautta delokalisoitu elektroniheikko vähentää nukleofiilisuutta verrattuna tilanteeseen, jossa elektronipari on paikallinen.
- Liuotin: protiset liuottimet (vesi, alkoholit) solvoivat pieniä, kovia ioneja (esim. F−) tehokkaasti ja heikentävät niiden nukleofiilisuutta; aprotiset polaariset liuottimet (esim. DMSO, DMF) suosivat kovia nukleofiilejä ja edistävät SN2-reaktioita.
Nukleofiilisyys vs. emäksisyys
Nukleofiilisyys ja perussyvyys (emäksisyys) liittyvät toisiinsa mutta eivät ole sama asia. Molemmat kuvaavat elektroniparin lähettämisen halukkuutta, mutta:
- Emäksisyys mittaa kykyä sitoa protoni (H+) ja perustuu yleensä tasapainotilaan (thermodynamiikka).
- Nukleofiilisyys on kinetiikkaa: se kuvaa reaktionopeutta, jolla nukleofiili hyökkää elektrofiiliin (esim. SN2-reaktiossa). Siksi aine voi olla vahva emäs mutta heikko nukleofiili tietyissä olosuhteissa ja päinvastoin.
Tyypilliset nukleofiiliset reaktiot
Yleisimmät nukleofiiliset prosessit orgaanisessa kemiassa ovat:
- Nukleofiilinen substituutio — kaksi päämekanismia:
- SN2: concerted (yhteinen) mekanismi, jossa nukleofiili hyökkää ja lähtöryhmä poistuu samanaikaisesti. Reaktionopeus riippuu sekä substraatista että nukleofiilistä (bimolekulaarinen). Steriikka ja hyvä lähtöryhmä vaikuttavat merkittävästi.
- SN1: unimolekulaarinen mekanismi, jossa ensin muodostuu karbokationi (lähtöryhmän lähtö), ja nukleofiili liittyy vasta myöhemmin. Reaktionopeus riippuu pääasiassa substraatin kyvystä muodostaa karbokationi.
- Solvolyysi — neutraalien nukleofiilien, kuten alkoholien ja veden, osallistumista reaktioon kutsutaan solvolyysiksi (liuotin toimii nukleofiilina). Neutraaleja nukleofiilisiä reaktioita liuottimien kanssa kutsutaan usein solvolyysireaktioiksi.
- Nukleofiilinen additio karbonyylielementteihin — esim. hydrideilla (LiAlH4, NaBH4) tai karbonaattien nukleofiileillä additio C=O-ryhmiin.
- Nukleofiilinen konjugaatio (1,4-additio) — α,β-epätyydyksissä nukleofiili voi addetoitua konjugoituneeseen järjestelmään.
Esimerkkejä yleisistä nukleofiileistä
- Hydroksidi (OH−), alkoksidi (RO−)
- Halidi-ionit: F−, Cl−, Br−, I−
- Syanidi (CN−)
- Ammoniakki (NH3) ja amiinit (RNH2)
- Tioli-ionit (RS−) ja tiolit (RSH)
- Vesi (H2O) ja alkoholit toimivat neutraaleina nukleofiileinä solvolyysissä
Käytännön huomioita ja reaktiokinetiikka
- Lähtöryhmän laatu: hyvä lähtöryhmä (esim. tosylaatit, bromidi, jodidi) helpottaa substituutioreaktioita.
- Temperatuuri ja konsentraatiot: SN2-tyyppisissä reaktioissa nukleofiilin konsentraatio vaikuttaa suoraan reaktionopeuteen.
- Soveltuvuus synteesissä: valitsemalla oikea nukleofiili, liuotin ja lähtöryhmä voidaan ohjata reaktiota haluttuun mekanismiin ja tuotteeseen.
Yhteenvetona: nukleofiilit ovat elektroneja luovuttavia aineita, joiden tehokkuus riippuu varauksesta, elektronegatiivisuudesta, polarisoituvuudesta, steriikasta, resonanssista ja liuottimesta. Ne osallistuvat keskeisiin orgaanisiin reaktioihin, kuten nukleofiilisiin substituutioihin ja additioihin, ja niiden käyttäytymisen hallinta on tärkeää kemiallisessa synteesissä.
Neutraaleja nukleofiilisiä reaktioita liuottimien, kuten alkoholien ja veden, kanssa kutsutaan "solvolyysireaktioiksi". Nukleofiilit voivat osallistua nukleofiilisiin substituutioreaktioihin. Näissä reaktioissa nukleofiili vetää puoleensa täydellistä tai osittaista positiivista varausta.