Röntgenkristallografia on menetelmä, jolla voidaan selvittää molekyylin kolmiulotteinen rakenne atomitasolla. Menetelmä perustuu siihen, että atomien elektronipilvi hajottaa eli sirottaa röntgensäteitä. Kun monien atomien sironnat yhdistyvät kiteessä, syntyy karakteristinen diffraktiokuvio, josta tutkija voi laskea elektronitiheyden ja päätellä, missä atomit sijaitsevat. Röntgenkristallografiaa käytetään sekä orgaanisiin että epäorgaanisiin yhdisteisiin, pienmolekyyleistä aina suuriin biomolekyyleihin kuten proteiineihin ja nukleiinihappoihin. Vaikka yleisesti näyte ei välittömästi tuhoudu, voimakas tai pitkäaikainen säteily voi aiheuttaa säteilyvaurioita, minkä vuoksi käytetään muun muassa jäädyttämistä ja nopeita ilmaisimia vaurioiden vähentämiseksi.
Miten menetelmä toimii
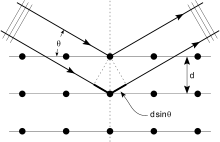
Perusperiaate on yksinkertainen: kiteeseen suunnattu röntgensäteily siroutuu kiteen tasojen kautta ja muodostaa diffraktiokuvion. Diffraktion voimakkuudesta ja kulmasta voidaan laskea kidehilassa olevien tasojen etäisyydet ja elektronitiheys. Keskeinen matemaattinen yhteys on Braggin laki, joka ilmaisee diffraktion ehdon: nλ = 2d sinθ (missä λ on säteilyn aallonpituus, d on kidevuoan välinen etäisyys, θ on sirontakulma ja n on kokonaisluku).
Kiteytys ja näytteen valmistus
Röntgenkristallografian yksi suurimmista haasteista on saada hyvälaatuinen kide. Pienmolekyylien kiteet voidaan usein saada helposti, mutta suuret biomolekyylit vaativat usein pitkäkestoista optimointia: oikea liuostiheys, lämpötila, pH ja lisäaineet voivat ratkaista onnistumisen. Kiteet asetetaan röntgenlähteen eteen — nykyisin yleisimmin käytössä ovat joko laboratoriokoneiden röntgenputket tai voimakkaammat synkrotronilähteet. Monissa tapauksissa kide jäähdytetään (~100 K) säteilyn aiheuttamien vaurioiden vähentämiseksi.
Tiedonkeruu ja laskennallinen käsittely
Kun diffraktiokuvio on mitattu, datasta erotetaan satoja tai tuhansia heijastuspeilejä (reflektioita). Seuraavat päävaiheet ovat:
- Indeksointi — kuvion heijastukset liitetään kidehilaan ja yksikkösolun (unit cell) parametreihin.
- Integrointi ja skaalaus — heijastusten intensiteetit mitataan ja yhdistetään eri kuvioista samoina heijastuksina.
- Vaiheen ongelma — diffraktiokuvio antaa heijastusten voimakkuudet, mutta ei suoraan vaiheita. Vaiheen ratkaisuun käytetään menetelmiä kuten molekyylikorvauksen (molecular replacement), isomorfinen korvaus (MIR) tai anomaalinen dispersion (SAD/MAD).
- Fourier-muunnos — intensiteetteihin ja vaiheisiin perustuen lasketaan elektronitiheyskartta, josta rakennetaan atomimalli.
- Sovitus ja hienosäätö — rakennettua mallia hiotaan vähentämällä eroa mitattujen ja mallin ennustamien heijastusten välillä (R-factor, R-free) sekä tarkistetaan geometria ja kemialliset sidokset.
Tilastot ja laatu
Röntgenkristallografian tulos ilmoitetaan usein resoluutiona (esim. 1,5 Å — pienempi arvo tarkoittaa parempaa yksityiskohtaisuutta). Mallin laadun arvioinnissa käytetään myös R- ja R-free -arvoja sekä stereokemiallisia tarkistuksia (esim. Ramachandran-analyysi proteiineille). Hyvälaatuinen rakenne antaa selkeät elektronitiheyskontuurit ja luotettavat atomipaikat.
Teknologinen kehitys
Alkuajat Braggin perheen työstä (Sir William Bragg ja Sir Lawrence Bragg, Nobel 1915) ovat johtaneet huomattavaan kehitykseen. Lawrence Bragg oli myös Cambridgen Cavendish-laboratorion johtaja aikana, jolloin James D. Watson, Francis Crick, Maurice Wilkins ja Rosalind Franklin löysivät DNA:n kaksoiskierteen vuonna 1953 — löydös nojasi röntgendiffraktiokuviin. Nykyisin käytetään kehittyneitä säteilylähteitä kuten synkrotroneja ja vapaan elektronin lasereita sekä nopeita 2D-detektoreita, jotka mahdollistavat erittäin nopean ja herkästi mitatun datan. Myös laskenta on kehittynyt: automaattinen datan käsittely, molekyylikorvaus ja tehokkaat hienosäätöalgoritmit nopeuttavat rakenneanalyysiä.
Rajoitukset ja vaihtoehtoiset menetelmät
Röntgenkristallografialla on myös rajoituksensa. Se edellyttää kiteytymistä, joten rakenteet, joita ei saa kiteytettyä, jäävät vaikeasti tutkittaviksi. Lisäksi vedyt eivät välttämättä näkyvissä heikojen elektronitiheytensä vuoksi, ellei resoluutio ole riittävän korkea. Vaihtoehtoisia menetelmiä ovat esimerkiksi kryo-elektronimikroskopia (cryo-EM) ja ydinmagneettinen resonanssi (NMR), jotka voivat täydentää röntgentutkimuksia etenkin suurissa komplekseissa tai amorfisissa näytteissä.
Sovellukset
Röntgenkristallografia on keskeinen työkalu kemialle, biologialle ja lääketieteelliselle tutkimukselle. Sitä käytetään mm.:
- uuden lääkekandidaatin ja sitoutumismekanismin selvittämiseen (rakenneavusteinen lääkesuunnittelu),
- entsyymien, reseptoreiden ja muiden proteiinien toiminnan ymmärtämiseen,
- materiaali- ja katalyyttitutkimuksiin epäorgaanisissa yhdisteissä,
- pienmolekyylien stereometrian ja konformaation määrittämiseen orgaanisessa kemiassa.
Röntgenkristallografian vanhin ja yleisin toteutus on röntgendiffraktio (XRD). Yksittäiseen kiteeseen ammutaan röntgensäteilyä, jonka sironta tuottaa kuvion. Näiden kuvioiden avulla saadaan selville atomien sijoittelu kiteen sisällä ja siten molekyylin tarkka 3D-rakenne.