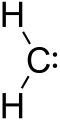Karbeeni on molekyyli, jonka keskeisenä piirteenä on yksi divalentti hiiliatomi: hiilellä on kaksi kemiallista sidosta ja lisäksi kaksi elektronia, jotka eivät muodosta sidoksia. Koska hiilen ympärillä on tällöin vain kuusi valenssielektronia, karbeeni on tyypillisesti hyvin reaktiivinen. Yksinkertaisin yleinen rakenne voidaan esittää muodossa R-(C:)-R', jossa ":" kuvaa vapaata elektroniparia tai elektroniparia/konfiguraatiota karbeenin hiilellä.
Elektroninen rakenne: singlet ja tripletti
Karbeenit esiintyvät kahdessa perus elektronimuodossa: singlet- ja tripletti-tiloina. Singlet-karbeenissa kaksi ei-sidos-elektronia muodostavat parin ja sijaitsevat yleensä samassa hybridiorbitaalissa (tyypillisesti sp2), jolloin karbeenilla on myös yksi tyhjä p-orbitaali. Triplett-karbeenissa puolestaan ne elektronit ovat sijoittuneet eri orbitaaleihin ja kummallakin on sama spin, eli karbeeni käyttäytyy diradikaalina.
Elektroninen järjestys vaikuttaa voimakkaasti karbeenin kemiallisiin ominaisuuksiin: singletit toimivat usein konservoivasti ja suorittavat esimerkiksi concerted-tyyppisiä additioreaktioita (esim. syklopropanointi), kun taas triplettit osallistuvat enemmän stepwise- tai radikaalimekanismeihin.
Stabilointi ja luokittelu
Karbeeneja voidaan stabiloida monin tavoin. Substituenttien luonne vaikuttaa singlet–tripletti-energiajakaumaan: elektronivetävät ja resonanssia tarjoavat ryhmät (esim. heteroatomit, konjugoituneet aryyliryhmät) suosivat singlet-tilaa, kun taas pelkät alkyliryhmät yleensä suosivat triplett-tilaa hyperkonjugaation ansiosta. Erityisen tunnettu ryhmä ovat heterosykliset tyylimetyylikarbeenit, kuten N-heterosykliset karbeenit (NHC), jotka ovat poikkeuksellisen stabiileja singlet-karbeeneja.
Metallikarbeenit luokitellaan usein Fischer- ja Schrock-tyyppeihin:
- Fischer-karbeenit: tyypillisesti matalan oksidaatiotilan metalli, karbeeni elektrofiilinen ja stabiloitu π-akseptoriryhmillä.
- Schrock-karbeenit: korkean oksidaation tason metalli, karbeeni nukleofiilinen ja enemmän karbanioniluonteinen.
Kemialliset reaktiot ja mekanismit
Karbeenit osallistuvat monenlaisiin reaktioihin:
- Additiot kaksoissidoksiin (esim. syklopropanointi), mikä on yleinen tapa muuntaa alkeeni syklopropaanijohdannaiseksi.
- Insertioihin yksinkertaisiin sidoksiin, kuten C–H- tai O–H-insertiot.
- Hydrogenin tai muiden atomien abstrahointiin sekä radikaalimaisiin siirtymiin, erityisesti triplettien tapauksessa.
- Yhdistymiseen muiden nukleofiilien tai elektrofiilien kanssa; karbeeni voi toimia sekä elektrofiilinä että nukleofiilinä riippuen elektronirakenteesta ja substituenteista.
Singlet- ja triplettikarbeenien reaktiomekanismit eroavat: singletit usein reagoivat konserttoidusti ja stereospesifisesti, kun taas triplettit reagoivat radikaalinevälitteisesti ja voivat johtaa eri stereokemiaan.
Syntetisointi ja esimerkit
Tavallisia karbeenien esiasteita ja generaatioreittejä ovat mm. diazoyhdisteiden hajoaminen (typellinen tapa on diazoketoneista tai diazoalkeeneista tapahtuva N2-eliminaatio), halogeno-substituoitujen prekursorien (esim. CHX3) deprotonointi, joka tuottaa dihalokarbeeneja kuten :CCl2, sekä lämpö- tai fotolyysi, joka voi synnyttää karbeeneja yksittäisinä välituotteina.
Useimmat yksittäiset orgaaniset karbeenit ovat hyvin lyhytikäisiä, mutta on kehitetty pysyviä (persistent) karbeeneja, esimerkiksi NHC-tyyppiset yhdisteet ja Arduengo-karbeenit, jotka voidaan isoloida ja karakterisoida. Lisäksi karbeeneja esiintyy tärkeissä katalyyttisissa järjestelmissä: tunnettu esimerkki on Grubbsin katalyytti, jonka kehitti Robert Grubbs — se sisältää ruteniumia ja karbeeni‑ligandin, ja sitä käytetään laajalti alkeenien metatesis‑reaktioissa.
Luotettavat analyysimenetelmät
Carbeneja ja niiden elektronista luonnetta tutkitaan useilla menetelmillä: elektronispiniresonanssi (ESR) on hyödyllinen triplettien ja radikaalien havaitsemiseen, NMR voi antaa tietoa singlet-karbeenien ympäristöstä, ja röntgenkristallografia voi paljastaa pysyvien karbeenien atomirakenteen. Spektritutkimukset yhdistettynä laskennalliseen kemiaan (DFT) auttavat ymmärtämään singlet–tripletti-eroja ja reaktiivisuutta.
Käytännön merkitys
Karbeenien kemia on keskeinen monilla alueilla: synteettisessä orgaanisessa kemiassa karbeenien avulla voidaan rakentaa kolmi- ja monimutkaisia renkaita, suorittaa insertio‑ ja funktionalisointireaktioita sekä toteuttaa selektiivisiä transformaatiota. Metallikarbeenien rooli katalyysissä (esim. alkeenien metatesis) on laajalti sovellettua teollisessa ja akateemisessa tutkimuksessa.
Yhteenvetona: karbeeni on monipuolinen mutta usein hyvin reaktiivinen hiilen divalentti muoto, jonka elektroninen rakenne (singlet tai tripletti), substituentit ja ympäristö määräävät sen kemialliset ominaisuudet ja sovellukset.