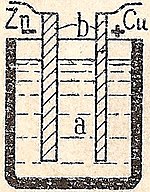
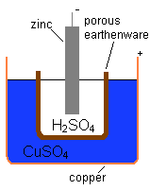
Kemiallinen kenno muuntaa kemiallisen energian sähköenergiaksi. Useimmat akut ovat kemiallisia kennoja. Akun sisällä tapahtuu kemiallinen reaktio, joka saa aikaan sähkövirran kulun. Periaatteessa kyse on kahden erilaisten aineiden välisten hapettumis–pelkistymisreaktioiden (redox) hyödyntämisestä siten, että elektroneja siirtyy aineelta toiselle ulkoisen johdon kautta — tämän elektronivirran voi käyttää sähkölaitteiden toimintaan.
Miten kemiallinen kenno tuottaa sähköä
Kemiallinen kenno koostuu yleensä kahdesta elektrodista (anodi ja katodi) ja niitä erottavasta elektrolyytistä. Lyhyesti:
- Anodi (negatiivinen napa): kemiallisessa reaktiossa aine hapettuu ja luovuttaa elektroneja.
- Kathodi (positiivinen napa): vastaanottaa elektroneja ja pelkistyy.
- Elektrolyytti: ionien johtava aine, joka sallii varauksen tasapainottamisen kennon sisällä ilman, että elektronit kulkevat suoraan elektrodien välillä.
- Elektronit kulkevat anodilta katodille ulkoisen piirin kautta — tämä elektronivirta on hyödyllinen sähköenergia.
Kennojen jännite riippuu käytetyistä kemikaaleista ja reaktioiden energiasta. Esimerkiksi tavallinen alkaliparisto antaa noin 1,5 V, NiMH- ja NiCd-kennot noin 1,2 V, ja litiumioniakut tyypillisesti noin 3,6–3,7 V per kenno.
Ladattavat ja ei-ladattavat paristot
Paristoja on kahta päätyyppiä - ladattavia ja ei-ladattavia.
Ei-ladattava akku (primääriparisto) tuottaa sähköä, kunnes sen sisältämät kemikaalit on käytetty loppuun. Tällaisia kutsutaan usein "käytä ja heitä" -paristoiksi. Yleisiä primäärikemioita ovat sinkki-hiili ja alkaliparistot.
Ladattava akku (toissijainen kenno) voidaan ladata uudelleen johtamalla sähkövirta taaksepäin kennon läpi; tämän reversoivan virran vaikutuksesta kemialliset reaktiot kääntyvät, ja akku voidaan käyttää uudelleen tuottamaan lisää sähköä. Ranskalainen tiedemies Gaston Plante keksi nämä ladattavat akut vuonna 1859 (lyijyakun periaate).
Termistössä suomen kielessä "paristo" usein viittaa kertakäyttöiseen kennon, kun taas "akku" tarkoittaa ladattavaa yksikköä — käyttö vaihtelee arkipuheessa.
Yleisiä paristokemioita ja ominaisuuksia
- Sinkki-hiili (zink-hiili): edullinen, käytetty perusparistoissa, alhainen kapasiteetti ja lyhyempi käyttöikä.
- Alkaliparisto: yleisin kertakäyttöinen paristo, parempi kapasiteetti ja varaus säilyy pitkään.
- NiCd (nikkelikadmium): varhainen ladattava tyyppi, kestävä mutta kärsii muistiefektistä ja sisältää myrkyllistä kadmiumia.
- NiMH (nikkelimetallihydridi): korvasi monissa sovelluksissa NiCd:n, suurempi kapasiteetti ja vähemmän ympäristöhaittoja.
- Lyijyakku: käytetään autoissa; raskas mutta suuritehoinen ja erittäin kierrätettävä. Auton 12 V akku koostuu kuudesta 2 V kennosta sarjassa.
- Litium-ioni (Li-ion): korkea energiatiheys, kevyt ja yleinen kannettavissa laitteissa ja sähköautoissa; vaatii suojaelektroniikkaa ylikuormituksen ja ylikuumenemisen estämiseksi.
Paristojen kapasiteetti mitataan yleensä milliampeeritunteina (mAh) tai ampeeritunteina (Ah). Energiatiheys ilmoitetaan wattitunteina per kilogramma (Wh/kg).
Käyttö, turvallisuus ja ympäristö
- Älä oikosulje paristoja tai akkuja — se voi aiheuttaa voimakkaan virtapiikin, kuumenemisen ja jopa palon.
- Sekoitettujen merkkien tai eri ikäisten paristojen käyttäminen yhdessä voi aiheuttaa epätasaista kuormitusta ja vuotoja; laitteissa suositellaan käyttämään samanlaisia ja saman ikäisiä kennoja.
- Lataus: käytä aina valmistajan suosittelemaa laturia ja latausprofiilia. Litiumakkuja ei tule yliladata tai ladata liian korkeassa lämpötilassa; se voi aiheuttaa lämmönnousun ja harvinaisissa tapauksissa thermal runaway -ilmiön.
- Itsepurkautuminen: ladattavat kennot menettävät varauksensa hitaasti myös käyttämättöminä. NiMH-kennoilla on korkeampi itsepurkautuminen kuin litium-ioni-kennoilla.
- Kierrätys ja hävittäminen: monet paristot sisältävät raskasmetalleja tai muita haitallisia aineita. Esim. lyijyakut ja käytetyt litiumakut tulee viedä asianmukaisiin kierrätyspisteisiin. Lyijyakut ovat erittäin kierrätettyjä, kun taas litiumakkujen kierrätys on haastavampaa mutta tärkeää.
- Selkeät merkkaukset: paristoissa on yleensä navat merkittynä + ja −. Myös muodot (AA, AAA, C, D, 9 V) ovat standardoituja fyysisiä kokoja, joita laitteet käyttävät.
Käyttökohteet ja esimerkkejä
Paristoja on monen muotoisia ja kokoisia, hyvin pienistä leluissa ja kameroissa käytettävistä paristoista autoissa käytettäviin paristoihin ja jopa suurempiin paristoihin. Sukellusveneissä tarvitaan erittäin suuria akkuja. Sähköajoneuvot käyttävät suuria litiumioniakkupaketteja, kun taas kannettavat laitteet hyötyvät kevyistä ja korkeatiheisistä kennoista.
Lyhyt historiallinen viite: ensimmäinen elektrochemiallinen paristo kehitettiin Alessandro Voltan voltaattisessa pinossa noin 1800, Daniell-kenno toi käytännöllisemmän ja stabiilimman lähteen myöhemmin, ja Gaston Planten kehitys 1859 johti käytännölliseen ladattavaan lyijyakkuun.
Yhteenvetona: kemiallinen kenno tuottaa sähköä kontrolloidulla kemiallisella reaktiolla, ja eri kennotyypit soveltuvat eri käyttötarkoituksiin riippuen energiatiheydestä, kustannuksista, turvallisuudesta ja kierrätettävyydestä. Oikea käyttö, lataus ja hävittäminen pidentävät kennon käyttöikää ja vähentävät ympäristövaikutuksia.