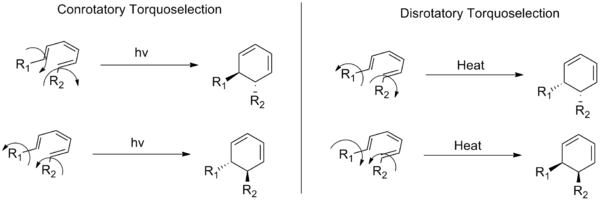
Konrotaatio ja disrotaatio kuvaavat sähkösyklisten reaktioiden kahden eri rotaatiomoodin stereokemiaa (eräs orgaanisten kemiallisten reaktioiden tyyppi). Konjugoidun kaksoissidosjärjestelmän päissä olevat substituentit pyörähtävät renkaan avautumisen tai sulkeutumisen aikana joko samaan suuntaan (konrotaatio, samaa kierrossuuntaa—myötä- tai vastapäivään) tai vastakkaisiin suuntiin (disrotaatio). Konrotaatiossa päätyatomien substituentit kääntyvät samaan suuntaan; disrotaatiossa ne kääntyvät vastakkaisiin suuntiin.
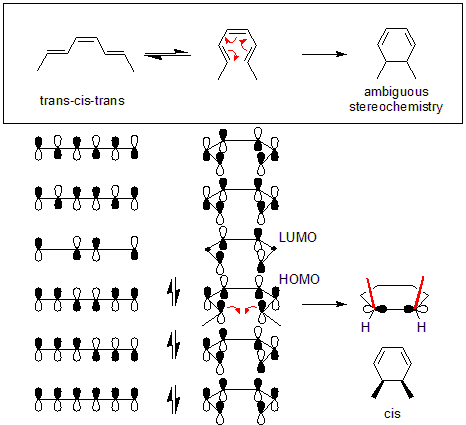
Selkeä esimerkki on trans–cis–trans‑2,4,6‑oktatrieenin muuntuminen cis‑dimetyylisykloheksadieeniksi (kuvan yläosa). Tässä tapauksessa pericyklisten orbitaalien symmetria edellyttää disrotatorista sulkeutumista: oktatrieenin korkeimmin miehitetyn molekyyliorbitaalin (HOMO) faasijärjestely vaatii, että päätyjen p- (π) orbitaalit liikkuvat vastakkaisiin suuntiin, jotta muodostuva σ‑sidos saa oikean symmetrian ja elektronitiheyden.
Säännöt ja kirjaimellinen muistisääntö
Orbitaalimekaniikka ja Woodward-Hoffmannin säännöt antavat yksinkertaisen tavan ennustaa, kumpi rotaatiomoodi tapahtuu. Perussääntö voidaan esittää elektronien lukumäärän avulla:
- Termiset (lämpöä käyttäen tapahtuvat) elektrosykliset reaktiot: jos systeemissä on 4n + 2 π‑elektronia, sulkeutuminen/muutokset noudattavat disrotatorista käyttäytymistä; jos systeemissä on 4n π‑elektronia, ne noudattavat konrotatorista käyttäytymistä.
- Fotokemialliset (valoindusoidut) elektrosykliset reaktiot: tilanteet ovat päinvastaiset eli 4n + 2‑järjestelmät reagoivat konrotatorisesti ja 4n‑järjestelmät disrotatorisesti.
Tämä johtuu orbitaalisen symmetrian säilymisestä pericyklisissä reaktioissa: sulkeutuminen tai avautuminen tapahtuu siten, että HOMO:n (tai valtion kriittisen orbitaalin) faasit sopivat yhteen uuden sidoksen muodostamisen aikana. Usein tätä havainnollistetaan HOMO‑kaavioilla, joissa tarkastellaan π‑orbitaalien vaiheparametreja päätyympäristöissä.
Esimerkkejä ja käytännön seuraukset
- 4π‑järjestelmä (esim. butadieeni) — lämpö: konrotaatio. Tämä johtaa tiettyihin stereospecificiteetteihin tuotteessa, eli lähtökonfiguraatiot määrittelevät tuotteen stereokemian.
- 6π‑järjestelmä (esim. (hexa)trieeni → sykloheksadieeni) — lämpö: disrotaatio (kuten oktatrieeni‑esimerkissä yllä).
- Jos samaa reaktiota indusoidaan valolla, rotaatiosuunnat vaihtuvat yllä esitetyllä tavalla.
Stereospesifisyys tarkoittaa, että lähtöalkyleiden geometria (cis/trans) määrää syntyvän renkaan substituenttien suhteellisen orientaation (esim. syn/anti), eikä se hajoa satunnaisesti. Tämä tekee elektrosyklisistä reaktioista hyödyllisiä stereoselektiivisessä synteesissä.
Woodward–Hoffmannin laajempi näkökulma
Woodward–Hoffmannin säännöt kokoavat edellä mainitut havainnot laajemmaksi periaatteeksi: pericyklisissä reaktioissa orbitaalinen symmetria tulee säilyttää, ja tästä seuraa, että tietyt reaktiot ovat "sallitumpia" (symmetrisesti sallittuja) kuin toiset sekä lämpö‑ että fotokemiallisissa olosuhteissa. Säännöt voidaan johtaa korrelaatiokaavioilla tai HOMO/LUMO‑analyyseilla ja niitä voi laajentaa muihin pericyklisiin reaktioihin (esim. sigmatransferiin, cycloadditioihin).
Käytännössä tämä tarkoittaa, että ennen kuin ennustat elektrosyklisen reaktion stereokemiaa, on hyvä laskea tai hahmottaa kyseisen polyneen HOMO:n faasijärjestely. Monissa synteettisissä suunnitelmissa Woodward–Hoffmannin säännöt ovat olleet ratkaisevia reaktion suunnittelussa ja selektiivisyyden hallinnassa.
Seuraavassa kuvassa näkyy myös ero konrotatoristen ja disrotatoristen reaktioiden välillä: