Kemiassa konjugoitu systeemi tarkoittaa useiden vierekkäisten p-orbitaaleista koostuvaa rakennetta, jossa on delokalisoituneita elektroneja. Konjugoituneet järjestelmät syntyvät yleensä, kun peräkkäiset moninkertaiset sidokset (kakso- tai kolmoissidokset) ovat erotettuina yksittäisillä sidoksilla tai kun yksinäiset elektroniparit tai varaukset voivat osallistua pi-järjestelmään. Tällaiset järjestelmät alentavat usein molekyylin kokonaisenergiaa ja lisäävät sen vakautta verrattuna täysin paikallisiin sidoksiin.
Mikä on konjugaatio ja miten se syntyy?
Konjugaatio perustuu p-orbitaalien päällekkäisyyteen yksittäisten (sigmasidoksen) yli kulkevien pi-orbitaalien muodostamiseksi. Kun vierekkäisten atomien p-orbitaalit ovat samassa tasossa ja päällekkäin, niiden pi-elektronit voivat delokalisoitua koko järjestelmän yli. Tämä tarkoittaa, että Pi-elektronit eivät enää kuulu yksittäiseen sidokseen tai atomiin, vaan muodostavat yhteisen elektronipilven useamman atomin yli.
Orbitaalikuvaus ja kvanttimekaniikka
Konjugoidun systeemin kvanttimekaaninen kuvaus tehdään usein molekyyliorbitaaliteorian avulla: erillisten p-orbitaalien kombinaatioista syntyy sidossidoksia (bonding), ei-sidossidoksia (antibonding) ja mahdollisesti ei-sidossidoksia. Konjugaation pituus vaikuttaa energiaeroihin — mitä pidempi delokalisaatio, sitä pienempi HOMO–LUMO-ero ja sitä enemmän järjestelmä absorboi valoa pidemmällä aallonpituudella (ns. bathokrominen siirtymä).
Aromaatisuus ja erikoistapaukset
Aromaatisuus on konjugaation erikoistapaus, jossa syklisessä järjestelmässä delokalisoituneet pi-elektronit antavat poikkeuksellisen suuren stabilisaation. Hückelin 4n+2 -sääntö kuvaa, millainen elektronimäärä johtaa aromaattisuuteen (esim. benseneen). Kaikki aromaattiset yhdisteet ovat konjugoituja, mutta kaikki konjugoituja järjestelmät eivät ole aromaattisia.
Rakenteelliset ja elektroniset merkit konjugaatiosta
- Sidospituudet: Konjugaatiossa sidospituudet poikkeavat puhtaista yksittäis- ja kaksoissidoksista — ne ovat usein välimaastossa, mikä näkyy röntgen- ja spektroskopiatutkimuksissa.
- Planaarisuus: Tehokas p-orbitaalien päällekkäisyys edellyttää yleensä atomien planaarista tai lähes planaarista asettelua. Kierteiset tai epäplanaariset muodot heikentävät konjugaatioita.
- Resonanssi: Konjugointia kuvataan usein resonanssihyrrillä (resonanssirakenteet), jotka auttavat ymmärtämään elektronien delokalisaatiota ja stabiilisuutta.
Vaikutukset kemiallisiin ja fysikaalisiin ominaisuuksiin
Konjugaatio muuttaa merkittävästi molekyylien käyttäytymistä:
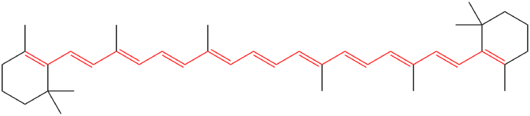
- Spektroskopia: Konjugaation piteneminen johtaa tyypillisesti punaiseen siirtymään UV–vis-spektrissä (alhaisempi energia-absorptio), minkä vuoksi pitkät konjugoidut järjestelmät voivat olla värillisiä.
- Reaktiivisuus: Konjugoidut diinit käyttäytyvät eri tavoin kuin yksittäiset alkeenit — esimerkiksi ne voivat reagoida sekä 1,2- että 1,4-additiolla. Konjugaatio stabiloi myös kationeja ja radikaaleja (esim. anionit/karbokationit allyylisijainnissa).
- Sähköjohtavuus ja puolijohdeominaisuudet: Pitkät konjugoidut polymeeriketjut ja kaksiulotteiset verkot voivat johtaa sähköä (esim. johtavat polymeerit, grafiitissa esiintyvä delokalisaatio tai hiilinanoputkissa).
- Stabilisaatio: Delokalisaatio vähentää reaktiivisten väliainemuotojen energiatasoa, mikä vaikuttaa reaktiokiertoihin ja tuotteen valintaan.
Esimerkkejä ja käytännön merkitys
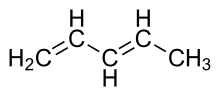
- Yksinkertaiset konjugoidut yhdisteet: 1,3-butadieeni — delokalisaatio aiheuttaa erikoisia reaktiopolkuja (Diels–Alder-enteraatio).
- Aromaatit: bentseeni — esimerkki täysin delokalisoituneesta kuuden elektronin syklistä järjestelmästä.
- Konjugoidut polymeerit: polyasetyyleeni tai johtavat polymeerit, joita käytetään elektroniikassa ja optoelektroniikassa.
- Hiilipohjaiset materiaalit: grafiitissa ja hiilinanoputkissa delokalisoituneet elektronit antavat erikoisia mekaanisia ja sähköisiä ominaisuuksia.
Muita huomioita
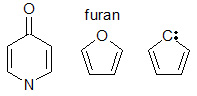
- Heteroatomit: Heteroatomien (esim. O, N, S) lone pair -elektronit voivat osallistua konjugaatioon, mikä vaikuttaa elektronitiheyteen ja emäksisyyteen/reaktiivisuuteen.
- D-orbitaalit: Suurempien atomien d-orbitaalit voivat myös osallistua konjugaatioon ja laajentaa delokalisaatiota, kuten mainittiin alkuperäisessä kuvauksessa.
- Rajoitukset: Kaikki "peräkkäiset" moninkertaiset sidokset eivät ole automaattisesti konjugoituneita — tarvitaan oikea geometria (orbitaalien kohdistus) ja elektronirakenne. Cross-konjugaatio ja konjugoinnin katkeaminen (esim. sp3-hiili) estävät delokalisaation.
- Teoreettiset menetelmät: Konjugaation kvantitatiiviseen kuvaukseen käytetään Hückelin lähestymistapaa, molekyyliorbitaalilaskentaa ja modernimpia menetelmiä kuten DFT:ää.
Yhteenvetona: konjugaatio on keskeinen käsite orgaanisessa kemiassa ja materiaalitieteissä, koska se selittää monia molekyylien stabiilisuuteen, värähtelyihin, reaktiivisuuteen ja sähkönjohtavuuteen liittyviä ilmiöitä. Konjugaation laajuus, geometria ja osalliset atomityypit määräävät käytännössä sen vaikutuksen kuhunkin järjestelmään.