Sähkösyklinen reaktio (elektrosyklinen): määritelmä, mekanismi ja esimerkit
Sähkösyklinen reaktio (elektrosyklinen) – selkeä määritelmä, mekanismi ja käytännön esimerkit (Woodward–Hoffmann, torquoselektiivisyys). Opas renkaiden synteesiin ja stereokemiaan.
Orgaanisessa kemiassa sähkösyklinen reaktio (elektrosyklinen reaktio) on eräänlainen perisyklinen uudelleenjärjestelyreaktio, jossa pi-elektronien liikkuessa syntyy tai häviää yksi piisidos ja vastaavasti muodostuu tai katkeaa yksi sigmasidos. Toisin sanoen reaktiossa tapahtuu concerted-siirtymä, jossa elektronit siirtyvät syklistä reittiä pitkin, ilman välivaiheen muodostumista, ja tuotteen ja lähtöaineen orbitaalien symmetria säilyy Woodward–Hoffmannin periaatteiden mukaisesti. Sähkösyklisillä reaktioilla on seuraavat olennaiset ominaisuudet:
- reaktiota voi indusoida valo (fotokemiallinen reaktio) tai lämpö (terminen reaktio); reaktion stereokemia riippuu usein siitä, kumpi tapa on käytössä;
- reaktiotapa määräytyy subsystemin pii-elektronien lukumäärän mukaan, erityisesti siinä osassa, jossa on eniten piisidoksia (esim. 4n tai 4n+2 π-elektronia);
- sähkösyklinen reaktio voi sulkea renkaan (sähkösykloituminen) tai avaada renkaan;
- reaktion stereospesifisyys määräytyy sen mukaan, kulkeeko reaktio konrotatorisen vai disrotatorisen siirtymätilan kautta—tämän ennustavat Woodward–Hoffmannin säännöt sekä orbitaalien symmetrian säilyminen.
Mekaniikka ja orbitaalinen selitys
Sähkösyklinen reaktio on concerted-perisyklinen prosessi, jossa pi-orbitaaleista muodostuu syklistä elektronipilveä siirtymätilan kautta. Reaktion sallituksi tai kielletyksi tulee se, että lähtöaineen ja tuotteen korkeimmin miehitettyjen molekyyliorbitaalien (HOMO) symmetria pystyy korreloitumaan jatkuvasti reaktion edetessä. Tätä selitetään kahdella yleisesti käytetyllä tavalla:
- Woodward–Hoffmannin säännöt: kertovat, että orbitaalien symmetrian säilyminen määrää, onko reaktio termisesti tai fotokemiallisesti sallittu ja onko siirtymätila konrotatorinen vai disrotatorinen.
- Frontier-orbitaaliteoria (HOMO/LUMO): selittää, miten reagoivien orbitaalien vaiheet ja amplitudit määrittävät, mikä rotaatiotapa (kon- tai disrotatorinen) johtaa edulliseen (energiaa alhaisempaan) siirtymätilaan.
Terminen vs. fotokemiallinen käytös (4n vs. 4n+2 π-elektronia)
Yleinen sääntö sähkösyklisille reaktioille liittyy pii-elektronien lukumäärään:
- 4n π-elektronia (esim. 4 π): termisesti reaktiot etenevät tyypillisesti konrotatorisesti, kun taas fotokemiallisesti ne etenevät disrotatorisesti.
- 4n+2 π-elektronia (esim. 6 π): terminen reaktio on yleensä disrotatorinen ja fotokemiallinen konrotatorinen.
Nämä käyttäytymiset johtuvat HOMO:n ja fotoneja absorboineen eksitoidun tilan orbitaalikonfiguraation eroista: eksitoidussa tilassa muuttuu täyttöaste ja symmetria, mikä kääntää sallitun rotaation suunnan.
Stereokemia: konrotatorinen vs. disrotatorinen
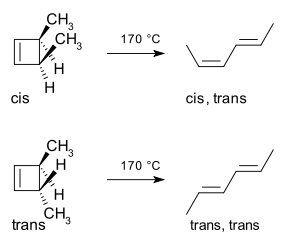
Konrotatorisessa liikkeessä molemmat reagoivan siteen päät pyörivät samaan suuntaan, kun taas disrotatorisessa ne pyörivät vastakkaisiin suuntiin. Tämä johtaa erilaisiin stereoisomeerisiin tuotteisiin, ja reaktio on usein stereospesifinen eli lähtöaineen konfiguraatio määrittää tuotteen stereokemian. Konkreettinen esimerkki on 3,4-dimetyylisyklobuteenin terminen rengasavaus:
Cis-isomeeri tuottaa vain cis,trans-2,4-heksaadieenia, kun taas trans-isomeeri antaa trans,trans-dieenin. Tämä seuraa siitä, että rengas avautuu disrotatorisesti siten, että syntyvien p-orbitaalien vaiheet vastaavat butadieenin HOMO:n vaiheita.
Frontier-orbitaalimenetelmä selittää tämän: reagoivan aineen sigmasidos avautuu siten, että syntyvillä p-orbitaaleilla on sama symmetria kuin tuotteen (butadieenin) HOMO:lla. Tämä edellyttää esimerkiksi konrotatorista tai disrotatorista avautumista vastaavasti, jotta orbitaalien vaiheet sopivat yhteen. Seuraava kuva havainnollistaa prosessin:
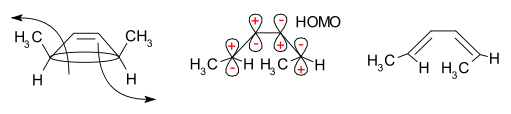
Tuloksen stereospesifisyys riippuu siis siitä, eteneekö reaktio konrotatorisen vai disrotatorisen prosessin kautta ja lähtöaineen alkuperäisestä stereokemiasta.
Torquoselektiivisyys
Torquoselektiivisyys tarkoittaa sitä, että substituenttien pyörimissuunta (”torque”) rengasavaus- tai -sulkeutumistilanteessa ei ole symmetrinen: substituentit voivat suosia toista pyörimissuuntaa, jolloin muodostuu pääasiassa yksi enantiomeeri tai diastereomeeri. Vaikka konrotatorisessa reaktiossa ideaalitapauksessa molemmat päät pyörisivät samaan suuntaan, substituenttien elektroniset ja steriiset vaikutukset voivat rajoittaa pyörimistä ja siten tuottaa torquoselektiivisen, stereoselektiivisen lopputuloksen. Torquoselektiivisuus on hyödyllinen työkalu asimmetrisessa synteesissä, koska sen avulla voidaan saavuttaa enantiomeerinen ylijäämä ilman ulkoista kemospesifistä katalyyttia.
Esimerkkejä ja sovelluksia
- Nazarovin syklisaatioreaktio: mainittu esimerkki sähkösyklisestä rengassulkeutumisesta. Kemistit hyödyntävät Nazarov-reaktiota muuntaakseen divinyyliketonit syklopentoneiksi. Reaktio etenee konsertidusti ja sen mekanismissa orbitaalien konjugaatio ja protonointi/elektrofiilinen aktivaatio ovat usein tärkeitä askelia. (Reaktion löysi Ivan Nikolajevitš Nazarov.)
- Syklobuteenin rengasavaus: kuvattu 3,4-dimetyylisyklobuteeni on klassinen esimerkki, joka demonstroi, miten lähtöaineen isomeria määrää tuotteiden stereokemian termisessä reaktiossa.
- 6π-sähkösykloituminen: konjugoitu triene (ks. heksatrieeni → sykloheksadieeni) sulkeutuu usein disrotatorisesti termisesti (4n+2 = 6 π), mikä on tärkeä askel monissa luonnontuotteiden synteeseissä.
Merkitys orgaanisessa synteesissä ja teoreettisessa kemiassa
Kemistit ja teoreettiset kemistit kiinnittävät huomiota sähkösyklisiin reaktioihin, koska ne tarjoavat selkeän yhteyden molekyylien geometriaan, orbitaalien symmetriaan ja Woodward–Hoffmannin ennusteisiin. Sähkösykliset reaktiot toimivat usein synteettisinä strategioina, joilla voidaan muodostaa renkaita tai muuttaa konfiguraatiota stereospesifisesti ilman välivaiheita. Lisäksi ne toimivat kokeellisina testeinä orbitaaliteorian ja symmetriaongelmien ymmärtämiselle.
Yhteenveto
Sähkösykliset reaktiot ovat konsertoituja, orbitaalisen symmetrian ohjaamia perisyklisiä prosesseja, joissa pi- ja sigma-sidosten välinen muutos johtaa rengasavauksiin tai -sulkeutumisiin. Woodward–Hoffmannin säännöt ja frontier-orbitaaliteoria ennustavat, millainen rotaatiotapa (kon- tai disrotatorinen) on sallitumpi termisessä tai fotokemiallisessa tilanteessa, ja torquoselektiivisyys selittää substituenttien vaikutuksen tuotteen stereokemiaan. Näiden reaktioiden ymmärtäminen on tärkeää sekä teoreettiselle orgaaniselle kemiassa että käytännön synteesimenetelmille.
Woodward-Hoffmanin säännöt
Woodward-Hoffmannin säännöt koskevat orbitaalisymmetrian säilymistä sähkösyklisissä reaktioissa.

Korrelaatiokaaviot yhdistävät reagoivan aineen molekyyliorbitaalit tuotteen molekyyliorbitaaleihin, joilla on sama symmetria. Korrelaatiokaaviot voidaan piirtää kahdesta prosessista.
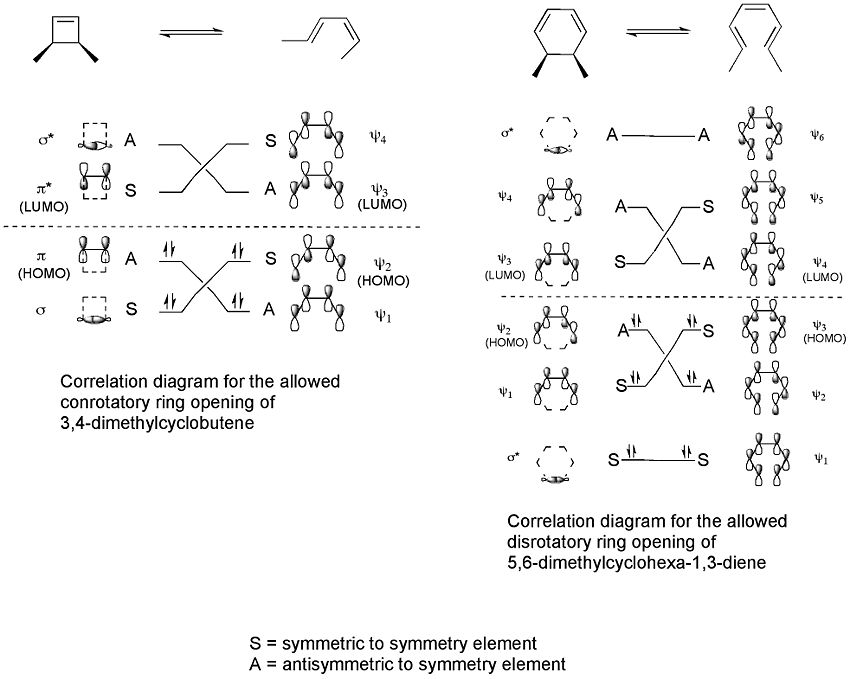
Nämä korrelaatiokaaviot osoittavat, että vain 3,4-dimetyylisyklobuteenin konrotatorinen rengasavaus on "symmetrisesti sallittua", kun taas 5,6-dimetyylisykloheksa-1,3-dieenin disrotatorinen rengasavaus on "symmetrisesti sallittua". Tämä johtuu siitä, että vain näissä tapauksissa siirtymätilassa esiintyisi maksimaalinen orbitaalien päällekkäisyys. Muodostunut tuote olisi myös pikemminkin perustilassa kuin kiihdytetyssä tilassa.
Rajamolekyyliorbitaaliteoria
Frontier Molecular Orbital Theory ennustaa, että renkaan sigmasidos avautuu siten, että syntyvillä p-orbitaaleilla on sama symmetria kuin tuotteen HOMO:lla.
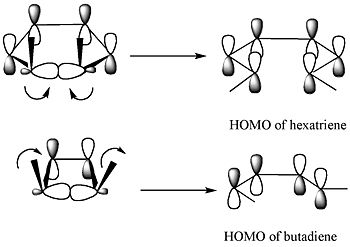
Yllä olevassa kaaviossa on kaksi esimerkkiä. 5,6-dimetyylisykloheksa-1,3-dieenin osalta (kaavion ylärivi) vain disrotatorinen moodi johtaisi p-orbitaaleihin, joilla on sama symmetria kuin heksatrieenin HOMO:lla. Molemmat p-orbitaalit pyörivät vastakkaisiin suuntiin. 3,4-dimetyylisyklobuteenin osalta (kaavion alin rivi) vain konrotatorinen moodi johtaisi siihen, että p-orbitaaleilla olisi sama symmetria kuin butadieenin HOMO:lla. P-oribtaalit pyörivät samaan suuntaan.
Erkaantuneen tilan sähkösyklisaatiot
Valo voi siirtää elektronin virittyneeseen tilaan, jossa se on korkeammalla orbitaalilla. Jännittynyt elektroni asettuu LUMO-tilaan, joka on korkeampi energiataso kuin elektronin vanha orbitaali. Jos valo avaa 3,4-dimetyylisyklobuteenin renkaan, syntyvä sähkösykloituminen tapahtuisi disrotatorisessa tilassa konrotatorisen tilan sijasta. Korrelaatiokaavio sallitun kiihdytetyn tilan renkaanavausreaktiosta osoittaa, miksi:
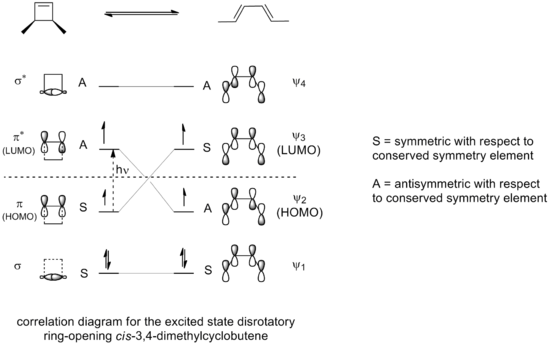
Vain disrotatorinen tila, jossa symmetria heijastustason suhteen säilyy koko reaktion ajan, johtaisi maksimaaliseen orbitaalien päällekkäisyyteen siirtymätilassa. Myös tämä johtaisi jälleen kerran sellaisen tuotteen muodostumiseen, joka on herätetyssä tilassa, jonka stabiilisuus on verrattavissa reagoivan yhdisteen herätettyyn tilaan.
Sähkösykliset reaktiot biologisissa järjestelmissä
Sähkösyklisiä reaktioita esiintyy luonnossa usein. Yksi yleisimmistä tällaisista reaktioista luonnossa on D3-vitamiinin biosynteesi.
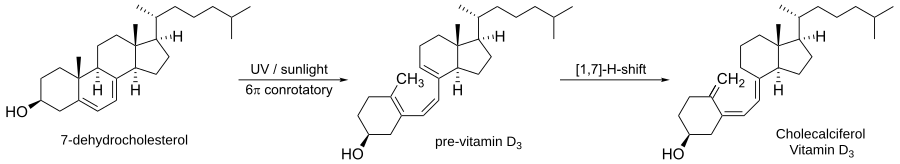
Ensimmäisessä vaiheessa valo avaa 7-dehydrokolesterolin renkaan ja muodostaa D3-esivitamiinin. Kyseessä on valokemiallisesti indusoitu konrotatorinen sähkösyklinen reaktio. Toinen vaihe on [1,7]-hydridisiirtymä D3-vitamiinin muodostamiseksi.
Toinen esimerkki on luonnossa esiintyvän oksepiinin aranotinin ja siihen liittyvien yhdisteiden ehdotettu biosynteesi.
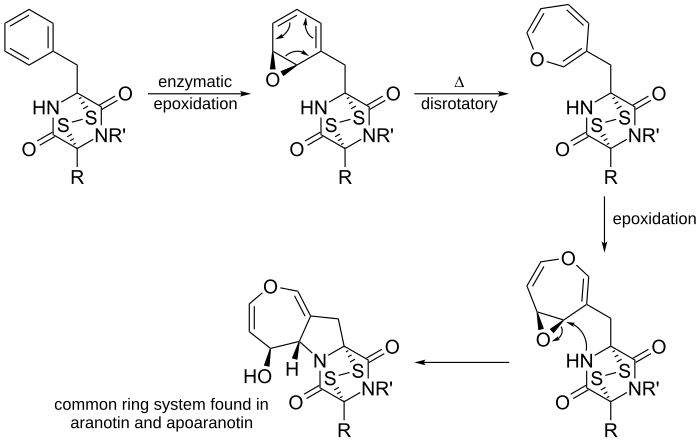
Fenyylialaniinia käytetään diketopiperatsiinin valmistukseen (ei kuvassa). Tämän jälkeen entsyymit epoksidaattavat diketopiperatsiinin arenioksidiksi. Tämä käy läpi 6π-disrotatorisen renkaan avautumisreaktion sähkösyklisaatioreaktion, jossa saadaan syklittymätöntä oksepiinia. Renkaan toisen epoksidaation jälkeen läheinen nukleofiilinen typpi hyökkää elektrofiilisen hiilen kimppuun muodostaen viisijäsenisen renkaan. Syntynyt rengasjärjestelmä on yleinen rengasjärjestelmä, jota esiintyy aranotiinissa ja sen sukulaisyhdisteissä.
Bentsonorikaradieeniditerpenoidi (A) järjestettiin uudelleen bentsosykloheptatrieeniditerpenoidiksi isosalvipuberliiniksi (B) keittämällä metyleenikloridiliuosta. Tätä muutosta voidaan pitää disrotatorisena sähkösyklisenä reaktiona, jota seuraa kaksi suprafaasista 1,5-sigmatrooppista vetymissiirtymää, kuten alla on esitetty:
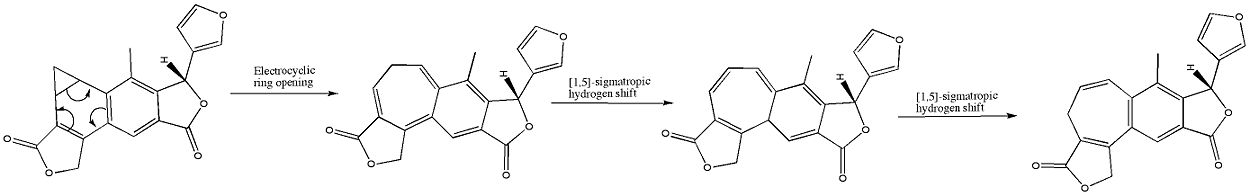
Laajuus
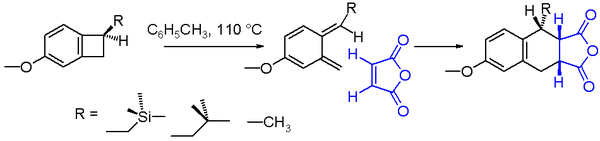
Esimerkki sähkösyklisestä reaktiosta on bentsosyklobutaanin kongrotatorinen terminen rengasavaus. Reaktiotuotteena syntyy erittäin epävakaa ortokinodimetaani. Tämä molekyyli voidaan vangita endoadditiossa vahvan dienofiilin, kuten maleiinihappoanhydridin, kanssa Diels-Alder-adduktiin. Kaaviossa 2 kuvatun bentsosyklobutaanin renkaan avaamisen kemiallisen saannon on havaittu riippuvan substituentin R luonteesta. Kun reaktioliuotin on tolueeni ja reaktiolämpötila 110 °C, saanto kasvaa metyylistä isobutyylimetyyliin ja trimetyylisilyylimetyyliin. Trimetyylisilyyliyhdisteen lisääntynyt reaktionopeus voidaan selittää piin hyperkonjugaatiolla, koska βC-Si-sidos heikentää syklobutaanin C-C-sidosta luovuttamalla elektroneja.
Biomimeettinen sähkösyklinen kaskadireaktio löydettiin tiettyjen endiandriinihappojen eristämisen ja synteesin yhteydessä:

Kysymyksiä ja vastauksia
K: Mikä on sähkösyklinen reaktio?
V: Elektrosyklinen reaktio on eräänlainen perisyklinen uudelleenjärjestäytymisreaktio, jossa tuloksena on, että yhdestä piisidoksesta tulee yksi sigmasidos tai yhdestä sigmasidoksesta piisidos.
K: Miten sähkösyklisiä reaktioita ohjataan?
V: Sähkösyklisiä reaktioita ohjataan valolla (fotoindusoitu) tai lämmöllä (terminen).
K: Miten pii-elektronien määrä vaikuttaa sähkösykliseen reaktioon?
V: Pi-elektronien määrä vaikuttaa sähkösyklisen reaktion reaktiotapaan.
K: Mitä tapahtuu sähkösyklisen prosessin aikana?
V: Elektrosyklisaatioprosessin aikana rengas voi sulkeutua.
K: Mikä määrää stereoseptiikan sähkösyklisessä reaktiossa?
V: Stereospesifisyys sähkösyklisessä reaktiossa määräytyy konrotatorisen tai disrotatorisen siirtymätilan muodostumisen perusteella, kuten Woodward-Hoffmannin säännöt ennustavat.
K: Mitä on torquoselektiivisyys suhteessa sähkösykliseen reaktioon?
V: Torquoselektiivisyydellä tarkoitetaan substituenttien pyörimissuuntaa sähkösyklisen reaktion aikana, joka voi tuottaa enantiomeerituotteita, jos se etenee konrotatorisen prosessin kautta, ja enantiomeeriylijäämää, jos se etenee torquoselektiivisen prosessin kautta.
K:Millainen esimerkki havainnollistaa, miten frontier-orbitaalimenetelmä selittää tämän?
V: 3,4-dimetyylisyklobuteenin terminen rengasavausreaktio tarjoaa esimerkin, joka havainnollistaa, miten frontier-orbitaalimenetelmä selittää, miten tämä toimii. Sigmasidos avautuu siten, että syntyvillä p-orbitaaleilla on sama symmetria kuin tuotteen (butadieenin) korkeimmin miehitetyllä molekyyliorbitaalilla (HOMO). Näin tapahtuu vain, jos rengas aukeaa konrotatorisesti, jolloin renkaan rikkinäisissä päissä olevien kahden lohkon merkit ovat vastakkaiset, kun taas disrotatorinen muodostaisi antisidoksen.
Etsiä