Pentaani on orgaaninen yhdiste, jonka kemiallinen kaava on C
5H
12. Se on alkaani, jossa on viisi hiiliatomia. Yleensä "pentaani" tarkoittaa kaikkia kolmea isomeeria (n-pentaani, isopentaani ja neopentaani). IUPAC:ssa pentaani edustaa kuitenkin vain n-pentaania. IUPACissa kaksi muuta isomeeria ovat 2-metyylibutaani ja 2,2-dimetyylipropaani. Syklopentaanin kemiallinen kaava on C
5H
10, joten se ei ole pentaanin isomeeri.
Perustiedot
Pentaanien yhteinen molekyylikaava on C5H12, ja molekyylimassa on noin 72,15 g·mol−1. Pentaanit ovat ei‑metallisia, epäpolaarisia hiilivetyjä, jotka ovat helposti haihtuvia ja heikosti vesiliukoisia mutta hyvin sekoittuvia orgaanisiin liuottimiin. Ne ovat palavia ja niiden höyryt voivat muodostaa räjähtäviä seoksia ilman kanssa.
Isomeerit ja rakenteet
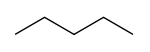
- n‑pentaani (pentaani): suora ketju, rakenne CH3–CH2–CH2–CH2–CH3. IUPAC‑nimi: pentaani. Tyypillinen kiehumispiste noin 36 °C; se on pistävän haihtuva, väritön neste huoneenlämpötilassa.
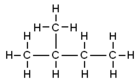
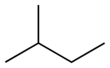
- isopentaani (2‑metyylibutaani): haarautunut ketju, rakenne (CH3)2CH–CH2–CH3. IUPAC‑nimi: 2‑metyylibutaani. Kiehumispiste noin 28 °C; myös neste huoneenlämpötilassa, mutta haihtuvampi kuin n‑pentaani.
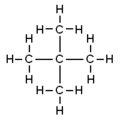
- neopentaani (2,2‑dimetyylipropaani): voimakkaasti haarautunut rakenne, keskusatomiin liittyy neljä metyyliryhmää, kaava (CH3)4C. IUPAC‑nimi: 2,2‑dimetyylipropaani. Kiehumispiste on merkittävästi alhaisempi (noin 10 °C), joten neopentaani on huoneenlämmössä kaasumaista tavallisen paineen vallitessa.
Haarautumisen lisääntyminen alentaa yleensä kiehumispistettä, koska molekyylien pinta‑ala ja siten dispersiovoimat pienenevät. Tästä syystä n‑pentaani kiehuu korkeammassa lämpötilassa kuin isopentaani ja neopentaani.
Fysikaaliset ja kemialliset ominaisuudet
- Molemminpuolisesti ne ovat värittömiä ja niillä on tyypillinen hiilivetymäinen haju.
- Sähkövarauksettomia, epäpolaarisia; käytännössä vesiliukoisuus on hyvin pieni.
- n‑Pentaanin tiheys on luokkaa 0,63 g·cm−3 (noin 20 °C); tiheys ja muut ominaisuudet vaihtelevat hieman isomeerien välillä.
- Reaktiivisuus: alkaaneille tyypillisesti suhteellisen vähän reaktiivisia, mutta ne palavat helposti ja osallistuvat halogenaatio‑reaktioihin radikaalimekanismein.
Käyttö ja esiintyminen
- Pentaanit esiintyvät luonnollisesti maakaasussa ja bensiinin/fraktioden osina. Niitä saadaan usein öljynjalostuksen sivutuotteena.
- Teollisuudessa n‑pentaania käytetään liuottimena, polttoainekomponenttina ja paisutusaineena vaahtomuovien (esim. polystyreenin) valmistuksessa.
- Isopentaanilla ja neopentaanilla on erikoiskäyttöjä, esimerkiksi koelaitteissa, jäähdytinaineissa tai tutkimuskemikaaleina. Ne voivat toimia myös standardikaasuina tai reagensseina orgaanisessa synteesissä.
Turvallisuus ja ympäristö
- Pentaanit ovat erittäin helposti syttyviä. Säilytä tiiviisti suljetuissa astioissa, poissa lämmönlähteistä ja avoimesta liekistä.
- Höyryjen hengittäminen voi aiheuttaa huimausta, päänsärkyä ja keskushermoston lamaantumista; suurina pitoisuuksina ne voivat olla turruttavia tai aiheuttaa tukehtumisen (poissulkeutumalla hapen saanti).
- Lyhytaikainen myrkyllisyys on yleensä alhainen, mutta pitkäaikaisesta altistumisesta ja suurista määristä voi seurata terveydellisiä haittoja. Käytä asianmukaisia suojavarusteita ja hyvästä ilmanvaihdosta huolehtien.
- Pentaanit ovat haihtuvia orgaanisia yhdisteitä (VOC) ja voivat edistää otsonin muodostumista troposfäärissä (kaupunkien smog‑ongelmat).
Yhteenvetona: termi "pentaani" voi arkikielessä tarkoittaa kaikkia C5H12‑isomeereja, mutta IUPAC‑terminologian mukaan pentaani tarkoittaa yksinomaan suoraa ketjua eli n‑pentaania. Sykliset C5‑yhdisteet, kuten syklopentaani (C5H10), poikkeavat kaavansa vuoksi eivätkä ole pentaanin isomeereja.