Kemiallinen kaava on tapa, jolla kemistit kuvaavat molekyyliä. Kaavassa kerrotaan, mitä atomeja ja kuinka monta kutakin atomityyppiä molekyylissä on. Joskus kaava kertoo, miten atomit liittyvät toisiinsa, ja joskus kaava kertoo, miten atomit ovat sijoittuneet tilassa.
Kirjain osoittaa, mikä kemiallinen alkuaine kukin atomi on. Alaindeksi osoittaa kunkin atomityypin lukumäärän. Esimerkiksi vetyperoksidin kaava on H 2O 2. Metaanissa on yksi hiiliatomi (C) ja neljä vetyatomia; kemiallinen kaava on CH 4. Sokerimolekyyli glukoosissa on kuusi hiiliatomia, kaksitoista vetyatomia ja kuusi happiatomia, joten sen kemiallinen kaava on C 6H 12O 6.
Kemiallisia kaavoja käytetään kemiallisissa yhtälöissä kuvaamaan kemiallisia reaktioita.
Ruotsalainen 1800-luvun kemisti Jöns Jacob Berzelius kehitti tämän järjestelmän kemiallisten kaavojen kirjoittamista varten.
Merkintätavat ja kaavatyypit
Kemiallisia kaavoja on useita tyyppejä riippuen siitä, mitä tietoa halutaan esittää:
- Molekyylikaava (molecular formula) kertoo tarkan atomiluvun molekyylissä, esim. C 6H 12O 6 (glukoosi).
- Empiirinen kaava (empirical formula) näyttää atomien suhteellisen määrän pienimpinä kokonaisina lukuina. Esimerkiksi glukoosin empiirinen kaava on CH 2O.
- Rakennekaava (structural formula) näyttää, miten atomit ovat sidoksissa toisiinsa (esim. viivoilla merkittyjä sidoksia tai rakenteellisia kaavoja). Rakennekaava antaa enemmän tietoa kuin pelkkä molekyylikaava.
- Tihennetty rakennekaava (condensed formula) on lyhennetty tapa esittää rakenne, esim. ethanolille CH 3CH 2OH.
- Viivakaava (skeletal formula) on yleinen orgaanisessa kemiassa; hiiliatomit ja vetyt usein jätetään pois, jolloin näkyvät vain sidokset ja funktionaaliset ryhmät.
- Kaava-yksikkö (formula unit) käytetään ionisille yhdisteille kuten NaCl, jossa esitetään pienin kokonainen suhde ioneja.
Merkintäsäännöt ja erityistapaukset
- Alkuaineen symbolissa ensimmäinen kirjain on iso ja mahdollinen toinen kirjain on pieni (esim. C = hiili, Co = koboltti, CO = hiilimonoksidi). Tämä erottaa eri alkuaineet toisistaan.
- Alaindeksi (n) kertoo kunkin alkuaineen atomien lukumäärän samassa molekyylissä. Yhden atomin tapauksessa alaindeksiä ei yleensä kirjoiteta (esim. O tarkoittaa O 1).
- Polyatomisten ryhmien lukumäärä ilmaistaan sulkujen ja alaindeksin avulla, esimerkiksi kalsiumhydroksidi on Ca(OH) 2 (kaksi OH-ryhmää per Ca).
- Ionien varaus merkitään yläindeksinä: esimerkiksi ammonium on NH 4+ ja sulfaatti on SO 42-.
- Hydraatit merkitään pisteellä: CuSO 4·5H 2O tarkoittaa kuparisulfaattipentahydraattia.
- Isotoopit voidaan ilmaista massaluvun yläindeksinä vasemmalla: 14C on hiilen isotooppi. (Tämä ei muuta kemiallisen alkuaineen symbolia.)
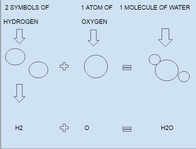
- Kemiallisissa reaktioissa kirjoitetaan kertoimet edessä näyttämään molekyylien tai kaava-yksiköiden määrän: esim. 2 H 2 + O 2 → 2 H 2O.
Yleisiä esimerkkejä ja selityksiä
- H 2O — vesi. Kaksi vety- ja yksi happiatomi molekyyliä kohden.
- H 2O 2 — vetyperoksidi, eri aine kuin vesi; sama koostumus (H ja O), mutta toinen sidosten järjestys ja ominaisuudet.
- CH 4 — metaani, yksinkertaisin hiilivety.
- C 6H 6 — bentseeni; empiirinen kaava on CH.
- NaCl — natriumkloridi (ioniyhdiste). Tässä esitetään kaava-yksikkö eikä molekyyliä.
- Ca(OH) 2 — kalsiumhydroksidi, sulkuja käytetään toistuvien ryhmien lukumäärän osoittamiseen.
- CuSO 4·5H 2O — kuparisulfaatti, joka sisältää viisi vesimolekyyliä per kaava-yksikkö (hydraatti).
Rajoitukset ja lisätieto
Kemiallinen kaava antaa usein tarkan atomikoostumuksen, mutta se ei välttämättä paljasta molekyylin kolmiulotteista rakennetta, sidosten tyyppiä tai stereokemiaa. Tällaiset tiedot vaativat rakennekaavoja, kolmiulotteisia malleja tai erikoismerkintöjä (esim. cis-/trans-, R/S-). Lisäksi resonanceja ja delokalisoituneita elektroneja kuvataan usein useilla rakennekaavoilla tai erityismerkein.
Yhteenveto
Kemiallinen kaava on tiivis tapa kuvata aineen atomikoostumusta. Perussäännöt — alkuaineen symbolit, alaindeksit, kertoimet, sulut ja varaukset — antavat selkeän ja yksiselitteisen merkinnän, jota kemistit ympäri maailmaa käyttävät. Kun tarvitaan lisätietoa sidoksista tai rakenteesta, käytetään rakennekaavoja tai täydentäviä esitysmuotoja.