Eliminaatioreaktio (orgaaninen kemia): määritelmä, E1/E2 ja esimerkit
Eliminaatioreaktio (org. kemia) — selkeä määritelmä, E1- ja E2‑mekanismit, käytännön esimerkit ja vinkit opiskelijoille ja kemisteille.
Orgaanisessa kemiassa eliminaatioreaktio tarkoittaa sitä, että jotkin atomit tai atomiryhmät poistetaan suuremmasta molekyylistä. Yleensä tässä reaktiossa syntyy kaksois- tai kolmoissidos (alkeenit tai alkyynit), mutta eliminaatio voi myös johtaa konjugoituihin tai aromaattisiin järjestelmiin, jos rakenne sen sallii. Eliminaatiot ovat keskeisiä reaktioita orgaanisessa synteesissä, koska ne tarjoavat tavan muodostaa tyydyttymättömiä yhdisteitä ja säätää kaksoissidoksen asento- ja stereokemiaa.
E1-mekanismi (kaksivaiheinen)
Ensimmäistä tapaa kutsutaan E1:ksi. Se tapahtuu kahdessa vaiheessa: ensin muodostuu hitaassa, määräävässä vaiheessa karbokationi, kun poistuva ryhmä lähtenee itsestään. Tämän jälkeen emäs tai muu perusta ottaa protonin karbokationin vieressä olevasta hiilestä, jolloin muodostuu kaksoissidos.
- Rate-laki: reaktion nopeus riippuu vain substraatin konsentraatiosta (1. kertaluvun reaktio).
- Tyypilliset ehdot: heikot emäkset, polar protic -liuottimet ja tertiääriset substraatit suosivat E1-reaktiota.
- Puolustukset: karbokationivälivaihe voi johtaa hydride- tai alkyyli-siirtymiin (rearrangements), jolloin lopputuote voi olla odottamaton.
E2-mekanismi (konsertinen)
Toista tapaa kutsutaan E2:ksi. Tämä tapahtuu yhdessä vaiheessa: emäs poistaa protonin, samalla kun poistuva ryhmä lähtee ja muodostuu kaksoissidos. Ei synny erillistä karbokationiväliainetta.
- Rate-laki: reaktion nopeus riippuu sekä substraatin että emäksen konsentraatioista (2. kertaluvun reaktio).
- Tyypilliset ehdot: vahvat, usein sterisesti esteiset emäkset (esim. t-BuOK) ja sekundääriset tai primaariset substraatit suosivat E2:ta.
- Stereokemia: E2-reaktiossa vaaditaan usein anti-periplanaarinen asento lähtöryhmän ja poistettavan protonin välillä, mikä vaikuttaa lopputuotteen stereokemiaan (trans-alkeenit ovat usein suosittuja).
E1cb ja muut erikoistapaukset
On myös E1cb-mekanismi, jossa reaktio etenee carbanionivälivaiheen kautta: ensin deprotonoituminen muodostaa stabiilin karbanionin (esim. stabiloituneen emäksellä tai elektronivetoisella ryhmällä), ja tämän jälkeen heikompi poistuva ryhmä lähtee. E1cb esiintyy usein, kun poistuva ryhmä on huono (kuten −OH) mutta lähistöllä on hyvin happoisa protoni (esim. β-hydrogeni lähellä karbonylia).
Säännöt, regio- ja stereoselektiivisyys
- Zaitsevin sääntö (Zaitsevin tai Saytzeff): usein muodostuu vakain (useimmiten eniten substituoitu) alkeeni. Poikkeus syntyy, jos emäs on sterisesti suuri — tällöin Hofmann-tuote (vähemmän substituoitu alkeeni) voi olla päätuote.
- Stereokemia: E2 vaatii usein anti-periplanaarisen orientaation lähtöryhmän ja poistettavan protonin välillä. Tämä rajoitus määrää usein cis/trans- tai E/Z-suhteet lopputuotteessa.
- Konjugaatio ja hyperkonjugaatio: alkeenin stabiliteetti kasvaa substituenttien ja konjugaatioiden myötä, mikä vaikuttaa tuotejakaumaan.
Tekijät jotka vaikuttavat reaktiotyyppiin
- Substraatin luokka (primäärinen, sekundaari, tertiäärinen): tertiääriset suosivat E1; primääriset johtavat useimmiten E2 tai SN2.
- Emäksen vahvuus ja steriikka: vahvat emäkset edistävät E2:ta; heikot emäkset voivat sallia E1:n etenemisen.
- Poistuvan ryhmän laatu: hyvä poistuva ryhmä (esim. halidi, tosyl-ryhmä) helpottaa eliminaatiota.
- Lämpötila: korkea lämpötila suosii yleensä eliminaatiota suhteessa substituutioon.
- Liuotin: polar protic -liuottimet suosivat karbokationeja (E1), aprotiset liuottimet voivat suosia konsertista E2:ta tai SN2:ta.
Käytännön esimerkkejä
- Alkyylhalidien dehydrohalogenaatio: esimerkiksi 2-bromibutaani + vahva emäs → 2-buteeni (E2-tyyppinen dehydrohalogenaatio).
- Alkoholien dehydraatio happokatalyysillä: alkoholien kanssa, kun lähellä on vahva happo (esim. H2SO4), vesimolekyyli voi poistua kaksoissidoksen muodostamiseksi (tyypillisesti E1-tertiäärisissä ja lämpöä käytettäessä).
- Dehydrohalogenaatio kahden peräkkäisen halogeenin poistolla voi johtaa alkyynin muodostumiseen.
- Muut keinot: POCl3/pyridiini tarjoaa vaakalaudallisen dehydrataation (eliminaatio ilman karbokationia), mikä on hyödyllistä, kun halutaan välttää rearrange-reaktioita.
Eliminaatio vs. substituutio
Eliminaatio kilpailee usein substituutioreaktioiden (SN1/SN2) kanssa. Usein säätelevät tekijät ovat samat: substraatin rakenne, nukleofiilin/emäksen luonne (vahva perus vs. hyvä nukleofiili), liuotin ja lämpötila. Korkea lämpötila ja vahvat emäkset suosivat eliminaatiota; heikommat nukleofiilit ja viileät olosuhteet taas substituutiota.
Yhteenvetona: eliminaatioreaktiot (E1, E2, E1cb) ovat keskeisiä tapoja muodostaa kaksois- ja kolmoissidoksia orgaanisissa molekyyleissä. Mekanismi, olosuhteet ja reagenssit määräävät, millainen eliminaatio tapahtuu, mitä tuotteita muodostuu (Zaitsevin vs. Hofmann) ja syntyykö välivaiheena karbokationi tai karbanioni sekä onko riskiä rearrange-reaktioille.
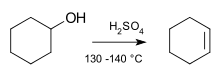
Sykloheksanolimolekyylin eliminaatioreaktio.
Kysymyksiä ja vastauksia
Kysymys: Mikä on eliminaatioreaktio orgaanisessa kemiassa?
V: Eliminoitumisreaktio on, kun jotkut atomit tai atomiryhmä otetaan pois suuremmasta molekyylistä, jolloin yleensä syntyy kaksois- tai kolmoissidos.
K: Mitkä ovat kaksi tärkeintä tapaa tehdä eliminaatioreaktio?
V: Kaksi tärkeintä tapaa tehdä eliminaatioreaktio ovat E1 ja E2.
K: Mitä eroa on E1:n ja E2:n välillä?
V: E1 tapahtuu kahdessa vaiheessa, kun taas E2 tapahtuu vain yhdessä vaiheessa. E1:ssä poistuva ryhmä poistuu itsestään ja sitten emäs tai muu aine poistaa toisen ryhmän. E2:ssa emäs ottaa pois yhden ryhmän ja samalla poistuva ryhmä poistuu.
K: Milloin tapahtuu yleinen eliminaatioreaktio?
V: Yleinen eliminaatioreaktio tapahtuu alkoholien kanssa, kun vahva happo on läsnä, ja vesimolekyyli voi poistua kaksoissidoksen muodostamiseksi.
K: Mikä on poistuva ryhmä eliminaatioreaktiossa?
V: Poistuva ryhmä on molekyyli tai atomi, joka voi poistua itsestään eliminaatioreaktiossa.
K: Mikä on emäs eliminaatioreaktiossa?
V: Emäs on aine, joka voi poistaa ryhmän eliminaatioreaktiossa.
K: Voiko eliminaatioreaktiossa syntyä kolmoissidos?
V: Kyllä, eliminaatioreaktio voi johtaa kolmoissidokseen.
Etsiä