Tässä artikkelissa käsitellään ainoastaan alkoholien kemiaa.
Juomissa käytetty alkoholi on etanolia; lisätietoja on osoitteessa Alkoholijuomat ja alkoholismi.
Kemiassa alkoholi on yleinen termi, jolla tarkoitetaan monia orgaanisia yhdisteitä, joita käytetään teollisuudessa ja tieteessä reagensseina, liuottimina ja polttoaineina. Alkoholit ovat hiilihydraatteja, jotka koostuvat alkyyliryhmästä, jonka hiiliatomiin on sitoutunut yksi tai useampi hydroksyyliryhmä (-OH). Alkoholi on väritöntä ja myös läpinäkyvää.
Huomautus: yllä oleva lause sisältää virheellisen yleistyksen. Alkoholit eivät ole sama asia kuin hiilihydraatit. Oikea määritelmä on, että alkoholit ovat orgaanisia yhdisteitä, joissa yksi tai useampi hydroksyyliryhmä (-OH) on liittyneenä hiiliatomiin. Hiilihydraatit ovat eräs erikoisryhmä orgaanisia molekyylejä (sokerit ja niiden johdannaiset), joilla on useimmiten useita hydroksyyliryhmiä ja karbonyliryhmä; termiä hiilihydraatteja ei tule sekoittaa yleiskäsitteen "alkoholit" kanssa.
Määritelmä ja rakenne
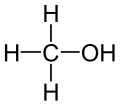
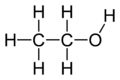
Alkoholit ovat orgaanisia yhdisteitä, joissa atomiryhmä −OH (hydroksyyliryhmä) sitoutuu sp3-hybridisoituneeseen hiiliatomiin. Yksinkertaisin alkoholiyhdiste on metanoli (CH3OH), etanoli (C2H5OH) on yleinen juomissa ja teollisuudessa. Hydroksyyliryhmän läheisyys muihin funktionaalisiin ryhmiin vaikuttaa yhdisteen ominaisuuksiin.
Luokittelu
- Primaariset alkoholi (1°): hydroksyyliryhmä sitoutuu hiileen, jolla on vain yksi hiili-hiili-sidos (esim. etanoli).
- Sekundaariset alkohol (2°): hydroksyyliryhmä sitoutuu hiileen, joka on yhteydessä kahteen hiileen (esim. isopropanoli).
- Teritaariset alkohol (3°): hydroksyyliryhmä sitoutuu hiileen, joka on yhteydessä kolmeen hiileen (esim. tert-butanoli).
- Moniarvoiset alkohol: yhdisteissä on useampi kuin yksi −OH-ryhmä, kuten glyseroli (3 −OH) tai etyleeniglykoli (2 −OH).
Fysikaaliset ominaisuudet
- Hydrogen-sidokset: Hydroksyyliryhmät muodostavat vetysidoksia, mikä nostaa alkoholeiden kiehumispisteitä ja parantaa vesiliukoisuutta pienissä molekyyleissä.
- Liukoisuus: Pienet alkoholit (metanoli, etanoli) ovat hyvin vesiliukoisia; ketjun piteneminen vähentää liukoisuutta.
- Kiehumispisteet: Kiehumispiste riippuu molekyylipainosta ja vetysidosten määrästä — terääriset ja suuret molekyylit yleensä kiehuvat korkeammassa lämpötilassa.
- Tiheys: Useimmat alkoholit ovat vähemmän tiheitä kuin vesi, mutta ominaisuudet vaihtelevat.
- Haju ja maku: Monta alifaattista alkoholia on hajuttomia tai niillä on lievä makea/terävä haju; aromaattiset alkoholiyhdisteet voivat olla voimakkaammin hajuisia.
Kemialliset reaktiot
Alkoholit osallistuvat moniin tärkeisiin kemiallisiin reaktioihin, esimerkiksi:
- Hapetus: Primaariset alkoholit hapettuvat aldehydeiksi ja edelleen karboksyylihapoiksi; sekundaariset alkoholit hapettuvat ketoneiksi. Teritaarisia alkoholeja ei tavallisesti hapeteta helposti ilman C–C-sidoksen katkeamista.
- Dehydraatio: Alkoholeista voidaan poistaa vettä (H2O) etenemään alkeenien muodostumiseen (H2SO4 tai Al2O3 katalyysillä, korkeassa lämpötilassa).
- Substituutio: Hydroksyyliryhmä voidaan muuttaa hyväksi lähteeksi (esim. halogeenihydrokarbonaatiksi) nukleofiilisessa substituutiossa.
- Esteröityminen: Happo + alkoholi → esteri + vesi (tyypillinen kondensaatioreaktio, usein happokatalyytti).
- Transformaatiot: Alkoholit voivat muodostaa alkoksideja metallien kanssa (esim. Na → alkoksidi), osallistua Williamsonin eetterisynteesiin tai toimia lähtöaineina laajemmissa orgaanisissa synteeseissä.
Käyttötarkoitukset
- Liottimet: Alkoholit (etenkin etanoli, isopropanoli) ovat yleisiä liuottimia laboratoriossa ja teollisuudessa.
- Polttoaineet ja lisäaineet: Etanolia ja metanolia käytetään polttoaineina tai polttoaineiden lisäaineina; biodieselin ja muiden synteettisten polttoaineiden valmistuksessa alkoholeilla on keskeinen rooli.
- Kemianteollisuus: Alkoholit toimivat lähtöaineina erilaisten orgaanisten yhdisteiden (eteerit, esterit, aldehydit, ketonit) synteesissä.
- Kosmetiikka ja lääkkeet: Glyseroli, etanoli ja muut alkoholit ovat yleisiä kosmetiikassa, antiseptisissä tuotteissa ja lääkevalmisteissa.
- Antifriisit ja jäähdytysnesteet: Etyleeniglykoli ja propyleeniglykoli ovat alkoholeiden johdannaisia, joita käytetään jäähdytysnesteinä ja antifriiseinä.
Turvallisuus ja haitat
- Tulipalovaara: Monet alkoholit ovat helposti syttyviä — käsittele avotulen ja kipinöiden läheisyydessä varoen.
- Toksisuus: Alkoholeilla on vaihteleva toksisuus: metanoli on erittäin myrkyllistä (näköhermoon kohdistuva vaurio), etanoli on myrkyllistä suurina annoksina ja pitkäaikaiskäyttönä; muut alkoholit voivat aiheuttaa ärsytystä, keskushermoston lamaa tai muita haittavaikutuksia.
- Ympäristövaikutukset: Suuret määrät alkoholeja voivat vaikuttaa vesieliöihin ja ympäristön mikrobiologiaan.
- Työterveys: Käytä suojavarusteita (käsineet, suojalasit, toimiva ilmanvaihto) ja noudata kemikaaliturvallisuusohjeita käsiteltäessä puhtaita alkoholeja tai niiden seoksia.
Nimikkeistö ja kemian perusteet
IUPAC-nimissä alkoholin pääryhmä ilmaistaan päätteellä "-ol" (esim. etanoli). Hydroksyyliryhmän sijainti hiiliketjussa ilmoitetaan numerolla, mikäli se on tarpeen (esim. 2-propanoli). Funktionaalisuuden vaikutus fysikaalisiin ja kemiallisiin ominaisuuksiin perustuu elektronitiheyksiin, steriikkaan ja mahdollisuuteen muodostaa vetysidoksia.
Yhteenvetona: alkoholit muodostavat laajan ja monipuolisen yhdisteperheen, jolla on tärkeitä sovelluksia laboratoriokemian, teollisuuden, lääketieteen ja arjen tuotteiden aloilla. Niiden kemiallinen käyttäytyminen määräytyy hydroksyyliryhmän ja siihen liittyvän hiilirungon rakenteen perusteella, joten pienten muutosten sijainnissa tai hiiliketjun pituudessa voi olla suuri vaikutus ominaisuuksiin.