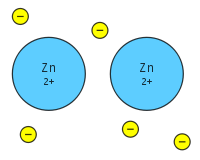
Metallisidos tarkoittaa sitä, että monet irtonaiset elektronien parvet ovat delokalisoituneina ja jakautuneina useiden positiivisten metallikationien välillä. Elektronit toimivat ikään kuin "liimana" tai elektronimerenä, joka pitää positiiviset atomiytimet koossa. Tämä sitomistapa eroaa sekä kovalenttisesta että ionisidoksesta ja selittyy osin metallien suhteellisen alhaisella ionisaatioenergialla, jolloin valenssielektronit irtoavat helposti yksittäisistä ytimistä ja liikkuvat vapaasti koko kiderakenteessa.
Elektronien delokalisaatio kuvataan usein elektronimeri‑mallilla: yksittäisiä elektroneja ei ole kiinnitetty tiettyihin atomeihin, vaan ne muodostavat käytännössä yhtenäisen elektronitiheyden, joka ympäröi positiivisia ioneja. Koska vapaiden elektronien ja ioniytimien välillä on voimakas sähköinen vetovoima, useimmilla metalleilla on korkeat sulamis‑ ja kiehumispisteet; periaate muistuttaa ionisidoksilla esiintyviä kokeellisia ilmiöitä.
Metallien yleiset ominaisuudet
Metallisidokset selittävät monia metallien tunnuspiirteitä:
- Lujuus ja pitkäikäisyys — sidosten kollektiivinen luonne antaa usein hyvän mekaanisen kestävyyden.
- Muovattavuus (taottavuus) ja sitkeys — atomitasolla metallin atomitasot voivat liukua toistensa ohi ilman, että elektronimeri kokonaan pettäisi, mikä mahdollistaa muokkaamisen ilman rikkoutumista.
- Kiilto — vapaat elektronit heijastavat valoa tehokkaasti, minkä vuoksi metallit ovat yleensä kiiltäviä.
- Lämmön ja sähkön johtuminen — delokalisoituneet elektronit siirtävät sekä sähkövarausta että lämpöenergiaa nopeasti.
Johtavuus — sähkö ja lämpö
Sähkönjohtavuus johtuu siitä, että vapaat elektronit voivat liikkua pitkienkin matkojen läpi metallissa ja siten muodostaa sähkövirta. Lämpöjohtuminen on samalla tavalla tehokasta, koska energian siirto tapahtuu osittain elektronien avulla. Siksi metallit ovat yleisesti hyviä sähkön- ja lämmönjohteita. Poikkeuksiakin on: jotkin ei‑metallit, kuten grafiitti, johtavat sähköä, koska niissä on delokalisoituneita elektroneja kerrosten välillä; ioniset yhdisteet puolestaan johtavat sähköä vain sulassa tilassa tai vesiliuoksissa, joissa ionit pääsevät liikkumaan vapaasti.
Miksi metallisidos syntyy ja miten se eroaa muista sidoksista
Perinteisessä atomimallissa metallisidoksen taustalla on se, että metalliatomien ulommilla orbitaaleilla on helppo luovuttaa tai delokalisoida elektroneja. Metallisidoksilla on vähintään yksi valenssielektroni, jota ne eivät jaa vain kahden naapuriatomin kesken kovalenttisella tavalla eivätkä myöskään yksinkertaisesti menetä sitä muodostaakseen täysin erillisiä ioneja. Sen sijaan metalliatomien ulommat energiatasot (atomiorbitaalit) ovat päällekkäin, jolloin syntyy laaja energiatila‑ tai bändijärjestelmä, jossa elektronit voivat liikkua vapaasti koko näiden atomien muodostamassa verkossa. Tässä mielessä metallisidos muistuttaa jonkin verran kovalenttiset sidokset, mutta elektronien delokalisaatio ja kollektiivinen luonne tekevät metallisidoksesta erillisen sidostyypin.
Metallisidoksen vahvuus vaihtelee: se riippuu muun muassa atomien varauksesta, elektronien lukumäärästä ja atomien koosta. Siirtymämetalleilla d‑elektronit voivat osallistua sidokseen ja lisätä sidoksen kompleksisuutta ja lujuutta.
Poikkeukset ja erityistapaukset
Kaikilla metalleilla ei välttämättä vallitse puhdas elektronimeri‑tyyppinen metallisidos. Esimerkiksi eräät elohopean yhdisteet ja joissain tapauksissa elohopea‑ionit käyttäytyvät eri tavoin. Tekstiesimerkkinä alkuperäisessä materiaalissa mainittu kemiallinen merkintä esiintyy muodossa Hg2+
2) — tällaiset monimutkaisemmat metallimetalli‑ ja koordinaatiosidokset voivat olla lähellä kovalenttista luonnetta ja niissä elektronit eivät aina ole täysin delokalisoituneita.
Seokset (alloyt)
Seos on metallien liuos eli kahden tai useamman metallin (tai metallin ja muun alkuaineen) yhteenliittymä. Seokset voivat olla esimerkiksi korvautuvia (substitutional), missä yksi metalliatomi korvaa toisen kriistallisessa rakenteessa, tai interstitiaalisia, joissa pienemmät atomit (kuten hiili rauta‑seoksissa) asettuvat metalliverkoston koloihin. Seokset muokkaavat metallien ominaisuuksia: lujuutta, kovuutta, korroosionkestävyyttä ja johtavuutta voidaan säätää huomattavasti oikeilla lisäaineilla. Useimmat seokset ovat edelleen kiiltäviä ja osoittavat metallien tyypillisiä käytöshyötyjä.
Yhteenvetona: metallisidos perustuu delokalisoituneisiin elektroneihin, jotka sitovat positiivisia ioneja elektronimeren avulla. Tämä selittää monia metallien mekaanisia, optisia ja sähkön‑ sekä lämmönjohtavuuteen liittyviä ominaisuuksia, mutta sidoksen tarkka luonne voi vaihdella alkuaineesta ja kemiallisesta ympäristöstä riippuen.