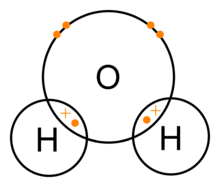
Kovalenttiset sidokset ovat kahden ei-metalliatomin välisiä kemiallisia sidoksia, joissa atomit sitoutuvat jakamalla valenssielektronejaan. Esimerkki on vesi, jossa vety (H) ja happi (O) sitoutuvat toisiinsa muodostaen (H2O). Täydellä ulkokuorella on yleensä kahdeksan elektronia, vedyn tai heliumin tapauksessa kaksi. Valenssielektronit ovat atomin ulkokuoren suhteellisen löysästi pidettyjä elektroneja. Elektronikuorien rakenne määräytyy kvanttimekaniikan mukaan.
Atomin elektronien lukumäärä määräytyy atomin protonien lukumäärän mukaan. Elektronit kiertävät atomiytimiä ikään kuin epäselvissä orbitaaleissa tai "alueissa" atomiytimen ympärillä. Ensimmäisessä kuoressa voi olla enintään kaksi elektronia; seuraavissa kuorissa yleinen käytännön sääntö on enintään kahdeksan elektronia (oktettilaki), mutta poikkeuksia, kuten laajennetut ulkokuoret, esiintyy.
Kovalenttiset sidokset syntyvät, kun atomit lähestyessään jakavat valenssielektroneja siten, että yhteinen elektroni- tai elektronipari on sidottu molempien atomiydinten läheisyyteen. Kun kaksi atomia muodostaa yhteisen orbitaalin, sen energiataso voi olla alhaisempi kuin alkuperäisillä yksittäisillä orbitaaleilla, jolloin sitoutuminen on energisesti edullista. Elektronin siirtyessä uuteen, sidoselektronia kuvaavaan orbitaaliin voi vapautua energiaa fotonin muodossa. Sidoksen muodostuessa molempien atomien välille syntyy usein pieniä osittaisvarauksia (dipoli), ja atomit pysyvät yhdessä sähkömagneettisen vetovoiman avulla. Sidoksen katkaiseminen vaatii yleensä samaa energiamäärää, joka vapautui sen muodostuessa (sidoksen dissosiaatioenergia).
Sidostyypit ja ominaisuudet
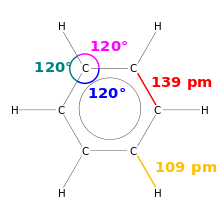
- Yksinkertainen, kaksinkertainen ja kolmoissidos: sidoksen järjestys riippuu jaettujen elektroniparien määrästä. Yksi pari = yksinkertainen (esim. C–C), kaksi paria = kaksinkertainen (C=C), kolme paria = kolmoissidos (C≡C). Usein kaksois- ja kolmiosidoksissa osa sidoksesta on pi (π)-sidosta, osa sigmasidos (σ).
- Sigma (σ) ja pi (π) -sidokset: σ-sidos syntyy suorasta orbitaalien päällekkäisyydestä akselin suunnassa, π-sidos syntyy sivuttaisesta päällekkäisyydestä. σ-sidos on yleensä vahvempi ja sallii vapaamman rotaation sidoksen ympäri kuin π-sidoset.
- Polaarinen vs. ei-polaarinen kovalenttinen sidos: jos atomien elektronegatiivisuudessa on merkittävä ero, sidosta kutsutaan polaariseksi — elektronipari vetäytyy enemmän elektronegatiivisemman atomin lähelle, jolloin syntyy osittaisvarauksia. Pieni tai olematon erotus johtaa ei-polaariseen sidospariin.
- Koordinaatti- eli datiivinen sidos: joskus molemmat sidoksessa olevat elektronit tulevat samalta atomilta; sidosta käsitellään silti kovalenttisena, mutta merkitään usein nuolella (→) selkeyttämään elektroniparin luovuttajaa.
- Resonanssi: joissain molekyyleissä sidosten elektronit voidaan esittää useilla Lewis-rakenteilla; todellinen rakenne on resonanssihybridi, mikä vaikuttaa sidosten pituuksiin ja energioihin.
Sidoksen energiat ja pituudet
Kovalenttisen sidoksen voimakkuus mitataan sidoksen dissipaatioenergiana (kJ/mol) ja pituutena (ångströmeina, Å). Yleensä korkeampi sidostilaus (kaksinkertainen/kolmoissidos) merkitsee lyhyempää ja vahvempaa sidosta. Esimerkiksi tavallinen O–H-sidos vesimolekyylissä on lyhyt (~0,96 Å) ja suhteellisen vahva, kun taas C–C (yksinkertainen) on pidempi ja heikompi.
Teoreettiset mallit
Kovalenttisia sidoksia voi kuvata eri teorioilla. Valenssihybridi- tai valenssiksiteoria korostaa atomiorbitaalien päällekkäisyyttä ja elektronipareja (Lewis-rakenteet). Molekyyliorbitaaliteoria (MO) puolestaan rakentaa molekyylin orbitaalit koko systeemin kvanttimekaanisista orbitaaleista ja selittää esimerkiksi delokalisoituneita elektroneja ja spektroskopisia ominaisuuksia. Molemmat lähestymistavat täydentävät toisiaan käytännön kemian ymmärryksessä.
Vesimolekyyli esimerkkinä
Vesimolekyyli koostuu yhdestä happiatomista ja kahdesta vetyatomista, joita yhdistää kovalenttinen sidos. Happi jakaa yhden elektronin kunkin vetyatomin kanssa muodostaen kaksi σ-sidosta. Koska happi on merkittävästi elektronegatiivisempi kuin vety, elektronipari vetäytyy enemmän hapen puoleen. Tästä syystä happiatomilla on pieni negatiivinen nettovaraus ja vetyatomeilla pieni positiivinen nettovaraus — vesimolekyyli on siis polaarinen molekyyli (sen varaus ei ole tasaisesti jakautunut).
Vesimolekyylin geometriaksi muodostuu kulmainen (bent) rakenne, jossa H–O–H -kulma on noin 104,5°. Jokainen O–H-sidos on noin 0,96 Å pitkä. Vesimolekyylin dipolimomentti on merkittävä (noin 1,85 Debyea), mikä selittää monia veden makroskooppisia ominaisuuksia.
Polaarisuuden seurauksena vesimolekyylit muodostavat vahvoja vetysidoksia toistensa kanssa: positiivinen vety vetää puoleensa toisen molekyylin negatiivista happiatomia. Vetysidokset eivät ole kovin vahvoja yksittäin verrattuna kovalenttisiin sidoksiin, mutta ne ovat riittävän voimakkaita ja lukuisia antaakseen vedelle korkean kiehumispisteen, suuren pinta-energian, hyvän liuottavuuden monille ionisille ja polaarisille aineille sekä ainutlaatuisia biologisesti tärkeitä ominaisuuksia.
Käytännön merkitys
Kovalenttiset sidokset ovat keskeisiä orgaanisessa kemiassa, biologiassa ja materiaaleissa, koska ne muodostavat molekyylien runkot ja määräävät molekyylien muodon, reaktiivisuuden ja fysikaaliset ominaisuudet. Sidosten polariteetti ja mahdolliset vetysidokset vaikuttavat esimerkiksi liukoisuuteen, reaktiivisuuteen ja molekyylien itsejärjestäytymiseen soluissa ja materiaaleissa.
Yhteenvetona: kovalenttinen sidos syntyy, kun atomit jakavat elektroneja struktuurin ja energian optimoinniksi. Sidoksen tarkka luonne (ei-polaarinen, polaarinen, koordinointi, σ/π, sidostilaus) riippuu atomien elektronirakenteesta ja elektronegatiivisuuseroista, ja sillä on suoria vaikutuksia molekyylin ominaisuuksiin, kuten veden tapauksessa.