Atomiorbitaalit ovat atomin ydintä ympäröiviä paikkoja, joissa elektronit ovat todennäköisimmin milloin tahansa. Se on matemaattinen funktio, joka kuvaa joko yhden elektronin tai elektroniparin aaltomaista käyttäytymistä atomissa.
Sanaa "kiertorata" käytetään, koska ajateltiin, että elektronit käyttäytyvät samalla tavalla kuin aurinkokunnassa, jossa ydin on kuin aurinko ja elektronit kiertävät kuin planeetat. Nykykäsityksen mukaan elektronit eivät kuitenkaan liiku selkeästi piirrettyjä ratoja pitkin, vaan niiden sijainti ja liiketila kuvataan todennäköisyysjakaumina — orbitalleina.
Alkuaineen atomiorbitaalien lukumäärä määräytyy alkuaineen jakson mukaan. Elektronit liikkuvat orbitaalien välillä sen mukaan, kuinka nopeasti ne liikkuvat ja kuinka monta muuta elektronia on olemassa. Orbitaalien energia- ja täyttöjärjestys riippuvat myös ydinsähkövarauksesta ja elektronien välisestä vuorovaikutuksesta.
Atomiteoriassa ja kvanttimekaniikassa atomiorbitaali on kvanttiluku. Kullakin tällaisella orbitaalilla voi olla yksi tai kaksi elektronia. Orbitaalien järjestäytyminen liittyy atomien elektronikonfiguraatioihin. Ne on johdettu varhaisempien spektroskopistien kuvauksista, joiden mukaan tietyt alkalimetallien spektriviivat ovat teräviä, pääasiallisia, hajanaisia ja perustavia.
Kvanttiluvut — miten orbitaalit määritellään
Jokainen atomiorbitaali voidaan yksilöidä neljällä kvanttiluvulla:
- pääkvanttiluku n (n = 1, 2, 3, ...): kertoo orbitaalin energiatason eli elektronikuoren ja suurin piirtein etäisyyden ydinosta.
- kulmakerroin- eli sideriaalinen kvanttiluku l (l = 0, 1, ..., n−1): liittyy orbitaalin muotoon (s, p, d, f ...).
- magnetinen kvanttiluku m_l (m_l = −l, ..., 0, ..., +l): kertoo orbitaalin suunnan avaruudessa (esimerkiksi p-orbitaalille on kolme eri m_l-arvoa).
- spinkvanttiluku m_s (m_s = +1/2 tai −1/2): kuvaa elektronin ominaiskiertymää eli spin‑suuntaa; kukin yksittäinen orbitaali voi sisältää korkeintaan kaksi vastakkaisspinistä elektronia (Pauli-kieltosääntö).
Orbitaalien nimet ja muodot
Kvanttiluvun l arvo vastaa orbitaalien nimityksiä:
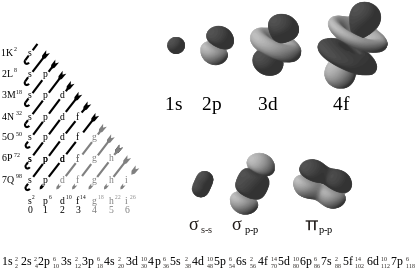
- s (l = 0): pallosymmetrinen orbitaali ilman kulmaniveläisiä solmuja.
- p (l = 1): kaksilobinen muoto, kolme orientaatiota (m_l = −1, 0, +1).
- d (l = 2): monimutkaisempi nelilobinen muoto, viisi orientaatiota.
- f (l = 3): vielä monilobisempi, seitsemän orientaatiota.
Orbitaalien tarkat muodot määräytyvät Schrödingerin yhtälön ratkaisuista ja niitä voi visualisoida todennäköisyyskuorina (esimerkiksi 90 % todennäköisyyskaaret). Orbitaalien nodet eli nollatasot jakautuvat radiaalisiin ja kulma‑ eli angulaarisiin nodoihin. Radiaalisten nodien määrä on n − l − 1 ja kulmanodien määrä on l.
Energia, degeneraatio ja monielektroniset atomit
Yksielektronisessa vetyatomissa kaikki orbitaalit, joilla on sama n, ovat energia‑arvoltaan yhtä; ne ovat degeneroituneita. Monielektronisissa atomeissa elektronien välinen keskinäinen hylkimisvoima ja ekranointi rikkoo tämän degeneraatioiden järjestyksen: tyypillisesti energia riippuu sekä n:stä että l:stä. Energiajärjestyksen likiarvo voidaan usein päätellä n + l -säännöllä (Aufbau‑periaate): pienempi n + l tarkoittaa alhaisempaa energiaa; jos n + l on sama, pienempi n merkitsee alhaisempaa energiaa.
Elektronikonfiguraatio ja täyttösäännöt
- Aufbau‑periaate: elektronit täyttävät alhaisimmasta energiasta alkavat orbitaalit.
- Pauli‑kieltosääntö: yhdessä orbitaalissa voi olla enintään kaksi elektronia, joilla on vastakkaiset spinit.
- Hundin sääntö: saman energian orbitaaliryhmän (esim. 2p) elektronit asettuvat ensin yksittäisinä samansuuntaisilla spineillä ennen kuin parittuvat — tämä minimoi elektronien hylkimisenergian.
Esimerkiksi alkuaineiden peruskonfiguraatiot: He = 1s2, Li = 1s2 2s1, O = 1s2 2s2 2p4. Lyhyt notaatiotapa käyttää jalokaasujen sulkeita ytimen korvikkeena (esim. Fe: [Ar] 4s2 3d6).
Kuinka monta orbitaalia ja elektronia kuorella voi olla
Kuorella n on yhteensä n^2 orbitaalia (eri l- ja m_l‑yhdistelmät), ja koska yhdessä orbitaalissa voi olla enintään kaksi elektronia, kokonaiskapasiteetti yhdelle kuorelle on 2n^2 elektronia.
Käytännön merkitys ja havainnollistaminen
Orbitaalikäsitettä käytetään laajasti kemian ja fysiikan selityksissä: kemialliset sidokset, hybridisaatio molekyyleissä, molekyyliorbitaalit ja spektroskopia perustuvat orbitaalien muotoihin ja energioihin. Orbitaalit eivät kuvaa elektronien "kiertämistä" ympyränmuotoisilla radoilla, vaan ne ovat todennäköisyysjakaumia — näin selitetään muun muassa atomin spektrejä ja kemiallisia ominaisuuksia.
Muita huomioita
- Joissakin siirtymämetalle ja raskaammissa alkuaineissa elektronikonfiguraatiot poikkeavat yksinkertaisimmista ennusteista johtuen d‑ ja f‑orbitaalien erityisistä energioista ja elektronispinien välisistä vaikutuksista.
- Atomiorbitaalit ovat ratkaisujen perusrakenteita myös molekyylien tutkimuksessa, joissa atomiorbitaalit yhdistyvät muodostaen molekyyliorbitaaleja.
- Kuvituksina usein käytetään elektronitiheyskuvia tai isopinta‑pintoja, jotka auttavat ymmärtämään, missä elektronin todennäköisyys on suurin.
Yhteenvetona: atomiorbitaali on kvanttimekaaninen kuvaus elektronin paikasta ja käyttäytymisestä atomissa, joka määritellään kvanttiluvuilla ja ilmenee eri muotoisina ja energioisina todennäköisyysjakaumina. Nämä käsitteet ovat keskeisiä kemian ja atomifysiikan selityksissä.