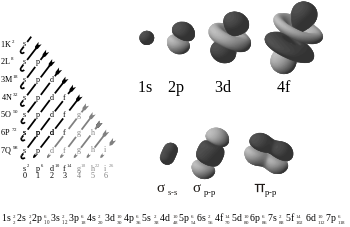
Kemiassa piisidokset (π-sidokset) ovat kovalenttisia kemiallisia sidoksia, joissa yhden elektronin kiertorata risteää (limittyy) toisen elektronin kiertoradan kanssa. Elektronit kulkevat kahdeksikon muotoista rataa (ks. kuva). Päällekkäisalueita on kaksi, koska radat ovat päällekkäisiä molemmilla lohkoilla. Vain yksi radan solmupisteistä kulkee molempien osallistuvien ytimien läpi.
Määritelmä ja perusrakenne
Yksinkertaisesti sanottuna π-sidos syntyy, kun kahden atomin p-tyyppiset atomiorbitaalit limittyvät sivusuunnassa (side-on), eli niiden elektronitiheys yltää päällekkäin kahdella erillisellä alueella nukleusten ylä- ja alapuolella. Tällainen päällekkäisyys eroaa sigmasidoksesta, jossa orbitaalit limittyvät päällekkäin akselin suuntaisesti (end-to-end).
Orbitaalinen selitys ja symmetria
Pi-sidoksen nimessä oleva kreikkalainen π-kirjain viittaa p-orbitaaleihin. Pi-sidoksen orbitaalisymmetria näyttää sidoksen akselin suuntaisesti katsottuna samalta kuin p-orbitaali: pi-orbitaaleilla on tyypillisesti yksi solmataso, joka sisältää sidoksen akselin. Tästä seuraa, että π-orbitaalien välillä on vaakasuunnassa tai sivusuunnassa rajoitetumpi päällekkäisyys kuin σ-orbitaaleilla, minkä vuoksi π-sidokset ovat usein heikommat kuin vastaavat σ-sidokset.
Moninkertaiset sidokset (kaksois- ja kolmoissidokset)
Usein pi-sidokset esiintyvät yhdessä σ-sidoksen kanssa muodostaen moninkertaisen sidoksen:
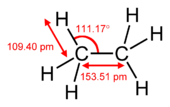
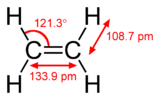
- kaksoissidos = yksi σ-sidos + yksi π-sidos (esim. eteenissä, C=C),
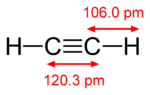
- kolmoissidos = yksi σ-sidos + kaksi π-sidosta (esim. etyynissä, C≡C),
- erityistapauksena allenit (kumulene-sarja), joissa kaksi π-järjestelmää voivat olla toisiaan vastaan orientoituneita (risti-π), jolloin pi-orbitaalit ovat kohtisuorassa toisiinsa nähden.
Kolmoissidoksessa kaksi π-sidosta syntyy kahdesta erillisestä p-orbitaaliparista, jotka ovat keskenään ortogonaalisia.
Energia, MO-kuvaus ja antibonding-orbitaalit
Kvanttimekaniikka selittää π- ja σ-sidosten energiat muodostuvien molekyyliorbitaalien avulla: kahden atomiorbitaalien lineaarisesta yhdistämisestä syntyy sidoksia muodostava (π) ja vastaavasti antibonding (π*) orbitaleja. Pi→pi* -siirtymät ovat tärkeä tekijä orgaanisessa fotokemiassa ja näkyvät UV–Vis-spektrissä.
Konjugaatio, delokalisaatio ja aromaattisuus
Kun π-orbitaaleja on lähekkäin useammassa atomissa, niiden elektronit voivat delokalisoitua eli jakautua useamman atomin yli. Tämä konjugaatio alentaa järjestelmän energiatilaa ja vaikuttaa kemiallisiin ominaisuuksiin:
- konjugoidut dioleenit ja polyeenit näyttävät poikkeuksellista stabiilisuutta ja muuttuneita absorptio-ominaisuuksia,
- aromaattiset järjestelmät (esim. bentseeni) ovat erityistapaus, jossa delokalisoituneet π-elektronit antavat huomattavaa stabilisaatiota noudattaen Hückelin 4n+2 -sääntöä.
Kemialliset ominaisuudet ja reaktiivisuus
Pi-elektronit sijaitsevat usein atomien ulkopuolella ja ovat helposti saavutettavissa, joten π-sidokset toimivat tyypillisesti reaktiokohtina:
- Elektrofiilinen additio on yleinen reaktio tyydyttämättömille sidoksille (esim. halogeenien tai H–H lisäys C=C -sidokseen), koska elektrofiili voi tarttua π-elektronipilveen, jolloin π-sidos avautuu ja muodostuu uusi σ-sidos.
- Hydrogenaatio, halogenointi ja hydroborointi ovat esimerkkejä prosesseista, joissa π-sidos muuttuu σ-sidokseksi.
- Konjugaatio vaikuttaa reaktiivisuuteen: delokalisoituneet π-järjestelmät voivat stabilisoida välituotteita ja ohjata reaktiopaikkoja.
Liikkumattomuus ja rotaatiovaraus
Pi-sidoksella yhdistetyt molekyyliosat eivät voi vapaasti kiertyä kyseisen sidoksen ympäri ilman, että π-sidos rikkoutuu. Pyöriminen tuhoaa kahden p-orbitaalin yhdensuuntaiset radat ja vaatii yleensä huomattavaa energiaa, joten kaksoissidokset estävät rotaation ja luovat stereokemiallisia mahdollisuuksia (cis/trans- eli E/Z-isomeria).
Spektrit ja tunnistusmenetelmät
Pi-sidosten läsnäolo näkyy useissa spektroskooppisissa menetelmissä:
- IR-spektroskopiassa C=C-venymäresonanssi esiintyy tyypillisesti noin 1600–1680 cm−1 ja C≡C noin 2100–2260 cm−1 (riippuen substituenteista ja konjugaatioasteesta),
- UV–Vis-spektroskopiassa konjugoidut π-järjestelmät absorboivat näkyvää tai UV-valoa π→π*-siirtymien vuoksi; konjugaatio siirtää absorptiota pidemmälle aallonpituudelle (red-shift),
- NMR-menetelmät ja kemialliset siirtymät ilmoittavat usein pi-elektronijärjestelmän vaikutuksesta protonien ja hiilien ympäristössä (esim. aromaatinen deshielding).
Erikoistapaukset: heteroatomit, d-orbitaalit ja metalli−ligandi‑π‑vuorovaikutukset
Vaikka π-sidokset liitetään yleisimmin p-orbitaaleihin, myös muut orbitaalit voivat osallistua π-tyyppiseen limittymiseen:
- heteroatomit (O, N, S) voivat antaa tai vastaanottaa osan π-elektronitiheydestä (esim. konjugoituneet imiinije ja enoli-tyyppiset rakenteet),
- siirto- ja takaperin-π-vuorovaikutukset (π-donor ja π-acceptor, kuten karbonyylien ja metallien välillä) ovat tärkeitä koordinaatiokemiassa ja katalyysissä,
- d-orbitaalien oletetaan tietyissä yhteyksissä voivan muodostaa π-tyyppisiä rajoituksia, mikä liittyy hypervalenssiin ja raskaisiin alkuaineisiin — käytännössä d-orbitaalien rooli sidoksissa on tapauskohtainen ja usein heikompi kuin yksinkertaistettu hypoteesi antaa ymmärtää.
Yhteenveto
π-sidokset ovat sivuttaispäällekkäisyyden kautta syntyviä kemiallisia sidoksia, joissa elektronit liikkuvat taas erityisissä π-orbitaaleissa. Ne ovat yleensä heikompia kuin σ-sidokset, mutta niillä on suuri merkitys molekyylien elektronirakenteessa, konjugaatiossa, reaktiivisuudessa ja spektrisissä ominaisuuksissa. Pi-elektronien delokalisaatio mahdollistaa muun muassa aromaattisuuden ja konjugaatio-energian hyödyntämisen erilaisissa kemiallisissa prosesseissa.