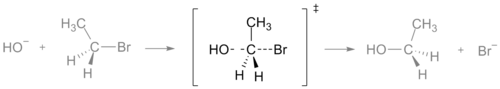Kemiallisessa reaktiossa siirtymätila on potentiaalienergiakuvan (reaktiokoordinaatin) korkeimmassa pisteessä oleva konfiguraatio — eli se piste, jossa systeemin energia on suurimmillaan reaktiossa reagenteistä kohti tuotteita. Tätä energiavaipan korkeinta kohtaa kutsutaan aktivoitumisenergiaksi. Kun kaksi tai useampi molekyyli sekoittuu ja törmää toisiinsa, tarvitaan riittävästi energiaa, jotta järjestelmä ylittää tämän energiakynnyksen; jos törmäyksellä tai lämpöliikkeellä on riittävästi energiaa siirtymätilan läpi, reaktio voi edetä ja muodostua uusia molekyylejä. Siirtymätilassa osa vanhoista sidoksista on katkeamassa samaan aikaan kun uusia sidoksia syntyy; se on tyypillisesti epästabiili, lyhytkestoinen rakenne. Kuvaajissa siirtymätila merkitään usein kaksoistikarilla ‡ (kaksoisdagger). Lisäksi siirtymätila vastaa potentiaalienergiatasapinnan ensimmäisen ordinaatin satulapistettä (saddle point), ei energiaminimiä.
Tutkimuksen haasteet ja erot välitiloihin
Siirtymätilojen tutkiminen on vaikeaa, koska niiden energiataso on korkea ja ajallinen kesto hyvin lyhyt — tyypillisesti femtosekunteja tai vähemmän. Tämän vuoksi siirtymätilaa ei yleensä voi eristää kokeellisesti samalla tavalla kuin stabiileja yhdisteitä. On tärkeää olla sekoittamatta siirtymätiloja välitiloihin: välitilat ovat energian minimipisteitä (stabiileja tai metastabiileja välituotteita), joita voi esiintyä reaktiosarjan keskellä ja joilla voi olla pitkä elinikä verrattuna siirtymätilaan. Siirtymätilan sijasta välitila näkyy potentiaalienergiakäyrässä aina laskuna (minimi) reaktion koordinaatissa.
Tutkimusmenetelmät — laskennalliset ja kokeelliset lähestymistavat
Siirtymätiloja tutkitaan sekä teoreettisin laskelmin että kokeellisin menetelmin. Laskennallisessa kemiassa etsitään yleensä konformaatiota, jolla on yksi imaginaarinen värähtelytaajuus (yksi negatiivinen toisen derivaatan arvo energian suhteen) — tämä on merkitsevä tunnusmerkki ensimmäisen ordinaatin siirtymätilalle. Tällaiset laskelmat tehdään esimerkiksi kvanttimekaniikan menetelmillä (DFT, ab initio). Usein lasketaan myös intrinsinen reaktiokoordinaattipolku (IRC, intrinsic reaction coordinate) varmistaakseen, että löydetty siirtymätila yhdistää halutut lähtöaineet ja tuotteet.
- Laskennalliset työkalut: elektronitiheyteen perustuvat menetelmät (DFT), korkeampitasoiset ab initio -menetelmät, siirtymätilahakualgoritmit ja IRC-laskelmat.
- Kokeelliset lähestymistavat: femtokemian spektroskopia, ajoitetut (time-resolved) spektroskopiat, kineettinen analyysi (esim. Arrheniuksen ja Eyringin yhtälöt), mahdollisten siirtymätilaan viittaavien rakenteiden mallintaminen ja siirtymätilaan analogien käyttö (esim. inhibiittorit entsyymitutkimuksissa).
- Kineettiset tunnisteet: kinetiikka (lämpötilariippuvuus), kinetiikan isotooppivaikutukset (KIE, kinetic isotope effects) ja lineaariset vapaan energian suhteet (esim. Hammett-analysa) antavat tietoa siirtymätilan luonteesta.
Teoria ja merkitys reaktiomekanismeissa
Siirtymätilateoria on keskeinen osa reaktiomekanismien ja kemiallisten kinetiikan ymmärrystä. Transition state -teoria (Eyringin tai Eyring–Polanyi -muoto) antaa yhteyden siirtymätilan vapaan energian ΔG‡ ja reaktionopeuden välillä: k = (k_B T / h) · exp(−ΔG‡ / (RT)), missä k on nopeusvakio, k_B Boltzmannin vakio, h Planckin vakio, T lämpötila ja R yleiskaasun vakio. Tämä erottaa puhtaan aktivoitumisenergian E_a ja termodynaamisen vapaan energian muutoksen siirtymätilassa (ΔG‡), jotka molemmat vaikuttavat reaktion nopeuteen mutta kuvaavat eri asioita.
Hammondin postulaatin mukaan siirtymätila muistuttaa enemmän lähtöaineita silloin kun reaktio on voimakkaasti ajelehtiva (endergoninen tai eksergoninen) — käytännössä siirtymätilan rakenne kallistuu kohti reagensseja tai tuotteita sen mukaan, kumpi puoli on alhaisempi energisesti. Tämä ajatus auttaa ennustamaan, mitkä sidokset ovat enimmäkseen muodostumassa tai katkeamassa siirtymätilassa.
Käytännön esimerkkejä ja katalyysi
Monissa tunnetuissa reaktioissa on tyypillinen siirtymätilan geometria: esimerkiksi nucleofiilinen substitution SN2 -reaktio kulkee lineaarisen siirtymätilan kautta, jossa lähtevän ryhmän ja tulevan nukleofiilin väliset sidokset ovat samanaikaisesti osittain muodostumassa ja katkeamassa (ns. “back-side attack”). Prototransfer-reaktioissa siirtymätila voi olla hyvin lyhyt ja protonin siirtyessä muodostuu lintumaista siirtymätilaa.
Katalyytit (mukaan lukien entsyymit) toimivat usein alentamalla siirtymätilan energiaa, muuttamalla siirtymätilan geometrista muotoa tai stabiloimalla siirtymätilaan liittyvän polarisaation. Tämän seurauksena aktivoitumisenergia pienenee ja reaktionopeus kasvaa merkittävästi.
Yhteenveto
Siirtymätila on reaktioreitin korkeimman energian piste, jonka ylittäminen vaaditaan reaktion etenemiseen. Vaikka siirtymätilaa ei voi yleensä eristää kokeellisesti, sen luonteen voi päätellä ja mallintaa yhdistämällä laskennallisia menetelmiä (esim. kvanttikemialliset laskelmat ja IRC) sekä kokeellisia havaintoja (kineettinen analyysi, isotooppivaikutukset, femtosekuntispektroskopia). Siirtymätilojen ymmärtäminen on keskeistä reaktiomekanismien selvittämisessä ja tehokkaan katalyysin suunnittelussa.