Kemiallinen kinetiikka (reaktiokinetiikka) – reaktionopeudet, mekanismit
Kemiallinen kinetiikka (reaktiokinetiikka): ymmärrä reaktionopeudet, mekanismit, törmäysteoria ja vaikutustekijät – käytännön nopeuslait, nopeusvakiot ja siirtymätilat.
Kemiallinen kinetiikka, jota kutsutaan myös reaktiokinetiikaksi, tutkii, kuinka nopeasti kemialliset reaktiot etenevät. Tähän sisältyy sen tutkiminen, miten eri olosuhteet, kuten lämpötila, paine tai käytetty liuotin, vaikuttavat reaktion nopeuteen. Kemiallisen kinetiikan avulla voidaan myös selvittää reaktiomekanismeja ja siirtymätiloja.
Kemiallisen kinetiikan perusajatusta kutsutaan törmäysteoriaksi. Sen mukaan molekyylien on törmättävä toisiinsa, jotta reaktio voisi tapahtua. Jos reaktion nopeutta voidaan lisätä, osumien määrän on siis kasvettava. Tämä voidaan tehdä monin tavoin.
Kokeiden avulla voidaan laskea reaktionopeuksia, joista saadaan nopeuslait ja nopeusvakiot. Nopeuslaki on matemaattinen lauseke, jonka avulla voidaan laskea reaktion nopeus reagenssien konsentraation perusteella.
Nopeuslaki ja reaktionopeus
Nopeuslaki ilmaisee reaktion hetkellisen nopeuden konsentraatioiden funktiona tyypillisesti muodossa v = k [A]^m [B]^n, missä v on reaktionopeus, k on nopeusvakio ja eksponentit m ja n ovat reaktion kertalukuja (order). Nämä kertaluvut eivät välttämättä vastaa stoikiometriaa, vaan ne määritellään kokeellisesti.
Reaktion kertaluvut ja nopeusvakion yksiköt:
- Ensimmäisen kertaluvun reaktio: v = k [A]. Yksikkö k: s-1.
- Toisen kertaluvun reaktio (esim. bimolekulaarinen A + B tai 2A): v = k [A][B] tai v = k [A]^2. Yksikkö k: M-1 s-1.
- Nollannen kertaluvun reaktio: v = k. Yksikkö k: M s-1.
Lämpötilan vaikutus ja energiakynnys
Yksi tärkeimmistä tekijöistä, joka määrää reaktionopeuden, on aktivaatioenergia (Ea). Usein reaktion nopeus seuraa Arrheniuksen lakia:
k = A exp(−Ea/RT),
missä A on esieksponenttitekijä (frekvenssitekijä), R on kaasuvakio ja T on lämpötila kelvineinä. Tämä yhtälö selittää, miksi pieni lämpötilan nousu voi johtaa huomattavasti suurempaan reaktionopeuteen.
Toinen tapa kuvata lämpötilariippuvuutta on siirtymätilateoria (Eyring), joka yhdistää reaktionopeuden vapausenergiaan ΔG‡:
k = (k_B T / h) exp(−ΔG‡/RT),
missä k_B on Boltzmannin vakio ja h Planckin vakio. Tämä antaa yhteyden termodynamiikan (vapausenergia) ja kinetiikan (nopeus) välille.
Reaktiomekanismit ja alkeisaskelmat
Reaktiomekanismi koostuu yhdestä tai useammasta alkeisaskelmasta, joista jokainen on luonteeltaan yksinkertaisempi (esim. unimolekulaarinen hajoaminen tai bimolekulaarinen törmäys). Mekanismin kautta voidaan ymmärtää, miten alkuainemolekyylit muuntuvat tuotteiksi ja mikä askel määrää reaktionopeuden (nopeutta rajoittava askel).
Yleisiä käsitteitä:
- Alkeisaskelen molekulaarius: uni-, bi- tai harvoin termomekulaareja reaktioita.
- Pseudoensimmäisen kertaluvun olosuhteet: kun yksi reagenssi on paljon suuremmassa määrin, sen konsentraatio voidaan pitää käytännössä vakiona, jolloin monimutkainen reaktio käyttäytyy ensimmäisen kertaluvun mukaan.
- Takaisinsuuntaiset ja esivakautetut tasapainot: joskus reaktion alkuosa muodostaa tasapainon, jonka jälkeen nopeutta rajoittava askel etenee.
- Jatkuvasuunnassa oletus (steady-state): populaatioiden (esim. radikaalien tai välituotteiden) muutokset oletetaan pieniä, jolloin niiden differentiaaliyhtälöitä yksinkertaistetaan.
Katalyysi ja ympäristötekijät
Katalyytti muuttaa reaktion mekanismia alentamalla aktivaatioenergiaa ja siten nopeutta lisäämällä, mutta ei kuluta itseään pois. Katalyysi voi olla:
- Homogeeninen – sama faasi kuin reaktio (esim. liuoskatalyysi).
- Heterogeeninen – eri faasi, esim. kiinteä katalyytti kaasufaasireaktiossa (tärkeä teollisuudessa).
- Enkymologinen – entsyymit toimivat biologisina katalyytteina ja voivat nostaa reaktionopeutta miljoonia kertoja.
Myös liuotin, paine, ionivoimakkuus ja pH vaikuttavat monien reaktioiden nopeuteen ja mekanismiin, erityisesti bio- ja elektrokemiallisissa reaktioissa.
Kokeelliset menetelmät ja reaktionopeuden määritys
Reaktionopeuksia mitataan monin eri tavoilla riippuen reaktiosta: spektroskopia (UV–Vis, IR), pH-mittaukset, konduktiivisuus, kaasuanalyysi (GC), titraus ja stopperimenetelmät. Kinetiikassa tavallinen lähestymistapa on:
- Alkukiertoanalyysi (initial rates) – mitataan alussa, kun tuotteiden takaisinvaikutus on vähäinen; avulla määritetään kokeelliset kertaluvut m ja n.
- Integroitu nopeuslaki – vertaamalla havaittuja konsentraatiovariaatioita aikaan voidaan tunnistaa nollas-, ensimmäinen- tai toisen kertaluvun käyttäytyminen ja laskea k.
- Pseudoensimmäisen kertaluvun menetelmät – käytetään, kun yksi reagenssi on suurina yliohvauksina.
- Isotooppivaikutus – substituutiot (esim. D/H) auttavat paljastamaan, rikkoutuuko tietty sidos nopeutusaskelessa (kinetic isotope effect).
Esimerkkinä ensimmäisen kertaluvun hajoaminen: ln([A]0/[A]t) = kt ja puoliintumisaika t1/2 = ln2/k. Toisen kertaluvun tapauksessa integroitu muoto on 1/[A]t − 1/[A]0 = kt.
Erikoistapaukset ja ilmiöt
Joissain järjestelmissä esiintyy ketjureaktioita (esim. radikaaliketjut poltossa ja orgaanisissa reaktioissa), joissa pieni määrä aloittavia lajeja voi johtaa nopeisiin ketjureaktioihin. Myös autokatalyysi (tuote itse kiihdyttää reaktiota) ja komplekseja dynamiikkaa (esim. oskilloivat reaktiot) esiintyy.
Miksi kemiallinen kinetiikka on tärkeää?
Kinetiikka antaa käytännön ohjeita reaktioiden hallintaan: teollisuudessa optimoidaan saanto ja turvallisuus, lääkekehityksessä ymmärretään metabolia ja reaktioaika, ympäristötutkimuksessa arvioidaan saasteiden hajoamista ja biokemiassa hahmotellaan solussa tapahtuvien reaktioverkostojen nopeuksia.
Yhteenveto: Kemiallinen kinetiikka yhdistää kokeellisen mittauksen ja teoreettisen mallinnuksen selvittääkseen, miten ja miksi reaktiot etenevät tiettyä nopeutta. Se kattaa nopeuslait, mekanismit, lämpötilan ja katalyytin vaikutukset sekä laajan joukon kokeellisia menetelmiä, joiden avulla reaktion yksityiskohdat voidaan paljastaa.
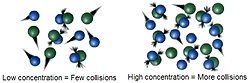
Suuremmassa pitoisuudessa molekyylit osuvat toisiinsa helpommin, joten reaktion nopeus on suurempi.
Reaktion järjestys
tasapaino on luonteeltaan dynaaminen
Tariffilakeja on monenlaisia, mutta yleisimmät niistä ovat:
- nollajärjestysreaktio: nopeus ei riipu pitoisuudesta.
- ensimmäisen kertaluvun reaktio: nopeus riippuu vain yhden reagoivan aineen konsentraatiosta.
- toisen kertaluvun reaktio: nopeus riippuu kahden reagoivan aineen konsentraatiosta tai yhden reagoivan aineen konsentraation neliöstä.
Näiden tietojen perusteella voidaan pohtia reaktion mekanismia. Jos se on esimerkiksi toisen kertaluvun reaktio, on todennäköistä, että reaktion molemmat molekyylit yhdistyvät nopeutta määrittävän vaiheen aikana. Tämä on mekanismin vaikein vaihe, koska siinä on suurin aktivoitumisenergia.
| Nukleofiilinen substituutio | Yksimolekyylinen nukleofiilinen substituutio (SN 1) - Bimolekyylinen nukleofiilinen substituutio (SN 2) - Nukleofiilinen aromaattinen substituutio (SN Ar) - Nukleofiilinen sisäinen substituutio (SN i) |
| Yksimolekyylinen eliminaatio (E1) - E1cB eliminaatioreaktio - Bimolekyylinen eliminaatio (E2). | |
| Elektrofiilinen additio - Nukleofiilinen additio - Vapaaradikaalinen additio - Sykloadditio | |
| Aiheeseen liittyvät aiheet | Alkeisreaktio - Molekyylit - Stereokemia - Katalyysi - Törmäysteoria - Liuotinvaikutukset - Nuolen työntäminen |
| Kemiallinen kinetiikka | |
Kysymyksiä ja vastauksia
K: Mitä on kemiallinen kinetiikka?
V: Kemiallinen kinetiikka, jota kutsutaan myös reaktiokinetiikaksi, on tutkimusta siitä, kuinka nopeasti kemialliset reaktiot etenevät ja kuinka erilaiset olosuhteet, kuten lämpötila, paine tai käytetty liuotin, vaikuttavat reaktion nopeuteen.
K: Mitä todetaan törmäysteoriassa?
V: Törmäysteorian mukaan molekyylien on törmättävä toisiinsa, jotta reaktio voisi tapahtua. Jos reaktion nopeutta voidaan lisätä, osumien määrän on siis kasvettava.
K: Miten reaktionopeudet voidaan laskea?
V: Kokeiden avulla voidaan laskea reaktionopeuksia, joista saadaan nopeuslait ja nopeusvakiot.
K: Mikä on nopeuslaki?
V: Nopeuslaki on matemaattinen lauseke, jonka avulla voidaan laskea reaktion nopeus reagenssien konsentraation perusteella.
K: Miten reaktion nopeutta voidaan lisätä?
V: Reaktion nopeutta voidaan lisätä lisäämällä molekyylien välisten törmäysten määrää. Tämä voidaan tehdä monella tavalla, kuten muuttamalla lämpötilaa, painetta tai käytettyä liuotinta.
K: Mitä ovat siirtymätilat?
V: Siirtymätilat ovat kemiallisten reaktioiden välivaiheita, jotka syntyvät, kun reaktantit muodostavat tuotteita ja energiaa vapautuu tai absorboituu tämän prosessin aikana.
Etsiä