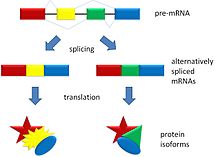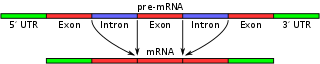
Vaihtoehtoisen liittämisen avulla DNA voi koodata useampaa kuin yhtä proteiinia. Se muuttaa lähetti- RNA:n eksonien koostumusta.
Miten vaihtoehtoinen splikointi toimii
Vaihtoehtoisessa splikoinnissa transkription tuottaman pre-messenger-RNA:n eksonit ja intronit tunnistetaan ja leikataan uudelleen splicing-prosessissa. Tämä prosessi tapahtuu suurena proteiini- ja RNA-kompleksina, nimeltään spliceosomi, joka koostuu useista snRNP-yksiköistä (esim. U1, U2, U4/U6 ja U5) sekä lukuisista apuproteiinista. Valitsemalla eri splispaikkoja sama esiaste-RNA voidaan yhdistää monella eri tavalla, jolloin muodostuu erilaisia kypsiä lähetti-RNA:ita, jotka käännetään eri proteiineiksi.
Tyypilliset vaihtoehtoisen splikoinnin mallit
- Eksonin ohitus (exon skipping) — tietty eksoni jätetään pois.
- Vaihtoehtoinen 5′- tai 3′-splispaikka — eksonin reunasta käytetään eri aloitus- tai lopetuspisteitä, jolloin eksonin sisältö muuttuu.
- Keskinäisesti pois sulkevat eksonit (mutually exclusive exons) — kahdesta eksonista käytetään aina vain yhtä.
- Intronin säilyminen (intron retention) — introni jää osaksi kypsää mRNA:ta.
Säätely ja kudos- sekä kehitysvaihekohtaisuus
Säätely tapahtuu cis-elementtien (splis-paikat, enhancers ja silencers RNA:ssa) ja trans-tekijöiden (RNA-sitovat proteiinit kuten SR-perheen proteiinit ja hnRNP:t) välisenä vuorovaikutuksena. On olemassa splikointiaktivaattoreita, jotka edistävät tietyn splispaikan käyttöä, ja splikointirepressoreita, jotka vähentävät sitä. Vaihtoehtoinen splikointi on usein kudosspesifistä ja myös kehitysvaiheittain ohjautuvaa: sama geeni voi tuottaa eri isoformeja esimerkiksi hermosoluissa, lihaksessa tai maksassa, tai eri kehitysajan kohdissa.
Lisäksi kromatiiniympäristö, geenin transkriptionopeus ja RNA:n sekundäärirakenne vaikuttavat siihen, mitkä splispaikat valikoituvat. Splikointi on usein osittain ko-transkriptionaalinen eli tapahtuu samaan aikaan RNA:n synteesin kanssa.
Funktionaaliset vaikutukset
Vaihtoehtoisella splikoinnilla voidaan vaikuttaa proteiinin rakenteeseen ja siten sen toimintaan, alirakenteisiin, solusijaintiin tai vuorovaikutuksiin muiden proteiinien kanssa. Se voi myös muuttaa UTR-alueita, mikä vaikuttaa lähetti-RNA:n vakauteen, translatoitumiseen ja solun sisäiseen lokalisointiin. Joissain tapauksissa vaihtoehtoinen splikointi voi johtaa mRNA:han, joka sisältää ennenaikaisen stop-kodon — tällöin mRNA tuhoutuu usein nonsense-mediated decay -järjestelmän (NMD) kautta, mikä on eräs transkription jälkeisen laadunvalvonnan muoto.
Esimerkkejä ja merkitys
Vaihtoehtoisen splikoinnin ansiosta ihmisellä on suhteessa pienempään geenimäärään suurempi proteiinimonimuotoisuus: arvioiden mukaan ~95 % monieksonisista geeneistä käy läpi vaihtoehtoista splikointaa. Tämä monimuotoisuus on tärkeä hermoston toiminnassa, immuunivasteessa, solujen signaalinvälityksessä ja monissa muissa prosesseissa.
Sairaudet ja terapianäkymät
Sairaudet voivat johtua tavanomaisesta poikkeavasta splikauksesta. Monet geneettiset häiriöt johtuvat spleikkauksen muutoksista tai splikointireittien häiriöistä. Esimerkkejä:
- Spinaalinen lihasatrofia (SMA): SMN2-geenin splikauksen muokkaus on hoitokeino — antisense-oligonukleotiditerapia nusinersen (Spinraza) muuttaa SMN2:n splikointia ja parantaa funktionaalisesti tärkeän eksonin sisältymistä.
- Duchennen lihasdystrofia: eksonin ohitusta hyödyntävät terapeuttiset exon skipping-lähestymistavat (esim. eteplirsen) pyrkivät palauttamaan osittain toimivan dystrofiinaproteiinin.
- Syövät: splicing-tekijöiden mutaatiot (esim. SF3B1, SRSF2, U2AF1) ja epänormaali splikointi voivat edistää tuumorikehitystä ja vaikuttaa hoitoresistenssiin.
Terapeuttisia strategioita ovat muun muassa antisense-oligonukleotidit, pienimolekyyliset splispaikkoja tai splicing-tekijöitä modulovat yhdisteet sekä geenieditointi. Nämä lähestymistavat pyrkivät korjaamaan haitallista splikointia tai muuttamaan splikattuja isoformeja suotuisampaan suuntaan.
Tutkimusmenetelmät
Vaihtoehtoista splikointia tutkitaan laajasti RNA-sekvensoinnilla (RNA-seq), pitkäluvun sekvensoinnilla (long-read sequencing), CLIP-sekvenoinnilla RNA-sitovien proteiinien kohdentumisen kartoittamiseksi sekä minigeeni- ja reporterijärjestelmillä. Nämä työkalut auttavat tunnistamaan splikointivariantteja, sääntelyelementtejä ja biologista vaikutusta soluissa ja kudoksissa.
Toisin sanoen, vaihtoehtoinen liittäminen lisää huomattavasti genomin koodaamien proteiinien monimuotoisuutta ja on keskeinen mekanismi sekä normaalissa solutoiminnassa että monissa sairauksissa. Usein toimimattomat tai haitalliset liitosmuunnokset käsitellään transkription jälkeisellä laadunvalvonnalla, kuten NMD:llä, ja lopulta proteiinitasolla vauriotuotteet voidaan poistaa solun proteaasisysteemeissä.
Vaihtoehtoista liittämistä on monenlaista: yleisin on eksonien ohitus. Eksoni voi sisältyä mRNA:han tietyissä olosuhteissa tai tietyissä kudoksissa ja jäädä pois mRNA:sta toisissa olosuhteissa. On olemassa splikointiaktivaattoreita, jotka edistävät tietyn splikointikohdan käyttöä, ja splikointirepressoreita, jotka vähentävät tietyn kohdan käyttöä. Uusia vaihtoehtoisen spleikkauksen tyyppejä löydetään jatkuvasti.
Sairaudet johtuvat tavanomaisesta poikkeavasta spleiskauksesta. Monet ihmisen geneettiset häiriöt johtuvat spleikkausvarianttien aiheuttamista häiriöistä. Epänormaalit liitosmuunnokset voivat myös vaikuttaa syövän kehittymiseen. Toimimattomat liitostuotteet käsitellään yleensä transkription jälkeisellä laadunvalvonnalla. Toisin sanoen entsyymit pilkkovat ne.