Entsyymit – määritelmä, toiminta ja merkitys solussa
Entsyymit: mikä ne ovat, miten ne toimivat ja miksi ne ovat ratkaisevia solussa — proteiinikatalyytit, jotka nopeuttavat biokemiallisia reaktioita. Lue lisää.
Entsyymit ovat solujen proteiinimolekyylejä, jotka toimivat biologisina katalyytteinä. Entsyymit nopeuttavat kemiallisia reaktioita elimistössä, mutta ne eivät kulu prosessissa, joten niitä voidaan käyttää yhä uudelleen ja uudelleen.
Lähes kaikki elävien olentojen biokemialliset reaktiot tarvitsevat entsyymejä. Entsyymin avulla kemialliset reaktiot etenevät paljon nopeammin kuin ilman entsyymiä.p39 Muita biokatalyyttejä ovat katalyyttiset RNA-molekyylit, joita kutsutaan ribosyymeiksi.
Reaktion alussa olevia aineita kutsutaan substraateiksi. Reaktion lopussa olevat aineet ovat tuotteita. Entsyymit käsittelevät substraatteja ja muuttavat ne tuotteiksi. Entsyymien tutkimusta kutsutaan entsymologiaksi.
Anselme Payen löysi ensimmäisen entsyymin vuonna 1833.
Miten entsyymit toimivat?
Entsyymin toiminnan keskeinen osa on sen aktivointi- eli aktiivinen kohta, johon substraatti sitoutuu. Kun substraatti ja entsyymi kohtaavat, tapahtuu usein rakenteellinen muutos entsyymissä (ns. induced fit), joka parantaa reaktion todennäköisyyttä. Entsyymit alentavat reaktion aktivaatioväylän energiaa, jolloin reaktio etenee paljon nopeammin kuin spontaanisti.
Rakenne ja spesifisyys
Suurin osa entsyymeistä on proteiineja ja niiden toiminta riippuu kolmio- ja neljännäisrakenteesta. Entsyymit ovat usein hyvin substraattispesifisiä: yksi entsyymi voi tunnistaa vain tietynlaisen sidoksen tai molekyylirakenteen. Nimitykset päättyvät suomalaisessa terminologiassa usein päätteeseen -aasi (esim. amylaasi, lipaasi, proteaasi), joskin poikkeuksia on (esim. DNA-polymeraasi).
Koentsyymit ja kofaktorit
Monet entsyymit tarvitsevat toimiakseen myös ei-proteiinisia tekijöitä:
- Kofaktorit: metallionit kuten Mg2+, Zn2+ tai Fe2+/Fe3+.
- Koentsyymit: orgaanisia molekyylejä, usein vitamiineista johdettuja (esim. NAD+, FAD, koentsyymi A), jotka kuljettavat elektroneja tai kemiallisia ryhmiä reaktioissa.
Tekijät, jotka vaikuttavat entsyymin toimintaan
- Lämpötila: Kohoava lämpö nopeuttaa tyypillisesti reaktiota tiettyyn pisteeseen asti, mutta liian korkea lämpö aiheuttaa entsyymin denaturoitumisen ja toiminnan menetyksen.
- pH: Jokaisella entsyymillä on optimaalinen pH-arvo; poikkeamat voivat muuttaa entsyymin varaustilaa ja rakenteellista sopivuutta.
- Substraatin ja entsyymin konsentraatio: Korkea substraattipitoisuus voi johtaa kyllästymispisteeseen, jossa reaktion nopeus ei enää kasva (Vmax). Kinetiikassa tämä kuvataan usein Michaelis–Mentenin mallilla ja Km‑arvolla.
- Inhibiittorit: Kilpailevat ja ei‑kilpailevat estäjät voivat hidastaa tai pysäyttää entsyymin toiminnan.
Inhibiittorit ja säätely
Entsyymejä voidaan säädellä useilla tavoilla:
- Kilpaileva inhibiittori sitoutuu aktiiviseen kohtaan estäen substraatin pääsyn.
- Ei‑kilpaileva inhibiittori sitoutuu muuhun kohtaan, muuttaa entsyymin rakennetta ja heikentää katalyyttistä kykyä.
- Irreversiibeli inhibiittori sitoutuu pysyvästi ja tuhoaa entsyymin toiminnan.
- Alosterinen säätely ja kovalenttinen modifikaatio (esim. fosforylaatio) muuttavat entsyymin aktiivisuutta soluissa vastaamaan metabolisia tarpeita.
Entsyymien merkitys solussa ja sovellukset
Entsyymit ovat keskeisiä energia‑aineenvaihdunnassa, DNA:n replikaatiossa ja korjauksessa, proteiinien hajotuksessa ja monissa muissa soluprosesseissa. Niillä on laaja käyttö myös teollisuudessa ja lääketieteessä:
- Elintarviketeollisuus: entsyymit parantavat prosesseja (esim. amylaasit tärkkelyksen hajotukseen).
- Lääkkeet: entsyymi-inhibiittorit toimivat monien tautien hoidossa (esim. ACE‑estäjät, proteaasin estäjät HIV‑hoidossa).
- Diagnostiikka: entsyymiaktivaatiot ja -mittaukset ovat keskeisiä laboratoriotesteissä (esim. ALAT, amylaasi).
- Biotekniikka ja ympäristönsuojelu: entsyymit katalysoivat kemiallisia reaktioita ympäristöystävällisemmin ja ovat keskeisiä biokatalyyteissä, immobilisoidut entsyymit parantavat toistettavuutta teollisuusprosesseissa.
Historialliset ja erityistapaukset
Anselme Payen eristi vuonna 1833 diastaasia, pidettynä ensimmäisenä tunnistettuna entsyyminä. Sittemmin selvisi, että suurin osa entsyymeistä on proteiineja, mutta myös ribosyymit (katalyyttinen RNA) voivat toimia entsyymeinä tietyissä reaktioissa, kuten RNA:n pilkkomisessa.
Yhteenveto
Entsyymit ovat elintärkeitä biologisia katalyyttejä, jotka tekevät solun kemiallisista reaktioista nopeita ja tehokkaita. Niiden toiminta perustuu tarkkaan rakenteeseen, spesifisyyteen ja usein myös apumolekyyleihin. Entsyymien tuntemus on keskeistä sekä peruselintojen ymmärtämisessä että niiden hyödyntämisessä lääketieteessä, teollisuudessa ja tutkimuksessa.
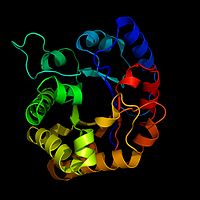
TIM-nimisen entsyymin nauhakaavio

TIM-nimisen entsyymin nauhakaavio
Entsyymin rakenne
Erilaisia entsyymejä on tuhansia, ja kukin niistä on ominainen sille reaktiolle, jota se katalysoi. Entsyymeillä on nimet, jotka kertovat, mitä ne tekevät. Entsyymien nimet päättyvät yleensä -aseen osoittaakseen, että ne ovat entsyymejä. Esimerkkejä tästä ovat ATP-syntaasi. Se valmistaa kemikaalia nimeltä ATP. Toinen esimerkki on DNA-polymeraasi. Se lukee ehjän DNA-juosteen ja käyttää sitä mallina uuden juosteen valmistamiseen.Yksi esimerkki entsyymistä on syljessä esiintyvä amylaasi. Se hajottaa tärkkelysmolekyylit pienemmiksi glukoosi- ja maltoosimolekyyleiksi. Toinen entsyymityyppi on lipaasi. Se hajottaa rasvat pienemmiksi molekyyleiksi, rasvahapoiksi ja glyseroliksi.d
Proteaasit ovat kokonainen entsyymiluokka. Ne hajottavat muita entsyymejä ja proteiineja takaisin aminohapoiksi. Nukleaasit ovat entsyymejä, jotka leikkaavat DNA:ta tai RNA:ta, usein tietyssä kohdassa molekyyliä.
Entsyymit eivät ainoastaan hajota suuria kemikaaleja pienemmiksi kemikaaleiksi. Toiset entsyymit ottavat pienempiä kemikaaleja ja rakentavat niistä suurempia kemikaaleja ja tekevät monia muita kemiallisia tehtäviä. Alla olevassa luokittelussa luetellaan päätyypit.
Biokemistit piirtävät usein kuvan entsyymistä, jota käytetään visuaalisena apuvälineenä tai karttana entsyymistä. Tämä on vaikeaa, koska entsyymissä voi olla satoja tai tuhansia atomeja. Biokemistit eivät voi piirtää kaikkia näitä yksityiskohtia. Sen sijaan he käyttävät nauhamalleja entsyymien kuvina. Nauhamalleilla voidaan näyttää entsyymin muoto ilman, että jokaista atomia tarvitsee piirtää.
Useimmat entsyymit eivät toimi, elleivät lämpötila ja pH ole juuri oikeat. Nisäkkäillä oikea lämpötila on yleensä noin 37o C (ruumiinlämpö). Oikea pH voi vaihdella suuresti. Pepsiini on esimerkki entsyymistä, joka toimii parhaiten, kun pH on noin 1,5.
Entsyymin kuumentaminen tietyn lämpötilan yläpuolelle tuhoaa entsyymin pysyvästi. Proteaasi hajottaa sen ja kemikaaleja käytetään uudelleen.
Jotkin kemikaalit voivat auttaa entsyymiä tekemään työnsä entistä paremmin. Näitä kutsutaan aktivaattoreiksi. Joskus kemikaali voi hidastaa entsyymin toimintaa tai jopa saada entsyymin toimimattomaksi. Näitä kutsutaan inhibiittoreiksi. Useimmat lääkkeet ovat kemikaaleja, jotka joko nopeuttavat tai hidastavat jonkin entsyymin toimintaa ihmiskehossa.
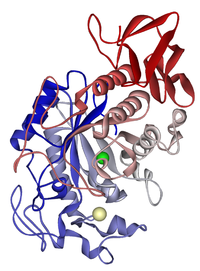
Syljen amylaasi: kloridi-ioni vihreä; kalsium beige
Entsyymin rakenne
Erilaisia entsyymejä on tuhansia, ja kukin niistä on ominainen sille reaktiolle, jota se katalysoi. Entsyymeillä on nimet, jotka kertovat, mitä ne tekevät. Entsyymien nimet päättyvät yleensä -aseen osoittaakseen, että ne ovat entsyymejä. Esimerkkejä tästä ovat ATP-syntaasi. Se tuottaa kemikaalia nimeltä ATP. Toinen esimerkki on DNA-polymeraasi. Se lukee ehjän DNA-juosteen ja käyttää sitä mallina uuden juosteen valmistamiseen.Yksi esimerkki entsyymistä on syljessä esiintyvä amylaasi. Se hajottaa tärkkelysmolekyylit pienemmiksi glukoosi- ja maltoosimolekyyleiksi. Toinen entsyymityyppi on lipaasi. Se hajottaa rasvat pienemmiksi molekyyleiksi, rasvahapoiksi ja glyseroliksi.d
Proteaasit ovat kokonainen entsyymiluokka. Ne hajottavat muita entsyymejä ja proteiineja takaisin aminohapoiksi. Nukleaasit ovat entsyymejä, jotka leikkaavat DNA:ta tai RNA:ta, usein tietyssä kohdassa molekyyliä.
Entsyymit eivät ainoastaan hajota suuria kemikaaleja pienemmiksi kemikaaleiksi. Toiset entsyymit ottavat pienempiä kemikaaleja ja rakentavat niistä suurempia kemikaaleja ja tekevät monia muita kemiallisia tehtäviä. Alla olevassa luokittelussa luetellaan päätyypit.
Biokemistit piirtävät usein kuvan entsyymistä, jota käytetään visuaalisena apuvälineenä tai karttana entsyymistä. Tämä on vaikeaa, koska entsyymissä voi olla satoja tai tuhansia atomeja. Biokemistit eivät voi piirtää kaikkia näitä yksityiskohtia. Sen sijaan he käyttävät nauhamalleja entsyymien kuvina. Nauhamalleilla voidaan näyttää entsyymin muoto ilman, että jokaista atomia tarvitsee piirtää.
Useimmat entsyymit eivät toimi, elleivät lämpötila ja pH ole juuri oikeat. Nisäkkäillä oikea lämpötila on yleensä noin 37o C (ruumiinlämpö). Oikea pH voi vaihdella suuresti. Pepsiini on esimerkki entsyymistä, joka toimii parhaiten, kun pH on noin 1,5.
Entsyymin kuumentaminen tietyn lämpötilan yläpuolelle tuhoaa entsyymin pysyvästi. Proteaasi hajottaa sen ja kemikaaleja käytetään uudelleen.
Jotkin kemikaalit voivat auttaa entsyymiä tekemään työnsä entistä paremmin. Näitä kutsutaan aktivaattoreiksi. Joskus kemikaali voi hidastaa entsyymin toimintaa tai jopa saada entsyymin toimimattomaksi. Näitä kutsutaan inhibiittoreiksi. Useimmat lääkkeet ovat kemikaaleja, jotka joko nopeuttavat tai hidastavat jonkin entsyymin toimintaa ihmiskehossa.

Syljen amylaasi: kloridi-ioni vihreä; kalsium beige
Lukko- ja avainmalli
Entsyymit ovat hyvin spesifisiä. Emil Fischer esitti vuonna 1894, että sekä entsyymillä että substraatilla on tietyt toisiaan täydentävät geometriset muodot, jotka sopivat täsmälleen toisiinsa. Tätä kutsutaan usein "lukko-avain-malliksi". Tämä malli ei kuitenkaan selitä, mitä seuraavaksi tapahtuu.Vuonna 1958 Daniel Koshland ehdotti lukko-avain-mallin muuttamista. Koska entsyymit ovat melko joustavia rakenteita, aktiivinen alue muotoutuu uudelleen vuorovaikutuksessa substraatin kanssa. Tämän seurauksena substraatti ei yksinkertaisesti sitoudu jäykkään aktiiviseen kohtaan. Aktiivisen alueen aminohappojen sivuketjut taipuvat sellaisiin asentoihin, että entsyymi tekee katalyyttisen työnsä. Joissakin tapauksissa, kuten glykosidaaseissa, myös substraattimolekyyli muuttaa hieman muotoaan, kun se siirtyy aktiiviseen kohtaan.
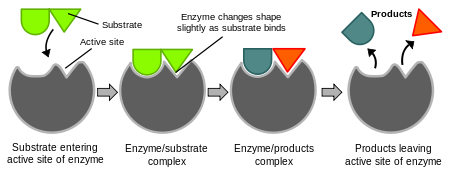
Kaaviot, jotka osoittavat entsyymin toimintaa koskevan indusoidun sopivuuden hypoteesin.
Lukko- ja avainmalli
Entsyymit ovat hyvin spesifisiä. Emil Fischer esitti vuonna 1894, että sekä entsyymillä että substraatilla on tietyt toisiaan täydentävät geometriset muodot, jotka sopivat täsmälleen toisiinsa. Tätä kutsutaan usein "lukko-avain-malliksi". Tämä malli ei kuitenkaan selitä, mitä seuraavaksi tapahtuu.Vuonna 1958 Daniel Koshland ehdotti lukko-avain-mallin muuttamista. Koska entsyymit ovat melko joustavia rakenteita, aktiivinen alue muotoutuu uudelleen vuorovaikutuksessa substraatin kanssa. Tämän seurauksena substraatti ei yksinkertaisesti sitoudu jäykkään aktiiviseen kohtaan. Aktiivisen alueen aminohappojen sivuketjut taipuvat sellaisiin asentoihin, että entsyymi tekee katalyyttisen työnsä. Joissakin tapauksissa, kuten glykosidaaseissa, myös substraattimolekyyli muuttaa hieman muotoaan, kun se siirtyy aktiiviseen kohtaan.

Kaaviot, jotka osoittavat entsyymin toimintaa koskevan indusoidun sopivuuden hypoteesin.
Toiminto
Entsyymireaktion yleinen yhtälö on:
Substraatti + entsyymi -> Substraatti:entsyymi -> Tuote:entsyymi -> Tuote + entsyymi.
Entsyymit alentavat reaktion aktivaatioenergiaa muodostamalla substraatin kanssa välikompleksin. Tätä kompleksia kutsutaan entsyymi-substraatti-kompleksiksi.
Esimerkiksi sakkaraasi, joka on 400 kertaa suurempi kuin sen substraatti sakkaroosi, pilkkoo sakkaroosin sen sisältämiksi sokereiksi, jotka ovat glukoosi ja fruktoosi. Sakarraasi taivuttaa sakkaroosia ja jännittää glukoosin ja fruktoosin välistä sidosta. Vesimolekyylit liittyvät mukaan ja tekevät halkaisun sekunnin murto-osassa. Entsyymeillä on nämä keskeiset ominaisuudet:
- Ne ovat katalyyttisiä. Ne lisäävät yleisesti reaktionopeutta 10 miljardia kertaa.p39 Itse entsyymi ei muutu reaktiossa.
- Ne ovat tehokkaita pieninä määrinä. Yksi entsyymimolekyyli voi muuntaa 1000 substraattimolekyyliä minuutissa, ja joidenkin tiedetään muuttavan 3 miljoonaa molekyyliä minuutissa.p39
- Ne ovat hyvin spesifisiä. Yksi entsyymi suorittaa vain yhden monista reaktioista, joihin substraatti kykenee.
Entsyymiaktiivisuuden valvonta
Entsyymien toimintaa ohjataan solussa viidellä eri tavalla.
- Entsyymituotantoa (entsyymigeenien transkriptio ja translaatio) voidaan lisätä tai vähentää solun ympäristön muutosten seurauksena. Tätä geenien säätelyn muotoa kutsutaan entsyymien induktioksi ja inhibitioksi. Esimerkiksi antibiooteille, kuten penisilliinille, vastustuskykyisissä bakteereissa indusoituu entsyymejä, jotka hydrolysoivat penisilliinimolekyylin.
- Entsyymejä voi esiintyä eri solukompartimenteissa. Esimerkiksi rasvahappoja syntetisoi yksi joukko entsyymejä sytosolissa, endoplasmisessa retikulumissa ja Golgin laitteessa. Sen jälkeen eri entsyymijoukko käyttää niitä energianlähteenä mitokondrioissa.
- Entsyymejä voidaan säädellä niiden omilla tuotteilla. Esimerkiksi lopputuote(t) estää usein yhtä reitin ensimmäisistä entsyymeistä. Tällaista säätelymekanismia kutsutaan negatiiviseksi takaisinkytkennäksi, koska tuotetun lopputuotteen määrää säätelee sen oma pitoisuus. Tämä estää soluja tuottamasta liikaa entsyymiä. Entsyymitoiminnan säätely auttaa pitämään elävien organismien sisäisen ympäristön vakaana.
- Entsyymejä voidaan säädellä muuttamalla niitä tuotannon jälkeen. Esimerkkinä voidaan mainita polypeptidiketjun pilkkominen. Kymotrypsiini, ruoansulatusproteaasi, tuotetaan haimassa inaktiivisessa muodossa ja kuljetetaan tässä muodossa mahalaukkuun, jossa se aktivoituu. Tämä estää entsyymiä pilkkomasta haimaa tai muita kudoksia ennen kuin se pääsee suolistoon. Tällaista inaktiivista entsyymin esiastetta kutsutaan zymogeeniksi.
- Jotkin entsyymit voivat aktivoitua, kun ne siirtyvät eri ympäristöön (esim. korkeasta pH:sta matalaan pH:han). Esimerkiksi influenssaviruksen hemagglutiniini aktivoituu muodon muuttuessa. Tämä johtuu happamista olosuhteista, jotka vallitsevat isäntäsolun lysosomissa.
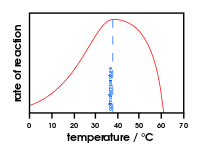
Kaavio, joka osoittaa lämpötilan muutoksen vaikutuksen entsyymiaktiivisuuteen.
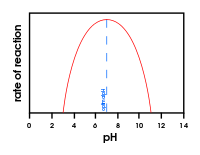
Kaavio, joka osoittaa pH:n muutoksen vaikutuksen entsyymiaktiivisuuteen.
Toiminto
Entsyymireaktion yleinen yhtälö on:
Substraatti + entsyymi -> Substraatti:entsyymi -> Tuote:entsyymi -> Tuote + entsyymi.
Entsyymit alentavat reaktion aktivaatioenergiaa muodostamalla substraatin kanssa välikompleksin. Tätä kompleksia kutsutaan entsyymi-substraatti-kompleksiksi.
Esimerkiksi sakkaraasi, joka on 400 kertaa suurempi kuin sen substraatti sakkaroosi, pilkkoo sakkaroosin sen sisältämiksi sokereiksi, jotka ovat glukoosi ja fruktoosi. Sakarraasi taivuttaa sakkaroosia ja jännittää glukoosin ja fruktoosin välistä sidosta. Vesimolekyylit liittyvät mukaan ja tekevät halkaisun sekunnin murto-osassa. Entsyymeillä on nämä keskeiset ominaisuudet:
- Ne ovat katalyyttisiä. Ne lisäävät yleisesti reaktionopeutta 10 miljardia kertaa.p39 Itse entsyymi ei muutu reaktiossa.
- Ne ovat tehokkaita pieninä määrinä. Yksi entsyymimolekyyli voi muuntaa 1000 substraattimolekyyliä minuutissa, ja joidenkin tiedetään muuttavan 3 miljoonaa molekyyliä minuutissa.p39
- Ne ovat hyvin spesifisiä. Yksi entsyymi suorittaa vain yhden monista reaktioista, joihin substraatti kykenee.
Entsyymiaktiivisuuden valvonta
Entsyymien toimintaa ohjataan solussa viidellä eri tavalla.
- Entsyymituotantoa (entsyymigeenien transkriptio ja translaatio) voidaan lisätä tai vähentää solun ympäristön muutosten seurauksena. Tätä geenien säätelyn muotoa kutsutaan entsyymien induktioksi ja inhibitioksi. Esimerkiksi antibiooteille, kuten penisilliinille, vastustuskykyisissä bakteereissa indusoituu entsyymejä, jotka hydrolysoivat penisilliinimolekyylin.
- Entsyymejä voi esiintyä eri solukompartimenteissa. Esimerkiksi rasvahappoja syntetisoi yksi joukko entsyymejä sytosolissa, endoplasmisessa retikulumissa ja Golgin laitteessa. Sen jälkeen eri entsyymijoukko käyttää niitä energianlähteenä mitokondrioissa.
- Entsyymejä voidaan säädellä niiden omilla tuotteilla. Esimerkiksi lopputuote(t) estää usein yhtä reitin ensimmäisistä entsyymeistä. Tällaista säätelymekanismia kutsutaan negatiiviseksi takaisinkytkennäksi, koska tuotetun lopputuotteen määrää säätelee sen oma pitoisuus. Tämä estää soluja tuottamasta liikaa entsyymiä. Entsyymitoiminnan säätely auttaa pitämään elävien organismien sisäisen ympäristön vakaana.
- Entsyymejä voidaan säädellä muuttamalla niitä tuotannon jälkeen. Esimerkkinä voidaan mainita polypeptidiketjun pilkkominen. Kymotrypsiini, ruoansulatusproteaasi, tuotetaan haimassa inaktiivisessa muodossa ja kuljetetaan tässä muodossa mahalaukkuun, jossa se aktivoituu. Tämä estää entsyymiä pilkkomasta haimaa tai muita kudoksia ennen kuin se pääsee suolistoon. Tällaista inaktiivista entsyymin esiastetta kutsutaan zymogeeniksi.
- Jotkin entsyymit voivat aktivoitua, kun ne siirtyvät eri ympäristöön (esim. korkeasta pH:sta matalaan pH:han). Esimerkiksi influenssaviruksen hemagglutiniini aktivoituu muodon muuttuessa. Tämä johtuu happamista olosuhteista, jotka vallitsevat isäntäsolun lysosomissa.

Kaavio, joka osoittaa lämpötilan muutoksen vaikutuksen entsyymiaktiivisuuteen.

Kaavio, joka osoittaa pH:n muutoksen vaikutuksen entsyymiaktiivisuuteen.
Entsyymi-inhibiittorit
Inhibiittoreita voidaan käyttää estämään entsyymin sitoutuminen substraattiin. Näin voidaan hidastaa entsyymin ohjaamaa reaktiota. Inhibiittorit sopivat löyhästi tai osittain entsyymin aktiiviseen kohtaan. Tämä estää tai hidastaa entsyymi-substraatti-kompleksin muodostumista.
Entsyymi-inhibiittorit
Inhibiittoreita voidaan käyttää estämään entsyymin sitoutuminen substraattiin. Näin voidaan hidastaa entsyymin ohjaamaa reaktiota. Inhibiittorit sopivat löyhästi tai osittain entsyymin aktiiviseen kohtaan. Tämä estää tai hidastaa entsyymi-substraatti-kompleksin muodostumista.
Denaturaatio
Denaturoituminen on entsyymin aktiivisen alueen peruuttamaton muutos, joka aiheutuu äärimmäisestä lämpötilan tai pH:n muutoksesta. Se vähentää reaktionopeutta, koska substraattimolekyyli ei mahdu aktiiviseen kohtaan, joten tuotteita ei voi muodostua.
Denaturaatio
Denaturoituminen on entsyymin aktiivisen alueen peruuttamaton muutos, joka aiheutuu äärimmäisestä lämpötilan tai pH:n muutoksesta. Se vähentää reaktionopeutta, koska substraattimolekyyli ei mahdu aktiiviseen kohtaan, joten tuotteita ei voi muodostua.
Kofaktorit
Kofaktorit eli koentsyymit ovat apumolekyylejä, joita tarvitaan entsyymin toimintaan. Ne eivät ole proteiineja, ja ne voivat olla orgaanisia tai epäorgaanisia molekyylejä. Molemmat molekyylityypit sisältävät joskus metalli-ionin keskellä, kuten Mg-2+, Cu-2+, Mn-2+ tai rauta-rikkiklusterit. Tämä johtuu siitä, että tällaiset ionit voivat toimia elektronin luovuttajina, mikä on tärkeää monissa reaktioissa. Entsyymien erilaisten pienten apulaisten tarve on perussyy siihen, miksi eläimet, meidät mukaan lukien, tarvitsevat hivenaineita ja vitamiineja.
Kofaktorit
Kofaktorit eli koentsyymit ovat apumolekyylejä, joita tarvitaan entsyymin toimintaan. Ne eivät ole proteiineja, ja ne voivat olla orgaanisia tai epäorgaanisia molekyylejä. Molemmat molekyylityypit sisältävät joskus metalli-ionin keskellä, kuten Mg-2+, Cu-2+, Mn-2+ tai rauta-rikkiklusterit. Tämä johtuu siitä, että tällaiset ionit voivat toimia elektronin luovuttajina, mikä on tärkeää monissa reaktioissa. Entsyymien erilaisten pienten apulaisten tarve on perussyy siihen, miksi eläimet, meidät mukaan lukien, tarvitsevat hivenaineita ja vitamiineja.
Luokitus
Kansainvälinen biokemian liitto on luokitellut entsyymit. Sen entsyymikomitea on ryhmitellyt kaikki tunnetut entsyymit kuuteen luokkaan:
- Oksido-reduktaasit: katalysoivat elektronien siirtoa.
- Transferaasit: siirtävät funktionaalisen ryhmän yhdestä molekyylistä toiseen.
- Hydrolaasit: lisäävät -OH (hydroksyyli)-ryhmän.
- Lyaasit: pilkkovat kemiallisia sidoksia ja lisäävät usein kaksoissidoksia tai rengasrakennetta.
- Isomeraasit: A -> B, jossa B on A:n isomeeri.
- Ligaasit: yhdistävät kaksi suurta molekyyliä: Ab + C -> A-C + b
Yksittäisille entsyymeille annetaan nelinumeroinen numero, joka luokittelee ne tietokannassa. p145
Luokitus
Kansainvälinen biokemian liitto on luokitellut entsyymit. Sen entsyymikomitea on ryhmitellyt kaikki tunnetut entsyymit kuuteen luokkaan:
- Oksido-reduktaasit: katalysoivat elektronien siirtoa.
- Transferaasit: siirtävät funktionaalisen ryhmän yhdestä molekyylistä toiseen.
- Hydrolaasit: lisäävät -OH (hydroksyyli)-ryhmän.
- Lyaasit: pilkkovat kemiallisia sidoksia ja lisäävät usein kaksoissidoksia tai rengasrakennetta.
- Isomeraasit: A -> B, jossa B on A:n isomeeri.
- Ligaasit: yhdistävät kaksi suurta molekyyliä: Ab + C -> A-C + b
Yksittäisille entsyymeille annetaan nelinumeroinen numero, joka luokittelee ne tietokannassa. p145
Entsyymien käyttö
Entsyymejä käytetään kaupallisesti:
- vauvanruoan valmistaminen - vauvojen ruoan esiruoan valmistelu
- suklaiden keskikappaleiden pehmentäminen
- biologinen pesujauhe - joka sisältää proteaasientsyymejä, jotka hajottavat lian ja lian. Se hajottaa suuret, liukenemattomat molekyylit pieniksi, liukeneviksi molekyyleiksi. Se toimii alhaisemmassa lämpötilassa, joten energiaa tarvitaan vähemmän (termostabiili).
Entsyymien käyttö
Entsyymejä käytetään kaupallisesti:
- vauvanruoan valmistaminen - vauvojen ruoan esiruoan valmistelu
- suklaiden keskikappaleiden pehmentäminen
- biologinen pesujauhe - joka sisältää proteaasientsyymejä, jotka hajottavat lian ja lian. Se hajottaa suuret, liukenemattomat molekyylit pieniksi, liukeneviksi molekyyleiksi. Se toimii alhaisemmassa lämpötilassa, joten energiaa tarvitaan vähemmän (termostabiili).
Aiheeseen liittyvät sivut
- Burst-kinetiikka
Aiheeseen liittyvät sivut
- Burst-kinetiikka
Kysymyksiä ja vastauksia
K: Mikä on entsyymi?
V: Entsyymi on solujen proteiinimolekyyli, joka toimii biologisena katalysaattorina.
K: Mikä on entsyymien tehtävä elimistössä?
V: Entsyymit nopeuttavat kemiallisia reaktioita elimistössä, mutta ne eivät kulu prosessissa, joten niitä voidaan käyttää yhä uudelleen ja uudelleen.
K: Tarvitaanko elävien olentojen kaikissa biokemiallisissa reaktioissa entsyymejä?
V: Kyllä, lähes kaikki elävien olentojen biokemialliset reaktiot tarvitsevat entsyymejä.
K: Mitä ovat substraatit?
V: Substraatit ovat aineita, jotka ovat reaktion alussa.
K: Mitä ovat tuotteet?
V: Tuotteet ovat aineita reaktion lopussa.
K: Miksi kutsutaan entsyymien tutkimusta?
V: Entsyymien tutkimusta kutsutaan entsymologiaksi.
K: Kuka löysi ensimmäisen entsyymin?
V: Ensimmäisen entsyymin löysi Anselme Payen vuonna 1833.
Etsiä