Absoluuttinen nollapiste on lämpötila, jossa aineen hiukkaset (molekyylit ja atomit) ovat mahdollisimman alhaisissa energiatiloissa. Monet pitävät virheellisesti ajatelmaa, että hiukkaset "pysähtyisivät" kokonaan absoluuttisessa nollapisteessä. Tämä ei kuitenkaan pidä paikkaansa: kvanttifysiikan mukaan hiukkasilla on aina niin kutsuttu nollapiste-energia. Nollapiste-energia ja Heisenbergin epävarmuusperiaate estävät hiukkasten täydellisen paikallaan pysymisen, koska tarkan sijainnin ja liikemäärän samanaikainen mittaaminen on rajallista.
Miksi absoluuttista nollaa ei saavuteta
Termodynamiikan kolmas laki muotoilee käytännössä, että absoluuttista nollapistettä ei voida saavuttaa finiittisessä prosessissa: jokaista jäähdytysaskelta kohti tarvitaan aina yhä enemmän työtä tai järjestelyä ja lopulta määrättömän monta askelta. Käytännössä lähelle 0 K:ta pääseminen vaatii yhä hienovaraisempia menetelmiä ja lopulta rajattoman ajan tai resurssit, joten täydellinen 0 K on saavuttamattomissa.
Kuinka lähelle nollaa on päästy ja miten
Tutkijat ovat päässeet erittäin lähelle absoluuttista nollaa. Yksi ennätys on noin 100 pK (sata pikokelviniä, eli noin 10⁻¹⁰ K) absoluuttisen nollapisteen yläpuolella. Eri kokeissa mitataan hyvin eri tapaisia lämpötiloja (esimerkiksi atomien liike-energia vs. systeemin termodynaaminen lämpötila), joten luvuissa on kontekstia.
Jäähdytykseen käytetään useita menetelmiä, joista yleisimpiä ja tärkeimpiä ovat esimerkiksi:
- Laserkylmäys ja Doppler-jäähdytys: lasereita käytetään atomien liikkeen hidastamiseen ja siten niiden kineettisen energian pienentämiseen.
- Esi- ja jatkojäähdytys: haihdutusjäähdytys (evaporative cooling) ja magneto-optinen anstabileeraus, joita käytetään Bose–Einstein-kondensaattien ja muiden erittäin kylmien atomipilvien luomiseksi.
- Adiabatic demagnetization ja diluutiokylmälaitteet: käytetään hyvin matalien lämpötilojen (mK–μK) saavuttamiseen erityisesti kiinteissä aineissa ja elektronijärjestelmissä.
- Sähkö- ja lämpöeristys sekä kokeelliset menetelmät, jotka minimoivat ympäristöstä tulevan lämmönsiirron.
Mitä aineelle tapahtuu lähellä 0 K
Miltei kaikkien aineiden terminen liike vähenee, mutta kvanttivaikutukset korostuvat. Esimerkkejä ilmiöistä, joita esiintyy hyvin alhaisissa lämpötiloissa:
- Bose–Einstein-kondensaatio: bosoneista koostuvat atomit voivat laskea samaan kvanttitilaan ja muodostaa makroskooppisen kvanttitilan.
- Superjohtavuus: monissa materiaaleissa sähkönjohtavuus kasvaa ja resistanssi voi laskea nollaan tietyllä kriittisellä lämpötilalla, mutta tämä koskee vain erityisiä aineita ja lämpötila-alueita — kaikki aineet eivät siis muutu täydellisiksi johteiksi automaattisesti.
- Supersisä ja superfluidisuus: jotkin aineet, kuten helium-4, muuttuvat supernesteiksi ja saavat ominaisuuksia, kuten kitkattoman virtauksen.
- Lattian värähtelyt (fononit) minimoituvat mutta nollapiste-värähtelyt säilyvät kvanttisesti.
On tärkeää huomata, että lause "tässä vaiheessa hiukkasten paine on nolla" on liian yksinkertaistava: ideaalikaasun paine lähestyy nollaa, jos hiukkasten kineettinen energia lähestyy nollaa, mutta kiinteissä aineissa ja kvanttisysteemeissä toimivat muut ilmiöt ja nollapiste-energia estävät yksinkertaisen nolla-arvon monissa tapauksissa.
Yhteys lämpötila-asteikkoihin ja termodynamiikan toiseen lakiin
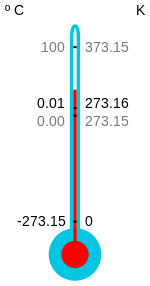
Kelvin- ja Rankinen lämpötila-asteikot on määritelty siten, että absoluuttinen nollapiste on 0 kelviniä (K) tai 0 astetta Rankinea (°R). Celsius- ja Fahrenheit-asteikot ovat sidottuja näihin siten, että absoluuttinen nollapiste vastaa −273,15 °C tai −459,67 °F.
Termodynamiikan toinen laki kertoo, että lämpövoimalla toimivien koneiden hyötysuhdetta rajoittavat lämpötilaerot: täysin häviötön (100 %) kone ei ole mahdollinen, koska osa energiasta pitää aina vapautua lämmöksi ympäristöön. Käytännössä hyötysuhdetta voidaan parantaa kasvattamalla kuuman lähteen lämpötilaa ja/tai laskemalla kylmän lähteen lämpötilaa, mutta absoluuttista nollaa ei voi saavuttaa loppuun asti, joten ideaalista 100 % hyötysuhdetta ei tule.
Yhteenveto: absoluuttinen nollapiste merkitsee fysiikan mukaan pienintä mahdollista lämpötilaa, mutta kvanttiefektit ja termodynamiikan periaatteet estävät täydellisen saavuttamisen. Lähelle 0 K:ta päästään moderneilla jäähdytysmenetelmillä, ja tällaiset olosuhteet paljastavat monia erikoisia kvantti-ilmiöitä, kuten Bose–Einstein-kondensaatioita ja superjohtavuutta.