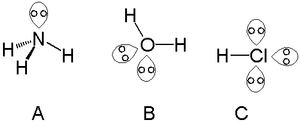
Yksinäinen pari tarkoittaa kahden elektronin paria, joka kuuluu samaan atomiorbitaalin tai -kuoren tilaan mutta ei osallistu atomien väliseen sidokseen. Ne sijaitsevat yleensä atomin uloimmassa, eli valenssikuoressa, ja yhdessä sidoksiin osallistuvien elektronien kanssa muodostavat atomin valenssielektronien kokonaismäärän. Yksinäiset parit ovat paikallisia ja usein energialtaan korkeampia kuin sidoselektronit, mutta niiden tarkka energia riippuu atomista ja ympäristöstä (elektronegatiivisuus, hybridisaatio, solvaatio jne.).
Rooli kemiallisissa reaktioissa
Yksinäiset parit toimivat usein reaktiivisina elektronipareina: ne voivat toimia nukleofiileina, jotka luovuttavat elektroniparin ja reagoivat elektrofiilien kanssa muodostaen uusia sidoksia. Monet nukleofiilit kantavat yksinäisiä pareja, jotka alkavat reaktion hyökkäyspisteenä. Lisäksi yksinäiset parit voivat osallistua koordinointisitoksiin, jolloin ne sitovat metalliatomin muodostaen kompleksin, tai delokalisoitua osaksi konjugoitua järjestelmää ja vaikuttaa resonanssiin.
Vaikutus molekyylin muotoon ja elektronitiheyteen
Yksinäiset parit vievät tilaa atomin ympäriltä ja niiden elektronit ovat paikallistuneempia kuin sidoselektronit. Tämän takia niiden välinen ja sidoselektronien välinen repulsio vaikuttaa molekyylin geometrian muodostumiseen. VSEPR-teorian mukaan elektroniparien välinen repulsio järjestyy siten, että parit asettuvat mahdollisimman kauas toisistaan. Repulsion suuruusjärjestys on tyypillisesti:
- yksinäinen pari – yksinäinen pari (LP–LP) > yksinäinen pari – sidospairi (LP–BP) > sidospairi – sidospairi (BP–BP)
Tämä selittää esimerkiksi, miksi veden H–O–H -kulma on noin 104,5° (kaksi yksinäistä paria pienentää kulmaa tetraedrisestä ~109,5°) ja miksi ammoniakka (NH3) on kolmiulotteinen pyramidi, ei tasainen kolmiokenttä: typellä on yksi yksinäinen pari, joka työntää sidoksia hieman kasaan.
Hybridisaatio ja vaikutus sidossogeometriaan
Yksinäiset parit sijoittuvat usein hybridiorbitaaleihin (esim. sp3 veden tapauksessa), mikä vaikuttaa siten sidosten suuntiin ja kulmiin. Joskus yksinäinen pari voi olla enemmän paikallistunut puhtaassa p-orbitaalissa (esim. tietyissä karbokationien esiasteissa tai joissain konjugaatio-tapauksissa), mikä muuttaa molekyylin elektronijakaumaa ja reaktiivisuutta.
Vaikutukset molekyylin ominaisuuksiin
- Polaarisuus ja dipolimomentti: Yksinäiset parit voivat lisätä atomin elektronitiheyttä ja vaikuttaa siten kokonaisdipoliin.
- H-tai muiden vetysidosten vastaanotto: Yksinäiset parit voivat toimia vetysidoksen vastaanottajina (esimerkiksi veden hapen yksinäiset parit vastaanottavat H–sidoksia).
- Happamuus–perussuhde (Lewis-hapetus/protoni-oton): Atomi, jossa on vapaa yksinäinen pari, voi toimia Lewis-emäksenä ja siten hapenoton tai protonin hyväksijänä.
- Formaalinen varaus: Yksinäinen pari voi kantaa kokonaisen negatiivisen varauksen, kuten hydriidilla tai halogenideilla, mikä vaikuttaa molekyylin sähköiseen rakenteeseen.
Piirrostekniikat ja laskenta
Kemiallissa Lewis-rakenteissa yksinäiset parit esitetään pisteinä atomin viereen. Kun lasketaan elektronien jakautumista ja muodollisia varauksia, yksinäiset parit on otettava huomioon täyttämään oktetteja tai muita oktettisääntöä vastaavia rakenteita. Kvanttikemialliset laskelmat (esim. molekyyliorbitaali- tai DFT-laskelmat) antavat yksityiskohtaisempaa tietoa yksinäisten parien energiasta, spatiallisesta jakautumisesta ja niiden vaikutuksesta reaktiivisuuteen.
Yhteenveto
Yksinäiset elektroniparit ovat keskeinen käsite kemiallisessa sidoksessa ja molekyylien geometriassa. Ne vaikuttavat reaktiivisuuteen, muotoon, polaarisuuteen ja kykyyn osallistua vetysidoksiin tai koordinointiin. Ymmärtäminen, miten yksinäiset parit jakautuvat ja miten ne vuorovaikuttavat sidoselektronien kanssa, auttaa selittämään monia molekyylien kemiallisia ja fysikaalisia ominaisuuksia.