Orgaanisessa kemiassa additioreaktio tapahtuu, kun kaksi molekyyliä yhdistyy ja muodostaa suuremman molekyylin. Tämä voi tapahtua vain silloin, kun toisella molekyyleistä on jo kaksois- tai kolmoissidos. Nämä voivat olla hiili-hiilisidoksia tai jopa hiili-happi, hiili-typpi ja muita. Toista kahdesta molekyylistä kutsutaan nukleofiiliksi, ja se antaa elektronit toiselle molekyylille uuden sidoksen muodostamiseksi. Toista molekyyliä kutsutaan elektrofiiliksi, ja se on se, joka saa elektronit.
Additioreaktio on eliminaatioreaktion vastakohta. Yleisiä esimerkkejä additioreaktioista ovat veden lisäys kaksoissidoksen yli ja nukleofiilinen hyökkäys karbonyyliin.
Mekanismi lyhyesti
Additioreaktioiden mekanismit vaihtelevat reaktiotyypin mukaan, mutta tyypillisiä piirteitä ovat:
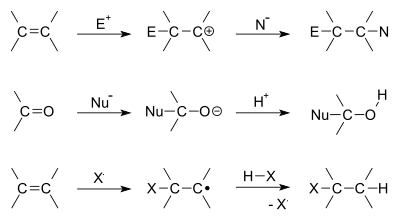
- Elektrofiilinen additio: elektronirikas kaksoissidos toimii nukleofiilinä ja hyökkää elektrofiilin kimppuun. Usein muodostuu väliaikainen karbokation (esim. HBr:n additiossa alkeeniin), jota seuraa nukleofiilin liittyminen.
- Nukleofiilinen additio: tyypillistä esimerkiksi hiiliylijakoisille (karbonyyleille), joissa nukleofiili hyökkää elektrofiiliseen hiileen ja muodostaa uuden yksinkertaisen sidoksen.
- Radikaalinen additio: vapaita radikaaleja sisältävät reaktiot (esim. peroksidi-indusoitu HBr:n additio) etenevät initiaation, propagoinnin ja terminaation kautta ja voivat johtaa anti‑Markovnikov‑tuotteisiin.
- Syklinen välivaihe: joissain reaktioissa (esim. brominaatio) muodostuu bromonium‑ionin kaltainen syklistetty välituote, joka määrää myöhemmän stereokemian.
Tyypit ja tunnusomaiset piirteet
- Elektrofiilinen additio alkeeneihin: yleisiä reaktioita ovat hydrohalogenointi (HCl, HBr), halogenointi (Br2, Cl2), hydration (H2O reaktiivisen välivaiheen kautta) ja epoksidaatio/avautuminen.
- Hydrogenaatio: H2:n additio kaksois‑ tai kolmoissidokseen katalyytin (Pd, Pt, Ni) läsnäollessa. Tyypillisesti syn-additio, eli hidrogenit lisätään samalle puolelle.
- Hydroborointiaoksidaatio: anti‑Markovnikov‑regioselektiivinen reitti, joka antaa alkoholituotteen ilman karbokationista johtuvia rearrangementeja; additio tapahtuu syn-tapauksena.
- Oxymercuration‑demercuration: antaa Markovnikov‑alkoholin ilman rearrangeerausta (ei karbokationivälivaihetta johtavassa muodossa).
- Konjugaattinen (Michael)‑additio: nukleofiilin additio α,β‑epätyydyttymän β‑hiileen (1,4‑additio), tyypillinen reaktio pelkistyneissä tai heikkojen nukleofiilien kanssa.
- Polymerisaatio (ketjuadditio): alkeenien radikaali‑ tai ionimekanismilla tapahtuva ketjuuntuva additio johtaa polymeereihin (esim. polyeteeni).
Regio‑ ja stereoselektiivisyys
- Markovnikovin sääntö: elektrofiilin (esim. H+) lisäännyttyä kaksoissidokseen, nukleofiili liittyy sinne, missä muodostuu vakaampi karbokationi (usein johtaa protonin asettumiseen vetyä sisältävälle hiilelle). Poikkeuksia syntyvät esimerkiksi radikaali‑olosuhteissa (anti‑Markovnikov) tai hydroboroinnissa.
- Stereoselektiivisyys: additio voi olla syn (molemmat ryhmät lisätään samalle puolelle) tai anti (vastakkaisille puolille). Esimerkiksi katalyyttinen hydrogenaatio on syn‑additio, kun taas halogeenien additio useimmiten antaa anti‑konfiguraation bromonium‑välivaiheen kautta.
Esimerkkejä
- HBr:n additio alkeeniin: elektrofiilinen additio, karbokationivälivaihe; radikaali‑olosuhteissa anti‑Markovnikov‑tuote voi muodostua.
- Brominaatio (Br2) alkeenille: muodostuu bromonium‑ionivälivaihe, jonka avautuminen nucleofiilillä antaa anti‑lisäyksen.
- Hydrogenaatio (H2 / Pd): kaksoissidos pelkistyy syn‑additiolla antaen alkaanin.
- Hydroborointi‑oksidaatio: antaa anti‑Markovnikov‑alkoholin syn‑additiolla (esim. BH3 → H2O2/−OH).
- Nukleofiilinen additio karbonyyliin: esimerkiksi hydriidiradikaaliin (LiAlH4, NaBH4) johtaa alkoholin muodostumiseen; tässä karbonyyli toimii elektrofiilinä.
- Konjugaattinen additio (Michael): enolaattien tai thiolien additio α,β‑epätyydyttymään tuottaa 1,4‑tuotteita.
- Polymerisaatio: eteenin radikaalinen additio johtaa polyeteenin muodostumiseen (ketjuadditio).
Miksi additioreaktiot ovat tärkeitä?
Additioreaktiot ovat keskeisiä rakentamaan ravintoaineiden, lääkkeiden ja muovien kaltaisia orgaanisia molekyylejä. Ne tarjoavat monipuolisia tapoja muuttaa kaksois‑ ja kolmoissidoksia halutuiksi funktionaalisiksi ryhmiksi säätämällä regio‑ ja stereokemiallista lopputulosta.