Suunnattu evoluutio (DE) on menetelmä, jota käytetään entsyymien tuottamiseen teollisiin tai lääketieteellisiin tarkoituksiin.
Menetelmänä on proteiinitekniikka, joka jäljittelee luonnonvalintaa.
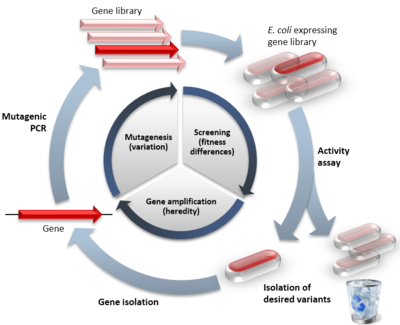
Perusajatuksena on, että geenin mutaatioita toistetaan toistuvasti, jotta saadaan aikaan muunnoskirjasto. Valinta eristää geenit, joilla on haluttu tehtävä. Ne toimivat mallina seuraavaa kierrosta varten.
Tämä voidaan tehdä in vivo (elävissä bakteeri- tai hiivasoluissa) tai in vitro (vapaasti liuoksessa tai mikropisaroissa).
Useampien mutanttien testaaminen lisää mahdollisuuksia löytää sellainen mutantti, jolla on halutut ominaisuudet.
In vivo -evoluution aikana jokainen solu (yleensä bakteeri tai hiiva) transformoidaan plasmidilla, joka sisältää eri muunnoskirjaston jäsenen. Ainoastaan kiinnostava geeni eroaa solujen välillä, ja kaikki muut geenit pidetään samoina.
Solut ilmentävät proteiinia joko sytoplasmassaan tai pinnallaan, jolloin sen toimintaa voidaan testata. Tämän formaatin etuna on, että ominaisuudet voidaan valita soluympäristössä, mikä on hyödyllistä, kun kehitettyä proteiinia tai RNA:ta aiotaan käyttää elävissä organismeissa.
Kun DE tehdään ilman soluja, siinä käytetään in vitro transkriptiotranslaatiota proteiinien tai RNA:n tuottamiseksi vapaasti liuoksessa tai keinotekoisten mikropisaroiden sisällä. Tästä on se etu, että se mahdollistaa useammat olosuhteet (esim. lämpötila, liuottimet). Sillä voidaan ilmentää proteiineja, jotka olisivat myrkyllisiä soluille. Lisäksi in vitro -evoluutiokokeissa voidaan tuottaa paljon suurempia kirjastoja (jopa 1015), koska kirjaston DNA:ta ei tarvitse lisätä soluihin. Tämä rajoittaa usein sitä, mitä voidaan tehdä.
Miten suunnattu evoluutio etenee käytännössä
Tyypillinen suunnatun evoluution työjärjestys sisältää kolme päävaihetta: 1) muunnoskirjaston luominen, 2) ilmentäminen ja fenotyypin mittaaminen tai valinta, sekä 3) parhaiden varianttien uudelleenkäyttäminen uusiin kierroksiin. Prosessi toistetaan iteratiivisesti, kunnes saavutetaan haluttu parannus.
Muunnostekniikat (kirjaston luominen)
- Error-prone PCR — virhealtis DNA-amplifikaatio, joka lisää pistemutaatioita satunnaisesti.
- DNA-shuffling — eri varianttien segmenttien rekombinointi, joka yhdistää hyödyllisiä mutaatioita.
- Saturaatio- ja kohdennettu mutageneesi — yksittäisten aminohappojen tai paikallisten alueiden systemaattinen muuttaminen.
- Mutator-kannat ja in vivo -mutageneesi — bakteerikantojen käyttö, joissa mutaatiotahti on kohonnut.
Genotyypin ja fenotyypin liittäminen
On tärkeää, että jokaisen proteiini- tai RNA-variantin genotyyppi voidaan liittää sen mitattuun fenotyyppiin. Tämä onnistuu eri tavoilla:
- Solupohjainen valinta — kasvukomplementaatio tai kilpailu, jossa vain halutun toiminnan omaavat solut selviävät.
- Seulonta — korkean läpimenon aktivaatiokokeet, fluoresenssipohjaiset mittaukset (FACS) tai värjäys, missä yksittäiset variantit mitataan erikseen.
- Kompartimentoiminen — emulsiot, mikropisarat tai kuplat sitovat DNA:n, proteiinin ja funktion samaan tilaan, jolloin voidaan valita parhaita pareja.
- Display-menetelmät — esimerkiksi fagi-, ribo- tai mRNA-display, joissa proteiini ja sen koodi säilyvät samassa kompleksissa.
In vivo vs. in vitro — edut ja rajoitukset
- In vivo: etuna biologinen konteksti (oikeat laskostumis- ja modifikaatio-olosuhteet), helppo laajamittainen tuotanto ja sovellettavuus eläviin järjestelmiin. Rajoitteena on transformaation ja kasvun aiheuttamat pullonkaulat sekä toksisuuteen liittyvät ongelmat.
- In vitro: mahdollista tehdä valtavia kirjastoja ja käyttää olosuhteita, jotka olisivat myrkyllisiä eläville soluille. Rajoitteena on usein monimutkaisten, solujen tarvitsemien modifikaatioiden puuttuminen sekä kalliimpi kuluerä ja tekninen vaatimus translatorio- ja ilmentämisjärjestelmille.
Sovellukset
Suunnattua evoluutiota käytetään laajasti:
- Teollisuusentsyymien optimointi (lämmönkestävyys, liuotteenkesto, toiminta eri pH-alueilla),
- Lääkekehitys (parannetut terapeuttiset proteiinit, pienemmät immunogeenisuudet),
- Biokatalyysi ja synteettinen biologia (uudet reaktiopolut ja katalyytit),
- Biosensorit ja diagnostiset proteiinit (sitoutumisherkkyyden parantaminen).
Esimerkkinä suunnatun evoluution merkittävästä vaikutuksesta: Frances H. Arnold sai Nobel-palkinnon 2018 työnsä ansiosta, joka kehitti tehokkaita menetelmiä entsyymien suunnattuun evoluutioon.
Valintastrategioiden hienosäätö
Menestyksen kannalta ratkaisevaa on valintapaineen (stringency) asettaminen: liian lievä valinta ei edistä parannuksia, liian kova valinta voi hävittää lupaavat, mutta vielä keskinkertaiset variantit. Tyypillisesti valinta kiristetään kierros kierrokselta.
Rajoitukset ja haasteet
- Riittävän laajan ja monipuolisen kirjaston luominen voi olla teknisesti haastavaa.
- Hitaat seulontamenetelmät muodostavat pullonkaulan; siksi korkean läpimenon (high-throughput) menetelmät ovat keskeisiä.
- Jotkut ominaisuudet, kuten monimutkaiset posttranslaationaaliset modifikaatiot, voivat olla vaikeita saavuttaa in vitro tai prokaryoottisoluissa.
Turvallisuus ja eettisyys
Suunnattu evoluutio käsittelee biologista materiaalia, joten tutkimuksessa on noudatettava biosafety- ja biosecurity-ohjeita sekä paikallista lainsäädäntöä. On tärkeää arvioida mahdolliset ympäristö- ja terveysriskit sekä huomioida eettiset näkökohdat, kuten dual-use -riski (menetelmien mahdollinen väärinkäyttö).
Yhteenveto
Suunnattu evoluutio on tehokas ja käytännöllinen tapa parantaa proteiinien ja entsyymien ominaisuuksia ilman täydellistä rakenteellista tietoa. Menestyksen avaimia ovat hyvä kirjastosuunnittelu, toimiva genotyypin–fenotyypin linkitys ja sopivien valinta- tai seulontatekniikoiden käyttö. Kun nämä elementit yhdistetään iteratiivisiin kokeisiin, voidaan saavuttaa merkittäviä parannuksia katalyyttiseen tehokkuuteen, stabiilisuuteen, spesifisyyteen ja muihin haluttuihin ominaisuuksiin.