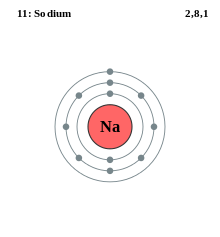
Elektronikuori on atomin ulkoinen osa atomiytimen ympärillä. Se on paikka, jossa elektronit ovat todennäköisimmin löydettävissä, ja sen voi ymmärtää kokoelmana atomiorbitaaleja, joilla on sama pääkvanttiluvun n arvo. Pääkvanttiluku n on positiivinen kokonaisluku (n = 1, 2, 3 …) ja se määrää kuoressa olevan energian ja tyypillisen etäisyyden ydintä kohti.
Kuorten ja alikuorten rakenne
Jokaisella elektronikuorella voi olla yksi tai useampia elektronin alikuoria eli alitasoja. Alitasot erotellaan kulmamomentin kvanttiluvun l perusteella (l = 0, 1, 2, 3…), ja niille annetaan yleisesti nimet s, p, d, f vastaavasti. Kullakin alitasolla on tietty määrä orbitaaleja, joilla on sama l, ja jokaisella orbitaalilla on tilaa korkeintaan kahdelle elektronille erilaisten spin-arvojen vuoksi.
Yhden kuoressa olevien elektronien maksimilukumäärä on yhtä suuri kuin 2 n 2 {\displaystyle 2n^{2}} 
- Alikuorien nimitykset ja vastaavat l-arvot: s (l = 0), p (l = 1), d (l = 2), f (l = 3).
- Orbitaaleja kussakin kuoressa on yhteensä n2 kpl, ja jokaisella orbitaalilla voi olla kaksi elektronia.
- Alikuoren elektronien maksimimäärä voidaan laskea kaavalla 2(2l+1) (esim. p-alikuorella l = 1 → 2·(2·1+1)=6 elektronia).
Täyttymisjärjestys ja kemiallinen merkitys
Kun elektronit sijoittuvat atomiin, ne täyttävät ensin alhaisimman energian omaavat orbitaalit (Aufbau-periaate). Käytännössä täyttymisjärjestys noudattaa likimääräisesti sarjaa 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p …, mutta poikkeuksiakin on (esim. kromi ja kupari atomien elektronikonfiguraatioissa esiintyy pieniä poikkeuksia stabiilien puolitäytettyjen ja täyttyneiden d-alikourien takia).
Ulkokuoren eli uloimman pääkvanttiluvun elektroneilla (valenssielektronit) on suuri merkitys alkuaineen kemiallisissa ominaisuuksissa ja sidoksentekokäyttäytymisessä. Atomit pyrkivät usein saavuttamaan vakaamman elektronirakenteen, esimerkiksi jalokaasujen vastaavan täyttymyksen, jolloin syntyy ioneja tai kovalenttisia sidoksia.
Bohrin malli ja kvanttimekaaninen tarkennus
Elektronikuorien nimi juontuu Bohrin mallista, jossa elektroniryhmien uskottiin kiertävän ydintä tietyin etäisyyksin siten, että niiden radat muodostivat "kuoria". Tanskalainen tiedemies Niels Henrik David Bohr esitti ajatuksen, ja se selitti osan atomien spektriviivoista.
Kuitenkin nykyaikainen atomimalli perustuu kvanttimekaniikkaan: elektronit eivät kierrä pitkin määrättyjä klassisia ratoja, vaan ne kuvataan aaltofunktioilla (orbitaaleilla), jotka antavat todennäköisyysjakauman siitä, missä elektronin löytäminen on todennäköisintä. Bohrin malli on siksi yksinkertaistus, joka toimii hyvin yksielektronisissa järjestelmissä (kuten vety), mutta se ei anna täsmällistä kuvaa monielektronisista atomeista.
Lisätietoa kvanttiluvuista ja periaatteista
Atomitilannetta kuvaavat pääkvanttiluvun n ja kulmamomentin kvanttiluvun l lisäksi magneettinen kvanttiluku ml (orbitaalin suuntausavaruudessa) ja spin-kvanttiluku ms (elektronin spinin suunta). Elektronit noudattavat Pauli-kieltosääntöä (kaksi elektronia ei voi jakaa samoja neljää kvanttilukua), ja Hundin sääntö määrää, miten elektronit jakautuvat samantasoisille orbitaaleille maksimoiden samansuuntaisen spinin ennen parittumista.
Yhteenvetona: elektronikuori on kvanttiluvun n mukainen elektronien energiatila-attribuutti, joka koostuu alikuorista ja orbitaaleista. Kuorien rakenne ja elektronien jakautuminen määräävät atomien kemialliset ominaisuudet, ja käsitettä on kehitetty Bohrin yksinkertaisesta mallista nykyiseen kvanttimekaaniseen kuvaukseen.