Fysiikan kvanttimekaniikassa Bohrin malli on Niels Bohrin ehdottama atomimalli. Bohrin malli on käyttökelpoinen vain keskusteltaessa vetyatomin käyttäytymisestä. Bohrin malli on erittäin käyttökelpoinen kuvaamaan vedyn emissiospektriä.
Bohrin mallin perusperiaatteet
- Elektroni liikkuu ytimenvaaran ympäri pyörivällä radalla, ja tietyt radat ovat stabiileja (niillä elektronit eivät säteile energiaa jatkuvasti).
- Orbitin liikemäärämomentti on kvantittunut: L = nħ, jossa n = 1, 2, 3, ... on pääkvanttiluku ja ħ = h/2π.
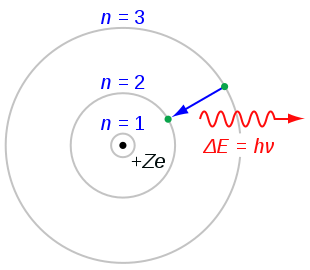
- Kun elektroni hyppää korkeammalta energiatasolta alemmalle, sen vapauttama fotonin energia määräytyy energiatason erotuksena: hν = Ei − Ef.
- Energiatasot vedyn tapauksessa saadaan kaavalla En = −13,6 eV / n^2, missä n on positiivinen kokonaisluku. Tämän seurauksena atomi voi emittoida tai absorboida vain tiettyjä, diskreettejä aallonpituuksia.
Tärkeimmät laskukaavat ja suureet
- Bohrin säde (pääorbitin säde, n = 1): a0 ≈ 5,29·10−11 m.
- Energiatasot: En = −13,6 eV / n^2.
- Fotonin aallonpituus laskee energian erotuksena Rydbergin kaavalla: 1/λ = R (1/nf^2 − 1/ni^2), jossa R ≈ 1,097·107 m−1.
Emissio- ja absorptiosarjat
Bohrin malli selittää vedyn spektriviivat ja niiden ryhmittymisen sarjoiksi:
- Lymanin sarja (nf = 1): UV-alueella
- Balmerin sarja (nf = 2): näkyvän valon alueella — kuuluisa Balmerin viiva Hα
- Paschenin, Brackettin ja muut sarjat: infrapuna-alueella (nf = 3, 4, ...)
Menestys ja rajoitukset
- Bohrin malli onnistuu erittäin hyvin ennustamaan vedyn (ja muissa yksielektronisissa, ns. vetyisiä ionien kuten He+, Li2+ -) spektriviivoja ja ionisaatioenergiaa.
- Malli antaa yksinkertaiset, helposti ymmärrettävät kaavat energia‑ ja sädearvoille sekä selittää diskreetit säteilyaallonpituudet.
- Rajoituksia: malli ei kuvaa monielektronisia alkuaineita, ei ota huomioon elektronien spin'iä eikä relativistisia tai hienorakenteellisia (fine structure) ilmiöitä. Myöskään Zeeman‑ ja Stark‑vaikutuksia tai siirtymien intensiteetteihin liittyviä valintasääntöjä (esim. Δl = ±1), jotka selittyvät täydellisemmin kvanttimekaniikan aaltotoimilla ja kvanttiluvuilla, se ei käsittele oikein.
- Bohrin malli oli tärkeä historiallinen askel, mutta se on sittemmin korvautunut Schrödingerin aaltofunktion ja koko nykyaikaisen kvanttimekaniikan kuvauksella, jossa elektronit eivät pyöri määriteltyinä radanaan vaan muodostavat orbitalleja.
Yhteenvetona, Bohrin malli on yksinkertainen ja havainnollinen kuvaus vedyn kvantittuneista tiloista ja emissiospektristä. Se tarjoaa edelleen opettavan ja laskennallisesti helpon lähestymistavan, vaikka nykyaikainen teoria antaa tarkemman ja yleispätevämmän kuvauksen atomien rakenteesta.