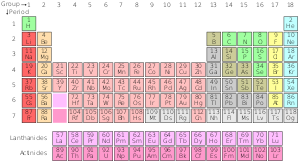
Kemiallisten alkuaineiden jaksollinen järjestelmä on luettelo tunnetuista kemiallisista alkuaineista. Taulukossa alkuaineet on sijoitettu järjestykseen niiden järjestyslukujen mukaan alkaen pienimmästä luvusta yksi, vedystä. Alkuaineen järjestysluku on sama kuin protonien lukumäärä kyseisessä atomin ytimessä. Jaksollisessa järjestelmässä alkuaineet on järjestetty jaksoihin ja ryhmiin. Taulukon alkuaineita sisältävää riviä kutsutaan jaksoksi. Kullakin jaksolla on numero, joka on 1-8. Jaksossa 1 on vain kaksi alkuainetta: vety ja helium. Jaksossa 2 ja 3 on molemmissa 8 alkuaineita. Muut jaksot ovat pidempiä. Jakson alkuaineilla on peräkkäiset järjestysluvut.
Jaksojen pituudet ja elektronikuoret
Jaksojen pituudet määräytyvät elektronikuorien ja -orbitaleiden täyttymisen mukaan. Perussääntö on, että alkuaineet siirtyvät järjestyksessä elektronien täyttäessä s-, p-, d- ja f-orbitaleja. Jaksojen tyypilliset pituudet ovat:
- Jakso 1: 2 alkuaineetta (s-shell täyttyy: 1s2).
- Jaksot 2 ja 3: kummassakin 8 alkuaineetta (s- ja p-orbitaalit: 2s2 2p6 jne.).
- Jaksot 4 ja 5: kummassakin 18 alkuaineetta (s-, p- ja d-orbitaalit osin mukana).
- Jaksot 6 ja 7: tavallisesti 32 paikkaa, koska f-orbitaalit (lantanoidit ja aktinoidit) liittyvät näihin jaksoihin; käytännössä jakso 7 sisältää myös monia synteettisiä, lyhytikäisiä alkuaineita.
Ryhmä, valenssielektronit ja kemialliset ominaisuudet
Taulukossa olevaa alkuaineiden saraketta kutsutaan ryhmäksi. Tavallisessa jaksollisessa järjestelmässä on 18 ryhmää. Jokaisella ryhmällä on numero: 1-18. Ryhmään kuuluvien alkuaineiden elektronit ovat järjestäytyneet samalla tavalla valenssielektronien lukumäärän mukaan, mikä antaa niille samanlaiset kemialliset ominaisuudet (ne käyttäytyvät samalla tavalla). Esimerkiksi ryhmä 18 tunnetaan jalokaasuina, koska ne ovat kaikki kaasuja eivätkä yhdisty muiden atomien kanssa.
Valenssielektronit eli uloimmat elektronit määräävät, miten atomi reagoi kemiallisesti: s- ja p-lohkojen alkuaineilla valenssi on yleensä selkeä (esim. alkalimetallit ryhmässä 1: yksi valenssielektroni), kun taas siirtymämetalleilla (d-lohko) ja f-lohkon alkuaineilla esiintyy moninaisempia hapetusasteita.
Jaksollisen järjestelmän lohkot
Jaksollinen järjestelmä jaetaan usein lohkoihin elektroniorbitaalien perusteella:
- s-lohko: ryhmät 1–2 ja helium. Alkali- ja maa-alkalimetallit.
- p-lohko: ryhmät 13–18. Sisältää epämetallit, metalloidit ja osan metalleista.
- d-lohko: ryhmät 3–12; nämä ovat siirtymämetalleja, joilla on tyypillisesti monia hapetusasteita ja metallisia ominaisuuksia.
- f-lohko: lantanoidit ja aktinoidit, jotka usein sijoitetaan taulukon alle erikseen niiden samanlaisten kemiallisten ominaisuuksien vuoksi.
Kemialliset luokat ja trendit
Kemistit ovat käyttäneet jaksollista järjestelmää havaitakseen alkuaineiden välisiä malleja ja suhteita. Jaksollisessa järjestelmässä on kolme pääryhmää: metallit, metalloidit ja epämetallit. Esimerkiksi taulukon alareunassa ja äärimmäisenä vasemmalla olevat alkuaineet ovat kaikkein metallisimpia ja oikealla ylhäällä olevat alkuaineet ovat vähiten metallisia. (Esimerkiksi cesium on paljon metallisempi kuin helium).
Yleisimmät jaksolliset trendit, joita kemistit seuraavat, ovat:
- Atomisäde: kasvaa siirryttäessä ylhäältä alas samassa ryhmässä ja pienenee vasemmalta oikealle samassa jaksossa.
- Ionisaatioenergia: eli energiamäärä, joka tarvitaan elektronin poistamiseen; tyypillisesti kasvaa vasemmalta oikealle ja pienenee ylhäältä alas.
- Elektronegatiivisuus: atomin kyky vetää sidoselektroneja puoleensa; yleensä kasvaa vasemmalta oikealle ja pienenee ylhäältä alas.
- Hapetusasteet ja kemiallinen monimuotoisuus: siirtymämetalleilla ja f-lohkon alkuaineilla voi olla useita vakaita hapetusasteita, mikä tekee niistä kemiallisesti monipuolisia.
Erityistapaukset ja käytännön huomioita
- Vety: usein sijoitettu jakson alkuun, mutta sen kemialliset ominaisuudet eivät täysin sovi yhteen minkään yhden ryhmän kanssa — se voi käyttäytyä sekä metalleille että epämetalleille tyypillisellä tavalla.
- Helium:
- Lantanoidit ja aktinoidit: f-lohkon alkuaineet ovat usein sijoitettu taulukon alle; aktinoideista osa on luonnossa radioaktiivisia ja monet ovat synteettisiä.
- Synteettiset alkuaineet: järjestysluvun kasvaessa monet alkuaineet ovat lyhytikäisiä, radioaktiivisia ja valmistettu laboratoriossa (transuraanit, eli uraniumin jälkeen).
Historia ja tieteellinen merkitys
Jaksollisen järjestelmän keksi venäläinen kemisti Dmitri Ivanovitš Mendelejev (1834-1907). Hänen tunnetuin panoksensa oli järjestelmän laatiminen siten, että se korosti toistuvia kemiallisia ominaisuuksia ja jätti tarkoituksella aukkoja tuntemattomille alkuaineille — hän myös ennusti niiden ominaisuuksia ja löysi useimmiten oikeita arvoja myöhemmin löydetyille alkuaineille. Hänen kunniakseen alkuaine 101 nimettiin hänen mukaansa mendelejiksi.
Vuonna 1990 Kansainvälinen puhtaan ja soveltavan kemian liitto (IUPAC) päätti käyttää uutta arabialaisia numeroita sisältävää ryhmänumerointia 1–18 korvaamaan aiemmat roomalaisiin numeroihin perustuvat järjestelmät. Roomalaisia numeroita käytettiin aiemmin laajalti, mutta nykyään IUPACin 1–18-numerointi on standardi.
Miksi jaksollinen järjestelmä on tärkeä?
Jaksollinen järjestelmä tarjoaa kemisteille ja muille tieteilijöille tehokkaan työkalun alkuaineiden ominaisuuksien ennustamiseen, reaktioiden ymmärtämiseen ja materiaalien suunnitteluun. Se yhdistää atomien rakenteen (protonit, neutronit, elektronit) ja makroskooppiset kemialliset käyttäytymismallit systemaattiseksi kokonaisuudeksi, jota voidaan laajentaa uusilla löydöillä ja synteesillä.