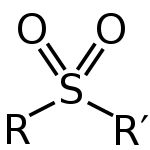
Sulfoni on molekyyli, jossa rikkiatomi on sitoutunut kahteen happiatomiin muodostaen S(=O)2‑rakenteen. Rikki muodostaa kaksi kaksoissidosta kahteen happiatomiin ja lisäksi kaksi yksinkertaista sidosta kahteen muuhun substituenttiin (yleensä orgaaniseen R‑ryhmään), joten yleinen rakenne voidaan kirjoittaa R–S(=O)2–R'. Rikki on tässä oksidaatiotilassa +6, mikä vaikuttaa yhdisteen polariteettiin ja fysikaalisiin ominaisuuksiin.
Rakenne ja ominaisuudet
Sulfoneilla (suom. sulfonit tai sulfonit, usein käytetään myös termiä sulfoni) on tyypillisesti korkea kiehumispiste ja suuri permittiivisyys verrattuna vastaaviin eetteri- tai hydrokarboniyhdisteisiin, koska S=O‑sidokset tekevät molekyylistä polaarisen. Monet yksinkertaiset sulfonit, kuten dimetyylisulfoni (tunnetaan myös nimellä MSM, methylsulfonylmethane), ovat kiinteitä tai korkean kiehumispisteen nesteitä ja liukenevat hyvin polaarisiin liuottimiin.
Valmistus
Yleisin synteesireitti on hapettamalla tioeettereitä (sulfidejä). Hapetus voidaan suorittaa esimerkiksi perhapoilla (mCPBA), vetyperoksidilla (H2O2) tai muilla hapettimilla siten, että ensin muodostuu sulfoxidi ja jatkohapetuksella saavuttaa sulfoni. Vaihtoehtoisia reittejä ovat sulfonyyli‑yhdisteiden käyttö, sulfonylkloridien reaktiot ja erilaiset katalyyttiset hapetusmenetelmät riippuen lähtöaineista ja halutuista substituenteista.
Kemiallinen käyttäytyminen
Sulfoneja pidetään yleisesti kemiallisesti melko stabiileina. Niissä alfa‑aseman vedyt (eli hiiliatomit, jotka ovat suoraan S‑atomia sitovien hiilien vieressä) ovat kuitenkin suhteellisen happamia ja ne voidaan deprotonoida voimakkailla emäksillä, jolloin muodostuu stabiloitu karbanioni. Tällaisia reaktiivisia väliainetta hyödynnetään orgaanisessa synteesissä (esim. Julia‑olefinaatiossa). Eräitä sulfoneihin liittyviä reaktioita ovat mm. Ramberg–Bäcklund‑muunnos (jossa halogenoitu alfahalo‑sulfoni muuntuu alkeeniksi) ja erilaiset alkylointi‑ ja kondensaatioreaktiot.
Käytöt
Niitä käytetään monissa tärkeissä kemiallisissa reaktioissa ja sovelluksissa. Esimerkiksi Julia‑olefinaatiossa sulfonin avulla aldehydistä saadaan alkeeni — tässä sulfonin alfahiili deprotonoituna toimii nukleofiilina ja mahdollistaa alkeenin muodostuksen.
Sulfoneja käytetään myös teollisina liuottimina (esim. sulfolane on tunnettu korkean kiehumispisteen, polaarinen liuotin petrokemian prosesseissa). Lisäksi sulfoneja löytyy lääkeaineista (esim. antibiootti dapsone kuuluu sulfonien ryhmään), sekä korkeasuorituskykyisissä polymeereissä kuten polysulfoneissa, joita käytetään teknisissä muoveissa ja suodattimissa. Myös kosmetiikassa ja ravintolisissä tavataan yksinkertaisia sulfoneja kuten MSM.
Turvallisuus ja ympäristö
Sulfonejen toksisuus vaihtelee yhdisteittäin. Monet alifatiset sulfones ovat suhteellisen vähän reaktiivisia ja niillä on matala akuutti myrkyllisyys, mutta kyseessä olevien yhdisteiden turvallisuusprofiili pitää aina tarkistaa erikseen. Joidenkin sulfonien, kuten dapsone, käytössä voi esiintyä haittavaikutuksia, ja sulfolanen tavoin tietyt sulfonejohdannaiset ovat olleet ympäristön saastuttajia poraustoiminnan ja teollisuuden yhteydessä. Käsittelyssä noudatetaan tavanomaisia kemikaaliturvallisuusohjeita: asianmukaiset suojavälineet, hyvä ilmanvaihto ja jätehuolto.
Yhteenvetona: sulfoni on orgaaninen rikki‑ ja happiyhdiste, jonka S(=O)2‑rakenne antaa sille erityisiä fysikaalisia ja kemiallisia ominaisuuksia. Sulfonit ovat hyödyllisiä synteesivälineitä ja teollisia yhdisteitä lääke‑, muovi‑ ja liuotinsovelluksissa.