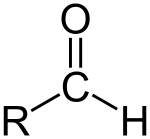
Aldehydi (/ˈældɪhaɪd/) on orgaaninen yhdiste, joka sisältää niin kutsutun formyyliryhmän. Formyyliryhmän yleinen rakenne on R-CHO, missä hiili on osa karbonyyli-ryhmää (C=O) ja on lisäksi sitoutunut vetyyn (–H) ja orgaaniseen sivuketjuun (R). Ryhmää, jossa ei ole sivuketjua, kutsutaan usein yksinkertaisesti aldehydiryhmäksi tai formyyliryhmäksi. Aldehydit poikkeavat ketoneista siten, että formyyliryhmä sijaitsee aldehydissä aina molekyylin päässä, kun taas ketonissa karbonyylihiili on molekyylin keskellä. Aldehydit ovat yleisiä orgaanisessa kemiassa ja niitä esiintyy laajasti luonnossa ja teollisuudessa; monet hajusteet ja aromaattiset yhdisteet kuuluvat aldehydien ryhmään.
Rakenne ja nimistö
Aldehydin tunnusomainen osa on karbonyylihiili (C=O), joka on sidottu myös vetyyn. Yleisformaali voidaan kirjoittaa R–C(=O)–H tai yksinkertaisesti R–CHO. Yleisiä esimerkkejä ovat:
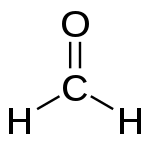
- Formaldehydi (IUPAC: methanal, CH2O) – yksinkertaisin aldehydi.
- Etanal (usein: asetaldehydi, CH3CHO).
- Bentseeni-aldehydi (bensaldehydi, C6H5CHO).
Nimityksissä IUPAC-käytäntö lisää pääryhmän nimen “-al” loppuun (esim. metanal, etanal). Yleisnimityksiä, kuten asetaldehydi ja formaldehydi, käytetään edelleen laajasti.
Fysikaaliset ominaisuudet
- Aldehydit ovat yleensä polaarisia, koska karbonyyli on dipolimolekyyli; tämä vaikuttaa niiden liukoisuuteen ja keittopisteisiin.
- Pienimolekyyliset aldehydit (esim. methanal, ethanal) ovat vesiliukoisia; pidemmät alifaattiset aldehydit ovat vähemmän liukoisia ja nesteitä tai kiinteitä aineita.
- Aldehydit yleensä haihtuvat helpommin kuin vastaavat alkoholijohdannaiset, mutta niiden keittopisteet ovat usein korkeammat kuin vastaavien hiilivetyjen johtuen dipolidipoli-interaktioista.
Kemiallinen reaktiivisuus
Aldehydit ovat yleensä reaktiivisempia kuin ketonit, koska karbonyylihiilen sähköinen tilanne tekee siitä helpommin elektrofiilisen. Tärkeimpiä reaktioita:
- Nukleofiilinen additio – karbonyylihiileen liittyy nukleofiili; tästä syntyy hemi-asetaaleja, asetaaleja, alkoholeja ym. Esimerkiksi hydraus (reduktio) tuottaa primäärisen alkoholin.
- Imiinien ja Schiffin emästen muodostus – aldehydit reagoivat primääristen aminoryhmien kanssa muodostaen imiinia (Schiffin emäs), mikä on tärkeää biokemiallisissa ja synteettisissä reaktioissa.
- Aldolikonensaation reaktiot – alifaattiset aldehydit, joilla on α-vetyjä, voivat muodostaa kondensaatiotuotteita (aldolireaktiot), joita hyödynnetään C–C-sidosten rakentamisessa.
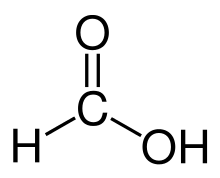
- Oxidaatio – aldehydit hapettuvat helposti karboksyylihapoiksi (R–COOH). Tämä tekee aldehydeistä tärkeän välituotteen monissa oksidatiivisissa muunnoksissa.
- Cannizzaro-reaktio – kun aldehydillä ei ole α-vetyä (esim. bentseeni‑aldehydi) ja reaktio tapahtuu vahvassa emäksessä, tapahtuu disproportioituminen: toinen molekyyli hapettuu happoksi ja toinen pelkistyy alkoholiksi.
- Wittig-reaktio – aldehydit reagoivat fosforiylideihin muodostaen alkeeneja; tämä on keskeinen menetelmä C=C‑sidosten muodostamisessa.
Valmistusmenetelmät
- Primäärisen alkoholin hapetus – tyypillinen laboratorio- ja teollisuusmenetelmä: primaarinen alkoholi hapetetaan kontrolloidusti aldehydiksi (välttää ylihapetusta happoon).
- Hydroformylaatio (oxo-prosessi) – teollinen menetelmä, jossa alkeeneista lisätään vetyä ja hiilimonoksidia muodostaen aldehydejä.
- Oksidatiivinen monomerin hajoitus tai sideketjujen katkaisu – tietyt reaktiot voivat tuottaa aldehydejä alkeeni- tai muista lähteistä.
- Dehydraus ja muut synteettiset menetelmät – useita orgaanisen synteesin reittejä voidaan käyttää erityyppisten aldehydien tuottamiseen.
Käyttö ja merkitys
Aldehydeillä on laaja teollinen ja kemiallinen käyttö:
- Formaldehydi on laajalti käytetty lähtöaine hartsien (urea‑formaldehydi, fenoli‑formaldehydi), liimojen ja desinfiointiaineiden valmistuksessa.
- Asetaldehydi on tärkeä välituote etikkahapon, asetaldehydiperoksideihin perustuvien synteesien ja muunnosten tuotannossa.
- Bentsaldehydi ja muut aromaattiset aldehydit ovat tärkeitä hajuste- ja makuyhdisteiden sekä lääkkeiden ja väriaineiden synteesissä.
- Orgaanisessa synteesissä aldehydejä käytetään laajalti C–C- ja C–N‑sidosten muodostamiseen sekä muiden funktionaalisten ryhmien esiasteina.
Turvallisuus ja ympäristö
Monet aldehydit ovat ärsyttäviä ja myrkyllisiä: esimerkiksi formaldehydi on tunnettu ärsyttäjä ja luokiteltu mahdolliseksi karsinogeeniksi. Aldehydit voivat olla helposti hapettuvia ja joissain tapauksissa herkkiä polymeroitumaan tai muodostamaan kondensaatiotuotteita, joten niiden varastointi usein vaatii stabilointia (esim. vesiliuoksina tai additiivien kanssa) ja asianmukaista käsittelyä. Työpaikoilla on noudatettava turvallisuusohjeita, kuten hyvä ilmanvaihto, suojakäsineet ja -lasit sekä asianmukainen jätteiden käsittely.
Yhteenvetona: aldehydit ovat monipuolinen ja reaktiivinen yhdisteiden ryhmä, jolla on suuri merkitys niin luonnollisissa prosesseissa kuin teollisessa kemian tuotannossa — mutta niiden reaktiivisuuden vuoksi myös asianmukainen käsittely ja turvallisuus ovat tärkeitä.