Sykloaditio on kemiallinen reaktio, jossa kahden tai useamman tyydyttymättömän reagoijan kaksois- tai kolmoissidoksia “kulutetaan” ja ne korvautuvat uudella rengasrakenteella. Se on perisyklinen kemiallinen reaktio, joka etenee yleensä yhdessä, samanaikaisessa siirtymätilassa: tyypillisesti kaksi tai useampia tyydyttymättömiä molekyylejä (tai saman molekyylin osia) yhdistyy muodostaen syklisen adduktin, ja sidosten kokonaislukumäärä “yksinkertaistuu” nettomääräisesti. Kyseessä on siis syklisoitumisreaktio, jossa syntyy uusi rengas atomeista ilman välivälituotteita.
Sykloadditiot nimetään yhdistyvien molekyylien π-komponenttien atomimäärän mukaan hakasuljenotaatiolla [i + j]. Tällöin Diels-Alder-reaktio on [4 + 2] -sykloadditio ja 1,3-dipolaarinen sykloadditio [3 + 2] -sykloadditio. Tämäntyyppinen reaktio on luonteeltaan pooliton additioreaktio.
Mekanismi ja orbitaalisäännöt
Sykloadditiot ovat tavallisesti yhdessä (concerted) eteneviä: sidokset katkeavat ja muodostuvat samanaikaisesti syklisessä elektroninsiirtosilmukassa. Reaktion kulku selittyy kahdella toisiaan täydentävällä tavalla:
- Orbitaalien symmetria (Woodward–Hoffmannin säännöt): Lämpöolosuhteissa sallitut sykloadditiot etenevät niin, että orbitaalit kohtaavat symmetriaa säilyttäen. Esimerkiksi [4 + 2] on lämpöisesti sallittu (suprafasiaalinen–suprafasiaalinen), kun taas yksinkertainen [2 + 2] on lämpöisesti kielletty mutta valokemiallisesti sallittu.
- Rajamolekyyliorbitaalit (FMO): Reaktionopeus määräytyy pääasiassa reagoijien HOMO–LUMO-yhteensopivuudesta. Normaalissa elektronikysynnässä dieni on elektronirikas (esim. -OR, -alkyyli) ja dienofiili elektroniköyhä (esim. -CN, -COR, -COOR). Käänteisessä elektronikysynnässä roolit vaihtuvat.
Diels–Alder ([4 + 2])
- Perusreaktio: 1,3-butadieeni + alkeeni (esim. eteeni) → sykloheks-1-eeni. Reaktio on stereospesifinen: dienofiilin cis-/trans-geometria säilyy rengastuotteessa.
- Endo-/exo-valikoivuus: Elektronia vetäviä π-ryhmiä sisältävien dienofiilien kanssa endo-tuote on usein kinetisesti suosittu (endo-sääntö), koska toissijaiset orbitaali-interaktiot stabiloivat siirtymätilaa.
- Regioselektiivisyys: Epäsymmetristen reaktanttien kanssa substituenttien ohjaus johtaa ennustettavaan orto-/para-analogiaan; FMO-analyysi auttaa tuotteiden suhteiden ennustuksessa.
- Hetero-Diels–Alder: Kun toinen komponentti sisältää heteroatomin (esim. C=O, C=N), saadaan heterosyklisiä renkaita, kuten dihydropyraneja tai dihydropyridiinejä.
- Intramolekulaarinen DA: Sama molekyyli sisältää sekä dienin että dienofiilin; muodostuu tiiviitä, usein polytsyklisten luonnonaineiden runkoja.
- Käänteisreaktio (retro-DA): Lämmittäminen voi pilkkoa renkaan takaisin lähtökomponentteihin; tätä hyödynnetään suojaryhmästrategioissa ja aromaattisten fragmenttien vapautuksessa.
- Katalyysi ja olosuhteet: Lewis-hapot (esim. BF3, AlCl3, TiCl4) aktivoivat dienofiilin ja kiihdyttävät reaktiota sekä parantavat selektiivisyyttä. Korkea paine (negatiivinen aktivaatiotilavuus) ja kohtalainen lämpö nopeuttavat; liuottimen polarisoituvuus voi lisätä nopeutta.
1,3-dipolaariset sykloadditiot ([3 + 2])
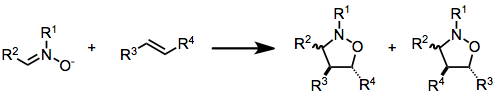
- Tyypilliset 1,3-dipolit: Orgaaniset atsidit (N3−), nitronit, nitrilioksidit ja atsometiiniylidit.
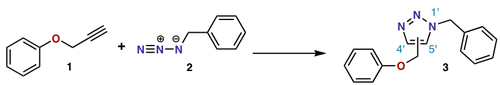
- Tuotteet: Viisijäseniset heterosyklit, kuten 1,2,3-triatsolit, isoksatsolidit ja pyrrolidiinijohdannaiset.
- “Click”-kemia: Kupari(I)-katalysoitu atsidi–alkyyni-sykloadditio (CuAAC) tuottaa selektiivisesti 1,4-disubstituoituja 1,2,3-triatsoleja; reaktio on nopea, siedettää vettä ja monia funktionaaliryhmiä ja on bioortogonaalinen.
- Stereokemia ja regio-ohjaus: Substituenttivaikutukset ja mahdollinen metallikatalyysi ohjaavat regioselektiivisyyttä; asymmetriset katalyytit mahdollistavat korkean enantioselektiivisyyden.
Muita sykloadditioita ja erityistapauksia
- [2 + 2] -sykloadditiot: Kaksi alkeenia muodostaa syklobutaanin tyypillisesti valokemiallisesti. Karbonyylin ja alkeenin [2 + 2] tuottaa oksetaneja (klassinen valokemiallinen Paternò–Büchi-tyyppinen lisäys).
- [4 + 3] ja [5 + 2]: Antavat seitsemän- ja seitsenjäsenisiä renkaita esimerkiksi oksiallyylivälitteisesti ([4 + 3]) tai koordinaatiokatalyysillä ([5 + 2]).
- Keletrooppiset lisäykset: Kaksi uutta sidosta muodostuu samaan atomiin (esim. SO2:n additio; käänteisesti SO2:n eliminoituminen retro-DA-tyyppisesti).
Selektiivisyys ja suunnittelu
- Stereospesifisyys: Reagoijien cis/trans- ja E/Z-geometria heijastuu suoraan tuotteeseen; uusia kiraalikeskuksia muodostuu määritellysti.
- Regioselektiivisyys: Ennustettavissa FMO-analyysillä ja substituenttien ohjausvaikutuksilla; usein voidaan kääntää lisäämällä aktivoivia/poistavia ryhmiä tai vaihtamalla katalyyttiä.
- Asymmetrinen induktio: Kiraaliset Lewis-happokatalyytit ja orgaaniset katalyytit mahdollistavat korkean enantioselektiivisyyden.
Käytännön vinkkejä ja olosuhteiden optimointi
- Lämpötila: Kohtalainen kuumennus (esim. 25–120 °C) nopeuttaa ilman sivureaktioita; liian korkea lämpö voi suosia retro-reaktiota.
- Paine: Korkea paine (kymmenistä satoihin MPa) voi merkittävästi nopeuttaa ja parantaa saantoa erityisesti Diels–Alderissa.
- Liuotin: Polaariset, heikosti nukleofiiliset liuottimet (esim. dikloorimetaani, nitrometaani) ovat usein hyviä; vesi voi nopeuttaa joitakin Diels–Alder-reaktioita hydrofobisen vaikutuksen kautta.
- Suunnittelu: Dienten on oltava s-cis-konformaatiossa; steriset esteet ja konjugaatio vaikuttavat voimakkaasti reaktionopeuteen.
Sovellukset
- Luonnonaine- ja lääkesynteesi: Nopea renkaiden rakentaminen ja useiden kiraalikeskusten luonti yhdessä vaiheessa.
- Materiaalikemia: Verkottuminen, itsekorjautuvat materiaalit (esim. lämpöreversiibelit retro-DA-sidokset), valokemialliset kuvioinnit.
- Kemiallinen biologia: Bioortogonaaliset merkinnät (esim. triatsolien muodostus), proteiinien ja biomolekyylien hellävarainen konjugointi.
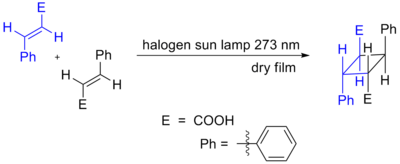
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)