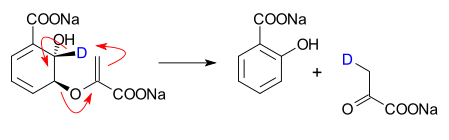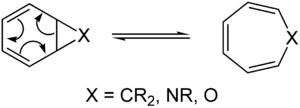
Orgaanisessa kemiassa perisyklinen reaktio on eräänlainen orgaanisten yhdisteiden välinen kemiallinen reaktio. Perisyklisissä reaktioissa molekyylin siirtymätila on rengas (jolla on syklinen geometria), ja reaktio etenee koordinoidusti. Perisykliset reaktiot ovat yleensä uudelleenjärjestelyreaktioita. Tärkeimmät perisyklisten reaktioiden ryhmät ovat:
- Sähkösykliset reaktiot
- Sykloadditiot
- Sigmatrooppiset reaktiot
- Ryhmänsiirtoreaktiot
- Keletrooppiset reaktiot
- Dyotrooppiset reaktiot
Yleensä perisykliset reaktiot ovat tasapainoprosesseja. Reaktiota on kuitenkin mahdollista työntää johonkin suuntaan, jos tuote on huomattavasti alemmalla energiatasolla. Tämä on Le Chatelierin periaatteen soveltamista reaktioon, jossa on mukana yksi molekyyli.
Moniin perisyklisiin reaktioihin liittyy samanlaisia vaiheittaisia radikaaliprosesseja. Kemistit ovat eri mieltä siitä, ovatko jotkin reaktiot perisyklisiä reaktioita. Ei esimerkiksi tiedetä lopullisesti, onko [2+2]-sykladition mekanismi koordinoitu (vai voiko se riippua reaktiivisesta järjestelmästä). Monilla perisyklisillä reaktioilla on samanlaisia reaktioita, jotka ovat metallikatalysoituja. Mutta nämä metallikatalysoidut reaktiot eivät myöskään ole varsinaisesti perisyklisiä. Metallikatalyytit stabiloivat reaktion välituotteita. Reaktio ei siis ole konsertoitu, vaan pikemminkin metallin stabiloima.
Albert Eschenmoserin suorittamassa korriinisynteesissä, joka sisälsi 16π-systeemin, käytettiin suurta valon aiheuttamaa vety-sigmatrooppista siirtymää.
Mikroskooppisen palautuvuuden periaatteen vuoksi on olemassa rinnakkainen joukko "retro" perisyklisiä reaktioita, jotka suorittavat käänteisreaktion.
Mikä tekee reaktiosta perisyklisen?
Perisyklinen reaktio etenee konsertoidusti siten, että sidokset muodostuvat ja katkeavat samanaikaisesti siirtymätilan syklisessä elektronikierron kautta. Tyypillisesti reaktiot ovat stereospesifisiä ja riippuvat orbitaalien symmetriasta: miten HOMO ja LUMO vuorovaikuttavat. Tästä seuraa sääntöjä ja rajoituksia, jotka määräävät, millaiset perisykliset reaktiot ovat termisesti tai fotokemiallisesti "sallituita".
Mekanismit ja orbitaalien symmetria (Woodward–Hoffmann)
- Perisyklisiä reaktioita ohjaavat orbitaalien symmetria- ja fazisuhteet. Woodward–Hoffmannin säännöt kertovat, millaiset elektroninsiirrot ovat konsertoituja ja siten termisesti tai fotokemiallisesti sallittuja.
- Thermal vs. photochemical: Sama reaktio voi olla termisesti estetty mutta fotokemiallisesti sallittu ja päinvastoin, koska excitointi muuttaa elektronien järjestelyä ja orbitaalien täyttöä.
- Suprafacial ja antarafacial: sidoksen muodostuminen tai siirtyminen voi tapahtua suprafacial-tavalla (saman puolen yli) tai antarafacial-tavalla (vastakkaiselta puolelta), mikä vaikuttaa stereokemiaan ja siihen, onko reaktio orbitaalien symmetrian suhteen sallittu.
- Sähkösyklisissä reaktioissa esiintyy usein conrotatory- ja disrotatory-liikkeitä, jotka kuvaavat substituenttien pyörimissuuntaa renkaan avaamisessa tai sulkeutumisessa.
Tärkeimmät perisyklisten reaktioiden tyypit (kuvaus ja esimerkkejä)
Seuraavassa selitetään lyhyesti luettelossa mainitut pääryhmät ja annetaan tyypillisiä esimerkkejä.
Sähkösykliset reaktiot
- Koskevat monisidosten avautumista tai sulkeutumista, esimerkiksi cyclobuteenin avautuminen 1,3-butadieniksi.
- Orientaatiot (conrotatory vs. disrotatory) riippuvat elektronien määrästä (4n tai 4n+2 π-elektronia) ja siitä, tapahtuuko reaktio termisesti vai fotokemiallisesti.
- Esimerkki: 4π-järjestelmän terminen avautuminen on yleensä conrotatory; 6π-järjestelmän terminen sulkeutuminen on disrotatory.
Sykloadditiot (cycloadditions)
- Diels–Alder ([4+2]) on kaikkein tunnetuin: termisesti sallittu, stereospesifinen ja erittäin hyödyllinen synteesissä. Antaa kuusijäsenisiä renkaita stereokontrollilla.
- [2+2]-sykloadditiot ovat termisesti yleensä orbitalisen symmetrian takia estettyjä, mutta fotokemiallisesti sallittuja. Lisäksi metallikatalyysi tai radikaalinen mekaanismi voi johtaa samanlaisiin tuotteisiin, mutta tällöin reaktio ei ole konsertoitu perisyklinen prosessi.
- Cheletropic-reaktiot (lueteltu alkuperäisessä tekstissä keletrooppiset reaktiot) ovat sykloadditioiden alalaji, jossa yksi atomi muodostaa kaksi sidosta samaan reagentoosiin (esim. joissain karbonyylin tai karbeenin lisäyksissä).
Sigmatrooppiset reaktiot
- Sigmatrooppisessa siirtymässä σ-sidos liikkuu konjugoitua π-järjestelmää pitkin ja elektronit kiertävät syklistä siirtymätilaa. Merkintätapa on [i,j]-sigmatropia, jossa σ-atomien etäisyydet muuttuvat.
- Esimerkkejä: Cope- ja Claisen-uudelleenjärjestelyt sekä [1,5]-vetysiirtymät. [1,5]-H-siirto voi olla suprafacial ja stereospecific.
- Eschenmoserin korriinisynteesissä mainittu 16π vety-sigmatrooppinen siirtymä on esimerkki fotokemiallisesti indusoitavasta laajasta perisyklisestä muutoksesta.
Ryhmänsiirtoreaktiot ja ene-reaktiot
- Ryhmänsiirtoreaktioihin kuuluu esimerkiksi ene-reaktio, jossa alkeeni (ene) ja elektrofiili (enophile) reagoivat siten, että yksi atomi (esim. vety) siirtyy ja uusi σ- ja π-sidos muodostuvat samanaikaisesti.
- Nämä reaktiot ovat usein stereospesifisiä ja voivat edetä konsertoidusti perisyklisin piirtein.
Dyotrooppiset reaktiot
- Dyotrooppisessa rearrangemennissa kaksi σ-sidosmolekyyliä siirtyy samanaikaisesti. Tyypillisesti molempien siirtojen välillä on synkronia, ja ilmiö esiintyy esimerkiksi tietyissä halogeeninsiirtymissä.
Stereokemia, todistus ja raja‑tapaukset
- Perisykliset reaktiot ovat usein stereospecific: lähtöaineen stereokemialliset piirteet heijastuvat tuotteeseen (cis/trans, syn/anti).
- Todaistusmekanismit perustuvat stereospesifisyyteen, isotopopainaviivauksiin, kinematiikkaan, sekvenssikokeisiin ja laskennallisiin orbitaalitutkimuksiin. Jos syntyy eristettäviä radikaali- tai ionivälituotteita, reaktio ei ole konsertoitu perisyklinen.
- Monet perisykliset reaktiot voidaan häiritä tai muuttaa metallikatalyytin avulla; tällöin mekanismi usein muuttuu vaiheittaiseksi, ja reaktio ei enää kuulu perisyklisiin prosesseihin.
Sovelluksia ja merkitys synteesissä
Perisykliset reaktiot ovat keskeisiä orgaanisessa synteesissä, koska ne tarjoavat tehokkaan tavan rakentaa monimutkaisia renkaistoja ja stereokeskeisiä rakenteita yhdellä askelmuutoksella. Diels–Alder-reaktio, sähkösykliset sulkeutumiset ja sigmatrooppiset uudelleenjärjestelyt ovat usein avainaskelia luonnonainemetabolian jäljittelyssä ja kokonaissynteeseissä.
Kun reaktio ei ole selvästi perisyklinen
Joissain tapauksissa tuotteet näyttävät perisyklisten reaktioiden kaltaisilta, mutta mekanismi voi olla vaiheittainen (radikaali- tai ionivälivaiheet) tai metallin välittämä. Esimerkiksi monet [2+2]-tuotteet syntyvät fotoreaktiolla tai metallikatalyysin kautta eikä niiden termistä konsertoitua reittiä voida pitää perisyklisenä. Siksi mekanismitutkimus on tärkeä osa perisyklisen katalogin määrittämistä.
Yhteenveto
- Perisykliset reaktiot etenevät konsertoidusti syklisen siirtymätilan kautta ja ovat usein stereospesifisiä.
- Orbitaalien symmetria (Woodward–Hoffmann) määrää, mitkä reaktiot ovat termisesti tai fotokemiallisesti sallittuja.
- Tärkeimpiä tyyppejä ovat sähkösykliset reaktiot, sykloadditiot, sigmatrooppiset siirtymät, ryhmänsiirtoreaktiot, keletrooppiset (cheletropic) ja dyotrooppiset reaktiot.
- Metallikatalyysi ja radikaalireitit voivat luoda tuotteita, jotka muistuttavat perisyklisiä tuotteita, mutta mekanismi tällöin poikkeaa konsertoidusta perisyklisestä reaktiosta.
Edellä oleva täydentää alkuperäistä kuvausta ja antaa käytännöllisiä näkökulmia perisyklisiin reaktioihin ja niiden synteettiseen merkitykseen.