Sigmatrooppinen reaktio on orgaanisessa kemiassa perisyklinen reaktio. Sigmatrooppisessa reaktiossa ei käytetä katalyyttiä, ja siihen osallistuu yksi molekyyli (katalysoimaton intramolekulaarinen prosessi). Siinä yksi σ-sidos muuttuu toiseksi σ-sidokseksi. Nimitys sigmatrooppinen on seurausta yksittäisten hiili-hiilisidosten pitkäaikaisesta nimityksestä "sigma" ja kreikan kielen sanasta tropos, joka tarkoittaa kääntymistä. Kyseessä on uudelleenjärjestelyreaktio, joka tarkoittaa, että molekyylin sidokset siirtyvät atomien välillä ilman, että molekyylistä poistuu atomeja tai siihen lisätään uusia atomeja. Sigmatrooppisessa reaktiossa substituentti siirtyy π-sidoksen yhdestä osasta toiseen osaan molekyylinsisäisessä reaktiossa, jossa π-systeemi järjestäytyy samanaikaisesti uudelleen. Todelliset sigmatrooppiset reaktiot eivät yleensä tarvitse katalyyttiä. Joitakin sigmatrooppisia reaktioita katalysoi Lewisin happo. Sigmatrooppisia reaktioita katalysoivat usein siirtymämetallit, jotka muodostavat välituotteita analogisissa reaktioissa. Sigmatrooppisista uudelleenjärjestelyistä tunnetuimpia ovat [3,3]-Cope-reaktio, Claisen-reaktio, Carroll-reaktio ja Fischerin indolisynteesi.
Mekanismi — konsertoitu perisyklinen siirtymä
Sigmatrooppiset reaktiot ovat yleisesti konsertoituja perisyklisiä prosesseja: siirtyvä σ-sidos ja sitä ympäröivä π-järjestelmä muodostavat syklisten elektronisiirtojen kautta taipuvan, syklisen siirtymätilan. Tämän siirtymätilan elektroninen järjestely noudattaa orbitalisymmetrian sääntöjä (Woodward–Hoffmann), eli reaktion todennäköisyys ja stereokemia määräytyvät HOMO–LUMO-orbitaalien synkroniasta. Usein siirtymätila voidaan ajatella eräänlaisena aromaattisena (Hückel- tai Möbius-tyyppisen) elektronikonfiguraation kautta stabiloituna.
Notaatio ja stereokemia
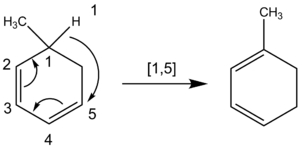
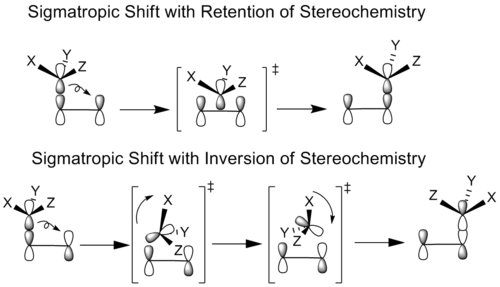
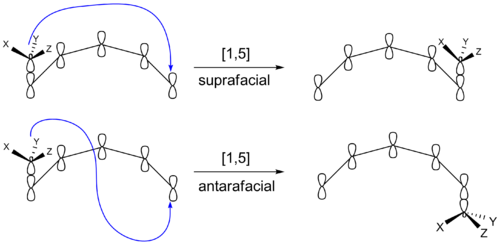
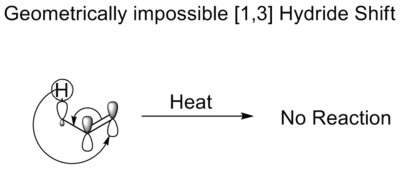
Sigmatrooppiset siirtymät merkitään muodossa [i,j], jossa i ja j ilmaisevat kuinka monnen atomin etäisyydelle kumpikin siirtyvän sidoksen päätepisteistä uusi sidos muodostuu pitkin conjugoitua ketjua. Esimerkiksi [1,5]-hydrogen shift tarkoittaa, että siirtyvä vetyatomi siirtyy ketjun yhden ja viiden sijainnin välille. Reaktion stereokemia voidaan luokitella sen mukaan, tapahtuuko siirtymä suprafaciaalisesti (sama puoli π-jonosta) vai antarafaciaalisesti (vastakkaiset puolet). Pienet atomit kuten vety voivat usein siirtyä suprafaciaalisesti, kun taas suurempien ryhmien antarafaciaalinen siirtymä on usein geometrisesti estetty.
Termiset vs. fotokemialliset olosuhteet
Monet sigmatrooppiset reaktiot tapahtuvat lämmön avulla (termisesti) ja noudattavat silloin tiettyjä orbitalisymmetrian valintaehtoja. Fotokemiallinen eksitointi voi muuttaa näitä valintaehtoja ja siten sallia reaktiotyyppejä, jotka termisissä olosuhteissa olisivat epäsuotuisia. Käytännössä tämä tarkoittaa, että sama rakenne voi reagoida eri tavalla valon tai lämmön vaikutuksesta.
Tunnettuja esimerkkejä
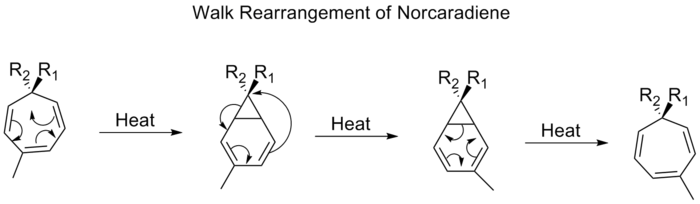
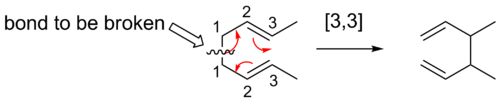
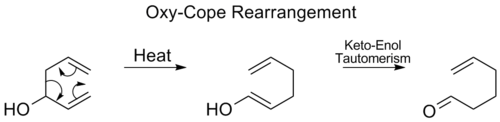
- [3,3]-Cope-reaktio — klassinen sigmatrooppinen uudelleenjärjestely 1,5-dieeneillä. Esimerkiksi 1,5-dieeni voi isomerisoitua toiseen 1,5-dieenimuotoon konsertoidun [3,3]-siirtymän kautta.
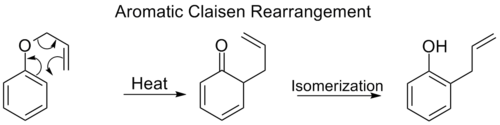
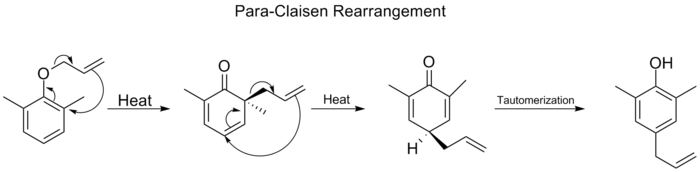
- Claisen-reaktio — [3,3]-sigmatrooppinen rearrangement, jossa allyylivinyylieetteri rearrangeoituu muodostaen usein γ,δ-epätyydyisiä tuotteita (esim. allyylifenolit tai γ,δ-unsaturated carbonyl -rakenteet riippuen lähtöaineesta ja olosuhteista). Claisen on laajasti käytetty synteesimenetelmä C–C-sidoksen rakentamiseen.
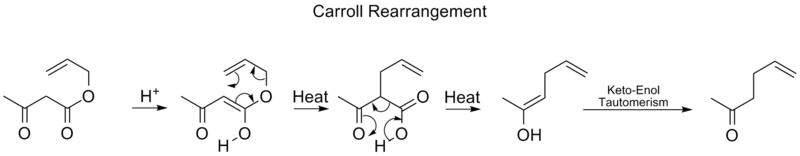
- Carroll-reaktio — decarboxylatiivinen [3,3]-tyyppinen siirtymä, jossa allyyli- tai vinylisterit voivat reorganisoitua ja samalla tapahtuu karboksyyliryhmän menetys muodostaen esimerkiksi allyyliketonin.
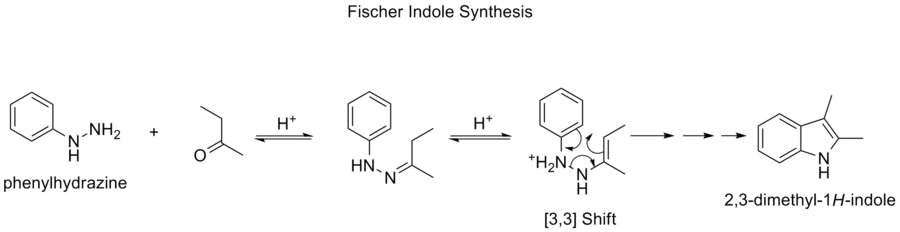
- Fischerin indolisynteesi — monivaiheinen synteesi, jonka mekanismiin kuuluu sigmatrooppisia vaiheita (esim. [3,3]-tyyppisiä uudelleenjärjestelyjä) hydrazoni-intermediaattien muuttumisessa indolirungoksi.
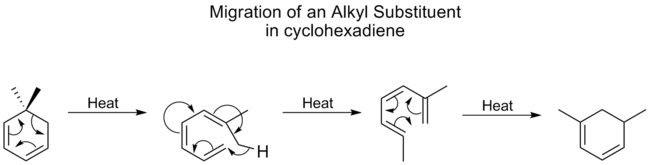
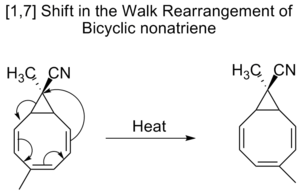
- [1,5]-hydride shift — yleinen tapaus joissa vety siirtyy konjugoituneissa järjestelmissä; tärkeä esimerkiksi tietyissä isomerisaatioissa ja tum-lab:issa.
Katalyysi ja poikkeukset
Vaikka sigmatrooppiset reaktiot periaatteessa eivät vaadi katalyyttiä, ne voivat olla helpommin toteutettavissa tai selektiivisempiä katalyyttien avulla. Lewisin hapot voivat aktivoida π-järjestelmää ja alentaa siirtymätilan energiaa, ja siirtymämetallikatalyysi voi muuttaa reaktiopolun kokonaan muodostaen metalli-organiset välituotteet, jotka eivät ole täysin konsertoituja mutta johtavat vastaavan lopputuotteen. Tällaiset katalysoidut polut saatetaan teknisesti erottaa klassisesta sigmatrooppisesta mekanismista, mutta ne hyödyntävät samaa sidoksen uudelleenjärjestelyn ideaa.
Käytännön merkitys
Sigmatrooppiset reaktiot ovat tärkeitä orgaanisessa synteesissä, koska ne mahdollistavat atomien ja funktionaalisten ryhmien selektiivisen siirron ilman erillisiä liitoksia tai suoria kovalenttisia katkaisuja ja liitoksia. Niitä käytetään rakenteiden muokkaamiseen, stereokemian kontrollointiin ja kompleksisten, polystruktuuristen molekyylien muodostamiseen luonnontuotteiden ja lääkeaineiden synteesissä.
Yhteenveto: Sigmatrooppinen reaktio on konsertoitu perisyklinen uudelleenjärjestely, jossa σ-sidos siirtyy toiseen kohtaan samalla kun π-järjestelmä reorganisoituu. Reaktion sallittavuus ja stereokemia määräytyvät orbitalisymmetrian perusteella (Woodward–Hoffmann). Tunnettuja esimerkkejä ovat mm. Cope- ja Claisen-reaktiot, ja näillä reaktioilla on laaja käyttöala synteesikemiassa.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)