Järjestäytymisreaktio on orgaaninen reaktio, jossa molekyylin hiilirunko järjestyy uudelleen. Tuloksena on alkuperäisen molekyylin rakenteellinen isomeeri. Usein substituentti siirtyy atomista toiseen atomiin samassa molekyylissä. Alla olevassa esimerkissä substituentti R siirtyy hiiliatomista 1 hiiliatomiin 2:
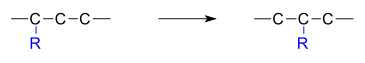
Myös molekyylien välisiä uudelleenjärjestelyjä tapahtuu.
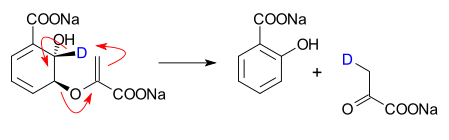
Miten uudelleenjärjestäytymisreaktiot kuvataan ja mitä ne tarkoittavat käytännössä
Joskus kemistit piirtävät nuolilla varustettuja kaavioita, jotka osoittavat, miten elektronit siirtyvät sidosten välillä uudelleenjärjestelyreaktion aikana. Monissa orgaanisen kemian oppikirjoissa on tällaisia kaavioita. Ne eivät kuitenkaan kerro koko reaktiomekanismia. Todellinen mekanismi uudelleenjärjestäytymisessä, jossa alkyyliryhmä liikkuu, on se, että ryhmä liukuu sujuvasti sidosta pitkin, ei ionisidoksen katkeaminen ja muodostuminen. Yksi esimerkki tästä on Wagner-Meerweinin uudelleenjärjestely:
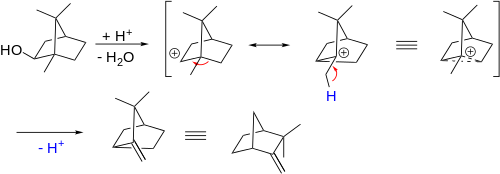
Perisyklisissä reaktioissa orbitaalien vuorovaikutukset ovat tärkeitä. Reaktioita ei voida selittää yksinkertaisten elektronien siirtojen sarjalla. Mutta kaarevat nuolet, jotka osoittavat erillisten elektroninsiirtojen sarjan, voivat antaa saman tuloksen kuin uudelleenjärjestäytymisreaktio. Kaaviot eivät kuitenkaan välttämättä ole realistisia. Allyylisessä uudelleenjärjestäytymisessä reaktio on ioninen.
Tärkeimmät reaktiotyypit ja esimerkkejä
Kolme tärkeää uudelleenjärjestäytymisreaktiota ovat 1,2-reaktiot, perisykliset reaktiot ja olefiinimetatoosi. Lisäksi on useita nimettyjä uudelleenjärjestelyjä, joilla on suuri merkitys synteesissä ja biologisissa prosesseissa. Alla on yleiskatsaus tärkeimmistä tyypeistä:
- 1,2-siirtymät (1,2-shift): pieni ryhmä (esim. hydride tai alkyyliryhmä) siirtyy vierekkäiselle hiilelle. Tyypillisesti liittyy karbokationien osallisuuteen (esim. Wagner–Meerwein). Migratorinen affiniteetti: usein hydride > aryyli > alkyyli, mutta ympäristö vaikuttaa.
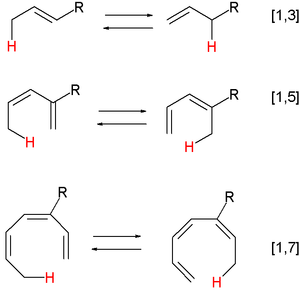
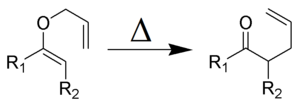
- Perisykliset reaktiot: konsertoituneita elektronisiirtymiä, joissa orbitaalien synkroninen vuorovaikutus määrää reaktion stereokemian (esim. sigmatropiset siirtymät kuten Cope- ja Claisen-uudelleenjärjestelyt, sekä elektroosien sulkeutuminen/avautuminen).
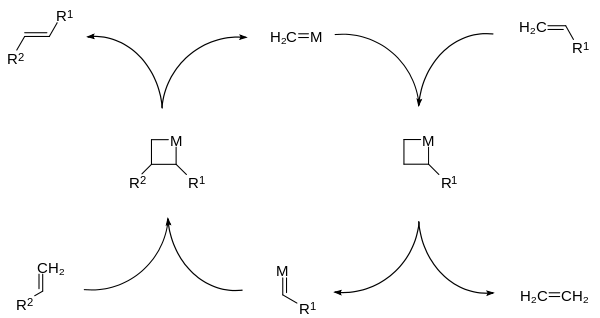
- Olefiinimetatoosi: kaksi alkeenia vaihtaa substituentteja katalysoidusti (usein metallikatalyyttien avulla). Tämä ei ole klassinen ”siirtymä” yksittäisessä molekyylissä, vaan katalyyttinen uudelleenjärjestely alkeenisidosten välillä.
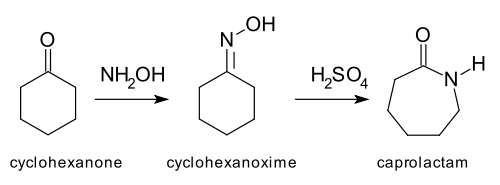
- Beckmann-, Curtius-, Baeyer–Villiger-, Schmidt- ja Pinacol-reaktiot: nimettyjä reorganisaatioreaktioita, joissa tapahtuu ryhmän siirtymä eri funktionaalisten ryhmien välillä (esim. Beckmann: oksimi → amidi; Baeyer–Villiger: ketoni → esteri).
- Enzymatic rearrangements: biologisissa järjestelmissä entsyymit, kuten mutaasit tai lyaasit, katalysoivat tarkkoja uudelleenjärjestelyjä (esim. isochorismate-pyruvaatti-lyaasin katalysoima reaktio, kuva yllä).
Mekanismien peruserot: konsertoitu vs. ioninen
Uudelleenjärjestäytymisreaktiot voivat edetä eri tavoin:
- Konsertoidut (concerted) reaktiot: kaikki sidosten muodostuminen ja katkeaminen tapahtuu samanaikaisesti. Tyypillistä perisyklisille ja sigmatropisille reaktioille. Konsertoitu mekanismi antaa usein ennustettavan stereokemian.
- Ioniset reaktiot: väliintuotteina ovat karbokationit, radikaalit tai karboanionit. Esimerkiksi monet 1,2-siirtymät etenevät karbokationivälituotteen kautta, jolloin substituentin migratio riippuu karbokationin stabiilisuudesta ja migratorisesta taipumuksesta.
Tekijät, jotka vaikuttavat uudelleenjärjestäytymiin
- Katalyytti ja olosuhteet: hapot (Brønsted- tai Lewis-hapot) edistävät usein karbokationivälitteisiä siirtymiä; metallikatalyytit mahdollistavat olefiinimetataasin.
- Ryhmätyyppi: hydride-siirtymät ovat usein nopeampia kuin alkyylisiirtymät; aryylisiirtymä voi olla erikoistapauksissa suosittu, jos konjugaatio säilyy.
- Stereokemia ja konformaatio: tietyt siirtymät vaativat tietynläisen orientaation siirtyvälle ryhmälle (esim. antiperiplanaarisuus sigmatropisissa reaktioissa).
- Entropia ja energia: välituotteiden stabiilisuus ja siirtymän olemassaolo määrittävät reaktion nopeuden ja tasapainon.
- Ympäristö: liuotin, lämpötila ja substraatin lähialueen substituentit vaikuttavat merkittävästi.
Stereokemia ja seuraukset synteesissä
Uudelleenjärjestäytymiset voivat muuttaa stereokeskuksia, johtaa epästereoselektiivisiin seoksiin tai päinvastoin antaa stereospesifisiä tuotteita riippuen mekanismista. Synteesissä uudelleenjärjestely voi olla hyödyllinen työkalu (esim. hiiliketjun muokkaus) tai ei-toivottu sivureaktio. Kemistit suunnittelevat reaktioreitit huomioiden mahdolliset uudelleenjärjestelyt ja valitsevat katalyytit/ehdot niiden ohjaamiseksi tai estämiseksi.
Tunnistaminen ja tutkimusmenetelmät
- NMR- ja massaspektrometria: rakenne- ja isomerointitunnistukseen.
- Isotooppileimaukset: kertovat, mikä atomi tai ryhmä liikkui reaktion aikana.
- Kinetiikka ja välituotteiden havaitseminen: auttavat erottamaan konsertoidun ja vaiheittaisen mekanismin.
- Laskennalliset menetelmät: orbitaalien vuorovaikutuksia ja siirtymätilojen energioita voidaan tutkia teoreettisella kemiolla.
Biologinen ja teollinen merkitys
Uudelleenjärjestäytymisreaktiot esiintyvät laajasti biosynteesissä (esim. terpeneiden muokkautuminen) ja ne ovat tärkeitä teollisessa orgaanisessa synteesissä (esim. raaka-aineiden muunnokset, heterosyklien muodostus). Entsyymit tarjoavat usein korkean selektiivisyyden ja toimintaympäristön, jossa uudelleenjärjestelyt tapahtuvat tehokkaasti ja stereokontrolloidusti.
Yhteenveto
Uudelleenjärjestäytymisreaktiot ovat monimuotoinen luokka reaktioita, joissa molekyylin atomien tai ryhmien paikallistaminen muuttuu ilman että kokonaan eri yhdisteitä muodostuu; tuloksena on yleensä rakenneisomeeri. Reaktiot voivat olla konsertoituja tai ionisia, ja ne ovat keskeisiä sekä orgaanisessa synteesissä että biologisissa prosesseissa. Kemistit käyttävät erilaisia strategioita ja analyyttisia menetelmiä ohjatakseen ja tutkiakseen näitä reaktioita.
.png)