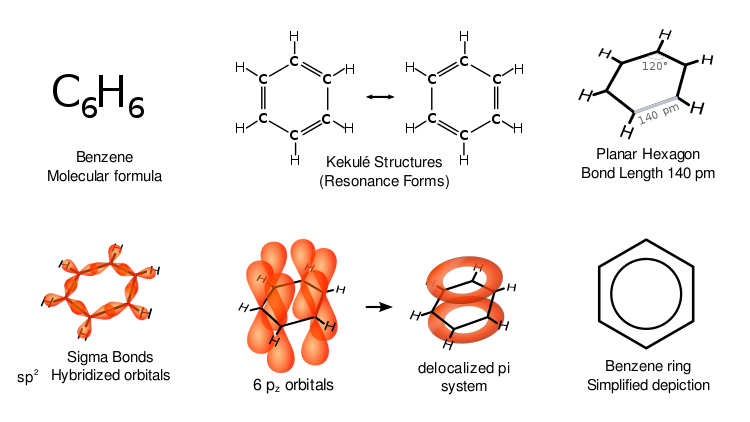Bentseeni, joka tunnetaan myös nimellä bentsoli, on orgaaninen kemiallinen yhdiste, jonka kaava on 6CH6. Se on väritön ja syttyvä neste, jolla on makea haju. Bentseenimolekyylit ovat rengas, jossa on kuusi hiiliatomia, joista kukin on sitoutunut yhteen vetyatomiin. Se on aromaattinen yhdiste, eli renkaassa on vuorotellen kaksoissidoksia.
Bentseeni on karsinogeeninen eli se voi aiheuttaa syöpää. Sillä on monia todellisia käyttötarkoituksia. Sitä käytetään lisäaineena bensiinissä, muoveissa, synteettisessä kumissa, väriaineissa ja se on teollinen liuotin, mikä tarkoittaa, että se voi liuottaa monia muita kemiallisia molekyylejä. Bentseeni on myös luonnollinen osa raakaöljyä, joten sitä on bensiinissä. Monet lääkkeet sisältävät bentseenistä valmistettuja osia.
Rakenne ja kemialliset ominaisuudet
Kemiallinen kaava: C6H6 (sub>6CH6 edellisen tekstin mukaisesti). Bentseeni on aromaattinen sykli, jossa kuuden hiiliatomin rengas muodostaa delokalisoituneen elektronijärjestelmän. Tämä tekee bentseenistä erityisen stabiilin verrattuna tavallisiin tyydyttymättömiin renkaisiin.
- Fysikaaliset tunnusluvut: väritön, haihtuva neste, tyypillinen kiehumispiste n. 80 °C ja tiheys alle veden (noin 0,88 g/cm³). Bentseeni on helposti syttyvä ja sillä on alhainen leimahduspiste.
- Reaktiivisuus: bentseeni osallistuu tyypillisesti elektrofiilisiin aromaattisiin substituutioreaktioihin (esim. nitraus, sulfonointi, halogenaatio) sen sijaan, että renkaassa tehtäisiin helppoja additioreaktioita.
Käyttö ja tuotanto
Bentseeniä tuotetaan pääosin öljynjalostuksen ja petrokemian prosesseissa. Teollisuudessa sitä käytetään lähtöaineena monien tärkeiden kemikaalien valmistuksessa, muun muassa:
- styreenin ja sitä kautta polystyreenin sekä muiden muovien valmistuksessa,
- fenolin ja aniliinin synteesissä, jotka ovat valmistuslähtöaineita lääkeaineille, väriaineille ja muille tuotteille,
- liuottimena ja reagenssina laboratoriokäytössä,
- bensiinin komponenttina ja sen epäpuhtautena (luonnollisesti raakaöljystä peräisin).
Altistuminen ja terveysvaikutukset
Lyhytaikainen altistuminen: hengitettynä bentseeni voi aiheuttaa haittoja kuten päänsärkyä, huimausta, uneliaisuutta, pahoinvointia ja nokea hengitysteissä. Suurempina pitoisuuksina voi seurata tajuttomuutta.
Pitkäaikainen altistuminen: bentseeni on liitetty verisolujen muutoksiin, erityisesti aplastiseen anemiaan ja leukemian (erityisesti myelooinen leukemia) riskiin. Kansainvälinen syöpätutkimusjärjestö IARC luokittelee bentseenin karsinogeeniseksi ihmiselle (ryhmä 1).
Elimistön käsittely: hengitysteitse imeytyminen on yleisin altistumisreitti; bentseeni metaboloituu maksassa ja sen metaboliitit voivat vaurioittaa solujen DNA:ta ja verisoluja.
Altistumisen rajoittaminen ja sääntely
- Työperäisissä ympäristöissä altistumisen raja-arvot vaihtelevat maittain. Esimerkiksi jotkin suositusarvot (esim. ACGIH) ovat alle 1 ppm pitkäaikaista keskiarvoa kohti. Tarkat arvot ja pakolliset raja-arvot löydät oman maan työturvallisuusviranomaisen ohjeista.
- Yksityishenkilöiden altistumista pyritään vähentämään päästörajoituksilla, bensiiniseosten sääntelyllä ja tupakoinnin vähentämisellä (tupakansavu sisältää bentseeniä).
Turvallinen käsittely ja ensiapu
- Käsittely: käytä suljettuja prosesseja, tehokasta ilmanvaihtoa, sekä asianmukaisia hengityssuojaimia ja kemikaalikestäviä suojakäsineitä. Vältä avotulen lähistöllä työskentelyä, sillä bentseeni on helposti syttyvä.
- Säilytys: viileässä, hyvin ilmastoidussa tilassa ja kaukana syttymislähteistä. Säiliöiden tulee olla maadoitettuja ja varustettu ylivuototurvallisuudella.
- Ensiapu: hengityksen vaikeutuessa siirrä henkilö raittiiseen ilmaan ja hakeudu lääkäriin. Ihokosketuksen jälkeen riisu saastuneet vaatteet ja pese iho runsaalla vedellä. Roiskeet silmiin huuhdellaan vedellä vähintään 15 minuutin ajan ja otetaan yhteys lääkäriin.
Ympäristövaikutukset
Bentseeni on haihtuva orgaaninen yhdiste ja voi päätyä ilmaan, maaperään ja pohjaveteen. Ilmassa se hajoaa suhteellisen nopeasti photokemiallisten reaktioiden avulla, mutta maaperässä ja vedessä bentseeni voi aiheuttaa pitkäkestoisempia paikallisia haittoja, erityisesti pohjavesien pilaantumista. Päästöt syntyvät muun muassa teollisuudesta, öljyvuodoista ja liikenteestä.
Yhteenveto
Bentseeni on tärkeä teollinen raaka-aine ja liuotin, mutta samalla se on merkittävä terveysriski, erityisesti pitkäaikaisen altistumisen yhteydessä. Asianmukaiset suojatoimet, päästöjen vähentäminen ja sääntely ovat keskeisiä keinoja suojella työntekijöitä ja ympäristöä. Jos epäilet bentseenialtistusta työssä tai kotona, ota yhteys työturvallisuudesta vastaavaan tahoon tai terveydenhuoltoon.

_1964,_MiNr_440.jpg)