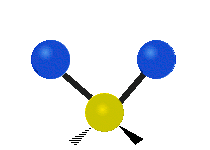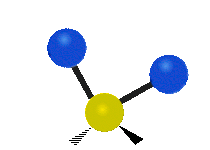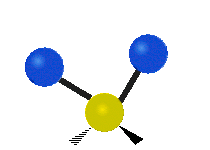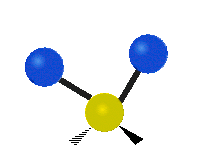
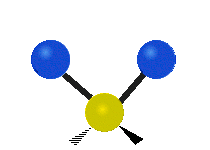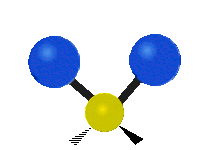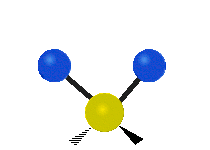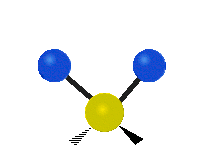
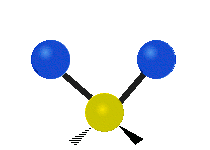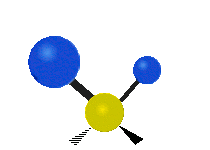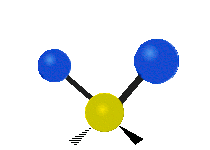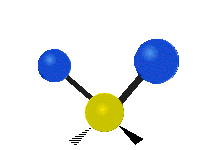
Molekyylien värähtelyt ovat yksi kolmesta erilaisesta molekyylien liiketyypistä, joita ovat translaatioliike (kun koko molekyyli liikkuu samaan suuntaan) ja rotaatioliike (kun molekyyli pyörii kuin kääntölevy). Molekyylin värähtelyliike tarkoittaa sitä, että molekyylin atomien väliset sidokset muuttavat pituuttaan ja/tai kulma-asentojaan ajassa — ajattele atomeja palloina, jotka on yhdistetty joustinmaisilla sidoksilla, jotka voivat venyä ja puristua tai taivuttaa kulmaansa.
Yksinkertaisin värähtely on kaksiatomisen molekyylin venytys, jossa kahden atomin välinen etäisyys muuttuu. Tällainen esimerkki on diatominen molekyyli kuten vety H2, typpi N2 tai happi O2, joissa on vain yksi värähtelymodeemi (aallonpituuden muuttuminen on venytys). Värähtelyt ovat kvantittuneita: energiatasona esiintyy diskreettejä arvoja, ja harmonisen värähtelijän malli antaa energia-arvoille muodon E = (v + 1/2) hν (v = 0,1,2...). Tämä aiheuttaa mm. nollapistesuuruuden (zero-point energy), eli v = 0 -tilassa energia ei ole nolla.
Värähtelytyypit ja normaali-tilat
Moniatomisessa molekyylissä yksittäisiä atomeja voi liikkua monella tavalla, mutta liikkeitä voidaan esittää normaali-tiloina (normal modes) — itsenäisinä värähtelyinä, joissa kaikki atomit liikkuvat tietyn kaavan mukaan.
- Venytys (stretching): sidoksen pituuden muutos. Voi olla symmetrinen tai epä-symmetrinen.
- Kulman taipuminen (bending): atomien välisten kulmien muutos. Muotoja ovat mm. scissoring (saksimainen), rocking, wagging ja twisting.
Jos molekyylissä on N atomia, normaalien värähtelyjen lukumäärä on yleensä 3N − 5 (lineaarisille molekyyleille) tai 3N − 6 (ei-lineaarisille molekyyleille). Esimerkiksi:
- Diatominen (N = 2): 1 värähtelytila (venytys).
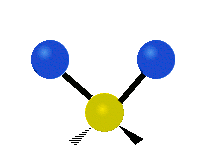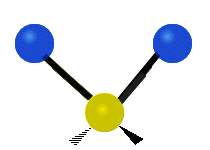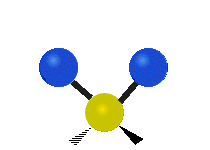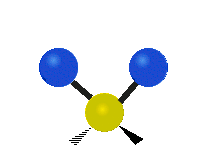
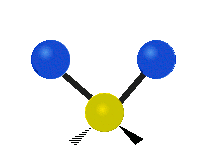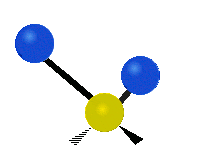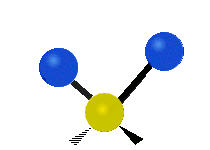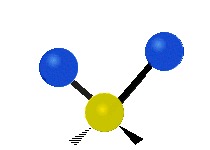
- Vesimolekyyli H2O (N = 3, ei-lineaarinen): 3 normaalia tilaa (symmetrinen venytys, epäsymmetrinen venytys, taivutus).
- Hiilidioksidi CO2 (lineaarinen): 3N−5 = 4 normaalia tilaa (symmetrinen venytys, epäsymmetrinen venytys, kaksi degeneraattia taivutukselle).
Mallit ja fysikaaliset tekijät
Yksinkertainen malli on harmoninen värähtelijä, jossa värähtelytaajuus ν liittyy sidoksen jäykkyyteen (voimavakio k) ja reduktioituun massaan μ kaavalla ν ∝ (1/2π)·√(k/μ). Siitä seuraa useita havainnollisia vaikutuksia:
- Vahvempi sidos (suurempi k) → korkea taajuus (korkeampi energia).
- Raskaammat atomit (suurempi μ) → matalampi taajuus. Tämä selittää isotoptunnuksen vaikutukset (esim. H → D siirtää taajuutta alaspäin).
- Reaalisissa molekyyleissä esiintyy anharomonisuutta, jolloin energiaerot eivät ole täysin tasavälein ja sidokset voivat katketa tai vaihtaa muotoa korkeissa tiloissa.
Spektroskopia ja käytännön merkitys
Molekyylien värähtelyjä mitataan pääasiassa infrapunaspektroskopialla (IR) ja Raman-spektroskopialla. Näillä menetelmillä tunnistetaan funktionaalisia ryhmiä ja mitataan sidosominaisuuksia. Tärkeitä seikkoja:
- IR‑aktiivisuus: värähtelymuutos, joka muuttaa molekyylin dipolimomenttia, näkyy IR-spektrissä.
- Homonukleaariset diatomit (esim. H2, N2, O2) eivät muuta dipolimomenttia venyessään ja ovat siten IR‑inaktiivisia, mutta ne voivat olla Raman-aktiivisia.
- Spektrin yksiköt usein annetaan taajuuden sijasta aalto- tai aallonlukuna (cm−1). Esimerkkejä tyypillisistä värähtelyalueista: C–H noin 3000 cm−1, C=O noin 1700 cm−1, O–H noin 3200–3600 cm−1.
Esimerkkejä ja sovelluksia
- Suoran esimerkin tarjoaa H2 tai N2 — molemmilla on vain yksi venytys, ja niiden spektrit kertovat sidoksen voimakkuudesta ja massa‑vaikutuksesta.
- Veden (H2O) kolme normaalia tilaa näkyvät selkeästi IR‑spektrissä ja ovat tärkeitä tunnistettaessa vettä ja hydroksyyli‑ryhmiä kemiallisissa analyyseissä.
- Värähtelyt vaikuttavat myös termodynamiikkaan (esim. lämpökapasiteetit, kemiallisten reaktioiden energiatasot) ja kemialliseen reaktiivisuuteen (energian jakautuminen sidoksille).
Yhteenvetona: molekyylien värähtelyt kuvaavat atomeihin kohdistuvia suhteellisia liikkeitä ja ovat keskeisiä molekyylien fysikaalisten ominaisuuksien ja tunnistamisen kannalta. Ne riippuvat sidosten jäykkyydestä, atomien massasta ja molekyylin rakenteesta, ja niitä tutkitaan laajasti spektroskopiaa ja teoreettisia malleja käyttäen.