Maailmankaikkeudessa on neljä yleistä aineen olomuotoa (tai faasia): kiinteä, neste, kaasu ja plasma. Aineen olomuoto vaikuttaa aineen ominaisuuksiin, kuten tiheyteen, viskositeettiin (kuinka hyvin se virtaa), muovattavuuteen (kuinka helposti se taipuu) ja johtavuuteen.
Peruskuvaus: miten hiukkaset järjestäytyvät
Erilaiset olomuodot eroavat toisistaan hiukkasten (atomien, molekyylien tai ionien) keskinäisen järjestyksen ja liikkeen perusteella. Yksinkertaistaen:
- Kiinteä: hiukkaset ovat tiukasti sidoksissa toisiinsa ja sijaitsevat likimain paikallaan, minkä vuoksi kiinteillä on oma muoto ja tilavuus.
- Neste: hiukkaset ovat lähekkäin mutta voivat liukua toistensa ohi, joten nesteellä on tietty tilavuus mutta ei pysyvää muotoa — se ottaa astian muodon.
- Kaasu: hiukkaset liikkuvat vapaasti ja ovat etäällä toisistaan; kaasulla ei ole omasta muotoa eikä vakioista tilavuutta, vaan se täyttää käytettävissä olevan tilan.
- Plasma: erittäin kuuma tai sähköisesti varautunut kaasu, jossa atomit ovat osittain tai täysin ionisoituneet (vapaita elektroneja ja ioneja); plasman sähkön- ja lämmönjohtavuus on suuri.
Kiinteät aineet
Kiinteillä aineilla on usein säännöllinen kiderakenne (kiteitä) tai epäsäännöllinen lasimainen rakenne (amorfit). Niiden ominaisuuksia:
- Kiinteät kestävät muodonmuutoksia ja niillä on korkea leikkauslujuus verrattuna nesteisiin.
- Lujuus, kovuus, sitkeys ja elastisuus vaihtelevat suuresti materiaalin mukaan (esim. metallit, keraamit, polymeerit).
- Joillain kiinteillä on hyvä sähkön- ja lämmönjohtavuus (metallit), toisilla ei (eristeet).
- Esimerkkejä: jää, rauta, muovi, lasi.
Nesteet
Nesteet virtaavat ja konvehoivat lämpöä tehokkaasti. Tärkeitä piirteitä:
- Viskositeetti: kuvaa kitkaa, joka hidastaa virtausta (esim. hunaja on viskoosimpaa kuin vesi).
- Pintajännitys: johtuu molekyylien vetovoimista pinnalla ja vaikuttaa pisaran muodostumiseen ja kapillaariseen ilmiöön.
- Nesteet voivat liuottaa aineita, minkä vuoksi ne toimivat usein reaktiomedioina ja liuottimina.
- Esimerkkejä: vesi, öljy, lyijy (sulassa olomuodossa), veri.
Kaasut
Kaasuissa hiukkaset liikkuvat vapaasti ja törmäävät toisiinsa ja astian seiniin. Ominaisuuksia:
- Helposti puristettavissa; niiden tilavuus riippuu paineesta ja lämpötilasta (ideaalikaasun laki antaa yksinkertaisen mallin).
- Kaasujen diffuusio eli sekoittuminen tapahtuu nopeasti verrattuna nesteisiin ja kiinteisiin.
- Monet kemialliset reaktiot ilmakehässä tapahtuvat kaasufaasissa.
- Esimerkkejä: ilmassa esiintyvät kaasut (typpi, happi), höyryt (veden höyry), vety.
Plasma
Plasma on ionisoitunut kaasu, jota esiintyy luonnossa ja teknologisissa sovelluksissa:
- Plasman hiukkaset (ionit ja elektronit) reagoivat voimakkaasti sähkö- ja magneettikenttiin.
- Plasma johtaa sähköä hyvin ja voi emittoida valoa (esim. revontulet, liekit, aurinko ja tähdet).
- Sovelluksia: neonvalot, kaasupurkauspohjaiset lamput, fuusioreaktorit (tutkimus), plasmaleikkurit.
- Plasma voi syntyä korkeassa lämpötilassa tai voimakkaan sähkökentän vaikutuksesta (esim. salamoinnissa).
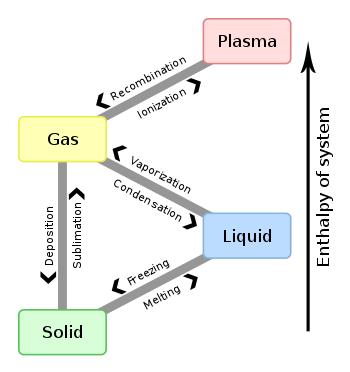
Olomuodon muutokset (faseihin liittyvät siirtymät)
Aine voi muuttua olomuodosta toiseen lämpötilan ja paineen muuttuessa. Tärkeimmät siirtymät:
- Sulatuminen (kiinteä → neste) ja jäähtyminen/kiinteytyminen (neste → kiinteä).
- Haihtuminen/keiminen (neste → kaasu) ja tiivistyminen (kaasu → neste).
- Sublimaatio (kiinteä → kaasu) ja kondensoituminen suoraan (kaasu → kiinteä).
- Ionisaatio (kaasu → plasma) ja rekombinaatio (plasma → kaasu).
Lisäksi on erityisiä pisteitä kuten kolmoispiste (kolme olomuotoa tasapainossa) ja kriittinen piste (jälkeen neste ja kaasu eivät erotu selvästi; syntyy superkrittinen fluidi).
Mittaaminen ja makroskooppiset ominaisuudet
Olomuotoihin liittyviä mitattavia suureita:
- Tiheys: massa tilavuusyksikköä kohti; yleensä kiinteissä suurin, kaasuissa pienin.
- Viskositeetti: nesteiden ja kaasujen virtausvastus.
- Lämpökapasiteetti ja lämmönjohtavuus: miten aine varastoi ja siirtää lämpöä.
- Kompressibiliteetti: kuinka helposti tilavuus muuttuu paineen vaikutuksesta.
Erikoistapaukset ja muut faasit
Neljän perusfaasin lisäksi tutkitaan useita erikoistapauksia:
- Superkriittinen fluidi: yli kriittisen lämpötilan ja paineen aine ei erotu nesteeksi ja kaasuksi — sillä on sekä tiheyden että diffuusiivisuuden ominaisuuksia.
- Bose–Einstein-kondensaatio: hyvin matalissa lämpötiloissa tietyt kvanttimekaaniset ilmiöt johtavat uuteen kollektiiviseen olomuotoon (pienissä määrin laboratoriossa).
- Puristunut aine/degeneroitunut aine: erittäin tiheät tilat (kuten valkoiset kääpiöt tai neutronitähdet) joissa kvanttimekaaniset paineilmiöt ovat merkityksellisiä.
Missä olomuodot esiintyvät ja miksi ne ovat tärkeitä
Olomuodot ovat läsnä jokapäiväisessä elämässä ja teknologiassa:
- Vesi esiintyy luonnossa kiinteänä (jää), nesteenä (järvet, meri) ja kaasuna (vesihöyry ilmakehässä) — tämä tekee veden olomuodonmuutoksista keskeisiä sää- ja ilmastoprosesseissa.
- Plasmat muodostavat tähtien ytimet ja auringon koronat sekä teknologiset laitteet kuten plasma- ja kaasuputkilamput.
- Materiaali- ja prosessi-insinöörit hyödyntävät olomuotojen tuntemusta valmistuksessa (valssaaminen, sulatus, höyrystys, phasemic processing).
Yhteenveto
Kiinteä, neste, kaasu ja plasma kuvaavat aineen yleisimpiä olomuotoja, joilla kullakin on tunnusomaiset rakenteet ja ominaisuudet. Lämpötila ja paine säätelevät olomuodon muutoksia; erityistapaukset ja eksoottiset faasit laajentavat tätä peruskuvaa. Olomuotojen ymmärtäminen on keskeistä luonnontieteissä, tekniikassa ja arkipäivän ilmiöiden selittämisessä.