Kaksi määritelmää
Pintajännitys, jota edustaa symboli γ, määritellään voimana pitkin yksikköpituista viivaa, jossa voima on pinnan suuntainen mutta kohtisuorassa viivaan nähden. Yksi tapa kuvitella tämä on kuvitella litteä saippuakalvo, jota rajoittaa toiselta puolelta kireä lanka, jonka pituus on L. Lankaa vetää kalvon sisäpuolelle voima, joka on yhtä suuri kuin 2 γ γ \displaystyle \scriptstyle \gamma }.  L (kerroin 2 johtuu siitä, että saippuakalvolla on kaksi sivua ja siten kaksi pintaa). Pintajännitys mitataan siis voimina pituusyksikköä kohti. Sen SI-yksikkö on newton per metri, mutta käytetään myös cgs-yksikköä dyne per cm. Yksi dyn/cm vastaa 0,001 N/m.
L (kerroin 2 johtuu siitä, että saippuakalvolla on kaksi sivua ja siten kaksi pintaa). Pintajännitys mitataan siis voimina pituusyksikköä kohti. Sen SI-yksikkö on newton per metri, mutta käytetään myös cgs-yksikköä dyne per cm. Yksi dyn/cm vastaa 0,001 N/m.
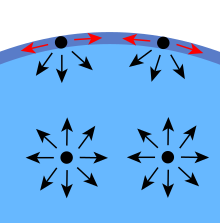
Vastaava määritelmä, joka on käyttökelpoinen termodynamiikassa, on pinta-alayksikköä kohti tehty työ. Jotta nestemassan pinta-ala kasvaisi määrällä δA, on siis tehtävä työmäärä γ, \displaystyle \scriptstyle \gamma }.  δA, tarvitaan. Tämä työ varastoidaan potentiaalienergiana. Näin ollen pintajännitys voidaan mitata myös SI-järjestelmässä jouleina neliömetriä kohti ja cgs-järjestelmässä ergsina cm:ä kohti2 . Koska mekaaniset järjestelmät pyrkivät löytämään tilan, jossa potentiaalienergia on mahdollisimman pieni, vapaa nestepisara on luonnollisesti pallon muotoinen, jolloin sen pinta-ala on mahdollisimman pieni tietyllä tilavuudella.
δA, tarvitaan. Tämä työ varastoidaan potentiaalienergiana. Näin ollen pintajännitys voidaan mitata myös SI-järjestelmässä jouleina neliömetriä kohti ja cgs-järjestelmässä ergsina cm:ä kohti2 . Koska mekaaniset järjestelmät pyrkivät löytämään tilan, jossa potentiaalienergia on mahdollisimman pieni, vapaa nestepisara on luonnollisesti pallon muotoinen, jolloin sen pinta-ala on mahdollisimman pieni tietyllä tilavuudella.
Pinta-alayksikköä kohti mitatun energian ja pituusyksikköä kohti mitatun voiman vastaavuus voidaan osoittaa dimensioanalyysin avulla.
Pinnan kaarevuus ja paine
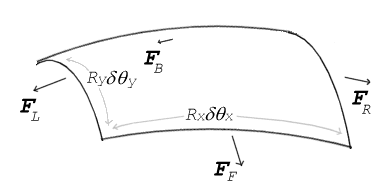
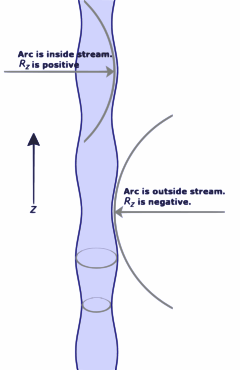
Jos jännitettyyn pintaan ei kohdistu normaalivoimaa, pinnan on pysyttävä tasaisena. Mutta jos pinnan toisella puolella oleva paine eroaa toisella puolella olevasta paineesta, paine-ero kertaa pinta-ala johtaa normaalivoimaan. Jotta pintajännitysvoimat kumoaisivat paineen aiheuttaman voiman, pinnan on oltava kaareva. Kaaviosta nähdään, miten pienen pintalaikan pinnan kaarevuus johtaa laikan keskipisteeseen nähden normaalisti vaikuttavien pintajännitysvoimien nettokomponenttiin. Kun kaikki voimat ovat tasapainossa, saadaan Young-Laplacen yhtälö:
Δ p = γ ( 1 R x + 1 R y ) {\displaystyle \Delta p\ =\ \ \gamma \left({\frac {1}{R_{x}}+{\frac {1}{R_{y}}}\right)} 
missä:
· Δp on paine-ero.
· γ \displaystyle \scriptstyle \gamma } on pintajännitys.
on pintajännitys.
· Rx ja Ry ovat kaarevuussäteitä kummallakin pinnan suuntaisella akselilla.
Oikealla puolella suluissa oleva suure on itse asiassa (kaksi kertaa) pinnan keskimääräinen kaarevuus (riippuen normalisoinnista).
Tämän yhtälön ratkaisut määräävät vesipisaroiden, lätäköiden, meniskien, saippuakuplien ja kaikkien muiden pintajännityksen määräämien muotojen muodon. (Toinen esimerkki on niiden jälkien muoto, jotka vesijuoksijan jalat jättävät lammen pintaan).
Alla olevasta taulukosta käy ilmi, miten vesipisaran sisäinen paine kasvaa säteen pienentyessä. Ei kovin pienillä pisaroilla vaikutus on hienovarainen, mutta paine-ero kasvaa valtavaksi, kun pisarakoko lähestyy molekyylikokoa. (Yksittäisen molekyylin rajoissa käsite muuttuu merkityksettömäksi).
| Δp eri säteiden vesipisaroille STP:ssä |
| Pisaran säde | 1 mm | 0,1 mm | 1 μm | 10 nm |
| Δp (atm) | 0.0014 | 0.0144 | 1.436 | 143.6 |
Nesteen pinta
On vaikea löytää jonkin mielivaltaisen muotoisen kehyksen rajaaman minimipinnan muotoa pelkällä matematiikalla. Jos kehys muotoillaan rautalangasta ja kastetaan saippualiuokseen, paikallisesti minimaalinen pinta ilmestyy saippuakalvoon muutamassa sekunnissa.
Tämä johtuu siitä, että paine-ero nesteen rajapinnan yli on verrannollinen keskimääräiseen kaarevuuteen, kuten Youngin ja Laplacen yhtälöstä käy ilmi. Avoimessa saippuakalvossa paine-ero on nolla, joten keskimääräinen kaarevuus on nolla, ja minimaalisilla pinnoilla on nollakeskikarheus.
Kontaktikulmat
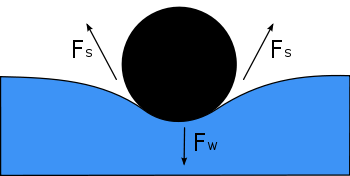
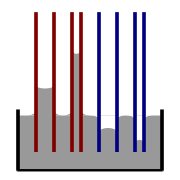
Minkä tahansa nesteen pinta on nesteen ja jonkin muun väliaineen välinen rajapinta. Esimerkiksi lammen yläpinta on lammen veden ja ilman välinen rajapinta. Pintajännitys ei siis ole pelkästään nesteen ominaisuus, vaan nesteen ja toisen väliaineen rajapinnan ominaisuus. Jos neste on säiliössä, nesteen ja ilman rajapinnan lisäksi sen yläpinnalla on myös nesteen ja säiliön seinämien välinen rajapinta. Nesteen ja ilman välinen pintajännitys on yleensä erilainen (suurempi) kuin nesteen pintajännitys astian seinien kanssa. Kun nämä kaksi pintaa kohtaavat, geometria tasapainottaa kaikki voimat.
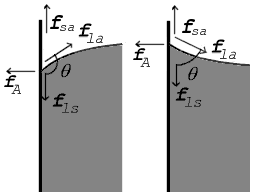
Kahden pinnan kohdatessa ne muodostavat kosketuskulman θ {\displaystyle \scriptstyle \theta }.  , joka on kulma, jonka pinnan tangentti muodostaa kiinteän pinnan kanssa. Oikealla olevassa kaaviossa on kaksi esimerkkiä. Jännitysvoimat on esitetty neste-ilman rajapinnan, neste-kiinteän aineen rajapinnan ja kiinteän aineen-ilman rajapinnan osalta. Vasemmanpuoleisessa esimerkissä nesteen ja kiinteän aineen sekä kiinteän aineen ja ilman välisen pintajännityksen erotus, γ l s - γ s a {\displaystyle \scriptstyle \gamma _{\mathrm {ls} \gamma _{\mathrm {sa}-\gamma _{\mathrm {sa} }}
, joka on kulma, jonka pinnan tangentti muodostaa kiinteän pinnan kanssa. Oikealla olevassa kaaviossa on kaksi esimerkkiä. Jännitysvoimat on esitetty neste-ilman rajapinnan, neste-kiinteän aineen rajapinnan ja kiinteän aineen-ilman rajapinnan osalta. Vasemmanpuoleisessa esimerkissä nesteen ja kiinteän aineen sekä kiinteän aineen ja ilman välisen pintajännityksen erotus, γ l s - γ s a {\displaystyle \scriptstyle \gamma _{\mathrm {ls} \gamma _{\mathrm {sa}-\gamma _{\mathrm {sa} }}  on pienempi kuin neste-ilman pintajännitys, γ l a {\displaystyle \scriptstyle \gamma _{\mathrm {la}} }}
on pienempi kuin neste-ilman pintajännitys, γ l a {\displaystyle \scriptstyle \gamma _{\mathrm {la}} }}  , mutta on silti positiivinen, eli
, mutta on silti positiivinen, eli
γ l a > γ l s - γ s a > 0 {\displaystyle \gamma _{\mathrm {la} \ > \ \gamma _{\mathrm {ls} }-\gamma _{\mathrm {sa} }\ >\ 0} 
Kaaviossa sekä pysty- että vaakasuuntaisten voimien on kumoututtava täsmälleen kosketuspisteessä, jota kutsutaan tasapainotilaksi. Vaakakomponentti f l a {\displaystyle \scriptstyle f_{\mathrm {la} }} kumoutuu adheesiovoimalla f A {\displaystyle \scriptstyle f_{\mathrm {A} }}
kumoutuu adheesiovoimalla f A {\displaystyle \scriptstyle f_{\mathrm {A} }}  .
.
f A = f l a sin θ {\displaystyle f_\mathrm {A} \ =\ f_{\mathrm {la} \sin \theta } 
Tärkeämpi voimatasapaino on kuitenkin pystysuunnassa. Pystysuora komponentti f l a {\displaystyle \scriptstyle f_{\mathrm {la} }} on täsmälleen kumottava voima f l s {\displaystyle \scriptstyle f_{\mathrm {ls}} }}
on täsmälleen kumottava voima f l s {\displaystyle \scriptstyle f_{\mathrm {ls}} }}  .
.
f l s - f s a = - f l a cos θ {\displaystyle f_{\mathrm {ls} }-f_{\mathrm {sa} {\ =\ -f_{\mathrm {la} =\ -f_mathrm {la} \cos \theta } 
| Neste | Solid | Kosketuskulma |
| vesi | | limettisoodalasi | | lyijylasia | | sulatettu kvartsi | | 0° |
| etanoli |
| dietyylieetteri |
| hiilitetrakloridi |
| glyseroli |
| etikkahappo |
| vesi | parafiini | 107° |
| hopea | 90° |
| metyylijodidi | limettisoodalasi | 29° |
| lyijylasia | 30° |
| sulatettu kvartsi | 33° |
| elohopea | limettisoodalasi | 140° |
| Eräät nesteen ja kiinteän aineen kosketuskulmat |
Koska voimat ovat suoraan verrannollisia niiden pintajännityksiin, on myös:
γ l s - γ s a = - γ l a cos θ \displaystyle \gamma _{\mathrm {ls} }-\gamma _{\mathrm {sa} }\ =\ -\gamma _{\mathrm {la} \cos \theta } 
jossa
· γ l s {\displaystyle \scriptstyle \gamma _{\mathrm {ls} }} on nesteen ja kiinteän aineen välinen pintajännitys,
on nesteen ja kiinteän aineen välinen pintajännitys,
· γ l a \displaystyle \scriptstyle \gamma _{\mathrm {la} }} on neste-ilman pintajännitys,
on neste-ilman pintajännitys,
· γ s a \displaystyle \scriptstyle \gamma _{\mathrm {sa} }} on kiinteän aineen ja ilman välinen pintajännitys,
on kiinteän aineen ja ilman välinen pintajännitys,
· θ {\displaystyle \scriptstyle \theta } on kosketuskulma, jossa koveran meniskin kosketuskulma on alle 90° ja kuperan meniskin kosketuskulma on yli 90°.
on kosketuskulma, jossa koveran meniskin kosketuskulma on alle 90° ja kuperan meniskin kosketuskulma on yli 90°.
Tämä tarkoittaa sitä, että vaikka neste-kiinteän aineen ja kiinteän aineen ja ilman pintajännityksen erotus, γ l s - γ s a {\displaystyle \scriptstyle \gamma _{\mathrm {ls} }-\gamma _{\mathrm {sa} }}  on vaikea mitata suoraan, mutta se voidaan päätellä neste-ilman pintajännityksestä γ l a {\displaystyle \scriptstyle \gamma _{\mathrm {la} }}
on vaikea mitata suoraan, mutta se voidaan päätellä neste-ilman pintajännityksestä γ l a {\displaystyle \scriptstyle \gamma _{\mathrm {la} }}  ja tasapainokontaktikulmasta, θ {\displaystyle \scriptstyle \theta }
ja tasapainokontaktikulmasta, θ {\displaystyle \scriptstyle \theta }  , joka on helposti mitattavissa olevien etenevien ja väistyvien kosketuskulmien funktio (ks. pääartikkeli kosketuskulma).
, joka on helposti mitattavissa olevien etenevien ja väistyvien kosketuskulmien funktio (ks. pääartikkeli kosketuskulma).
Sama suhde on olemassa oikealla olevassa kaaviossa. Tässä tapauksessa nähdään kuitenkin, että koska kosketuskulma on pienempi kuin 90°, nesteen, kiinteän aineen ja kiinteän aineen ja ilman välisen pintajännityseron on oltava negatiivinen:
γ l a > 0 > γ l s - γ s a {\displaystyle \gamma _{\mathrm {la} \ >\ 0\ >\ \gamma _{\mathrm {ls} \gamma _{\mathrm {sa}-\gamma _{\mathrm {sa} }} 
Erityiset kosketuskulmat
Huomaa, että erityistapauksessa veden ja hopean rajapinnassa, jossa kosketuskulma on 90°, nesteen, kiinteän aineen ja kiinteän aineen ja ilman välinen pintajännitysero on täsmälleen nolla.
Toinen erikoistapaus on, kun kosketuskulma on täsmälleen 180°. Erityisvalmisteisen teflonin sisältämä vesi lähestyy tätä. Kosketuskulma on 180°, kun nesteen ja kiinteän aineen välinen pintajännitys on täsmälleen yhtä suuri kuin neste-ilman välinen pintajännitys.
γ l a = γ l s - γ s a > 0 θ = 180 ∘ \displaystyle \gamma _{\mathrm {la} \ =\ \ \gamma _\mathrm {ls} }-\gamma _{\mathrm {sa} \ >\ 0\qquad \theta \ =\ 180^{\circ }} 















































.jpg)