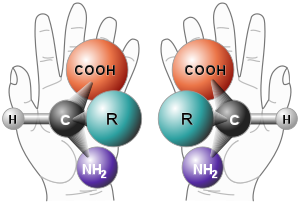
Kiraalisuus tarkoittaa, että esineellä tai rakenteella on kaksi muotoa, jotka ovat toistensa peilikuvia mutta joita ei voi asettaa päällekkäin siten, että ne sopisivat täydellisesti yhteen. Tällaisia muotoja kutsutaan enantiomeereiksi. Yksinkertainen arkipäiväinen esimerkki on ihmisen kädet: vasen käsi on oikean käden peilikuva, mutta et voi kääntää tai siirtää toista niin, että se näyttäisi täsmälleen samalta kuin toinen.
Kädet ja arkitodellisuus
Vasemman ja oikean käden ero auttaa ymmärtämään kiraalisuuden perusajatuksen käytännössä: esine voi näyttää samalta monesta kulmasta, mutta peilikuva ei ole superimponoituva (eli päällekkäin sovitettava) alkuperäisen kanssa. Tästä johtuu esimerkiksi se, että et voi laittaa vasemman käden hanskaa oikeaan käteesi tai kätellä henkilön oikeaa kättä käyttäen vasenta kättäsi ilman, että kädet olisivat eri asennossa.
Kiraalisuus kemiassa
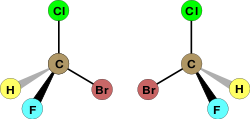
Monet orgaaniset molekyylit ovat kiraalisia. Tavallisin syy on hiiliatomi, johon on sitoutunut neljä eri ryhmää: tällainen atomi on stereokeskus eli chirality center. Kun molekyylillä on stereokeskus, se voi esiintyä kahden eri enantiomeerin muodossa (kutsutaan usein R- ja S-muodoiksi Cahn–Ingold–Prelog -sääntöjen mukaisesti).
Enantiomeerien fysikaaliset ominaisuudet (sulamis- ja kiehumispisteet, tiheys) ovat yleensä samankaltaisia, mutta ne eroavat siinä, miten ne kääntävät polarisoitua valoa (optinen aktiivisuus) ja miten ne reagoivat muiden kiraalisten järjestelmien, kuten biologisten entsyymien tai reseptorien, kanssa.
Miksi kiraalisuus on tärkeää?
- Biologiassa ja lääketieteessä enantiomeerit voivat vaikuttaa eri tavoin: toinen muoto voi olla aktiivinen lääkeainetta, toinen tehoton tai jopa haitallinen. Tunnettu esimerkki on thalidomidi, jonka eri enantiomeereillä oli eri vaikutuksia; käytännössä aine kuitenkin racemoituu elimistössä, joten ongelma ei ratkennut vain myymällä yhtä isomeeriä.
- Elintarvikkeet, hajusteet ja mausteet: monen aineen tuoksu tai maku riippuu siitä, kumpi enantiomeeri on läsnä.
- Teollisuus ja synteesi: monissa kemiallisissa prosesseissa pyritään tuottamaan tietty enantiomeeri (asymmetrinen synteesi) tai erottamaan pari (chiral resolution), koska molekyylin toiminta voi riippua siitä.
Miten kiraalisuutta havaitaan ja erotellaan?
Yleisimpiä menetelmiä ovat:
- Polarimetria: mitataan, kääntääkö ja kuinka paljon näyte polarisoidun valon tasoa.
- Kemiallinen resoluutio: muodostetaan diastereomeerejä (joilla on erilaiset fysikaaliset ominaisuudet) ja erotellaan ne, sitten palautetaan enantiomeerit.
- HPLC tai muut kromatografiset menetelmät käyttäen kiralista staattista faasia, joka erottaa enantiomeerit.
- Spektrimenetelmät ja röntgenkristallografia voivat näyttää molekyylin avaruudellisen rakenteen ja siten kiraalisuuden.
Muita kiraalisuuden muotoja ja esimerkkejä
- Arkisia esineitä: pariton kenkäpari, ruuvit (yleensä oikeakätisiä kierteitä), käsineet ja sakset voivat olla kiraalisia.
- Luonnossa esiintyy moni biologinen molekyyli vain yhtenä enantiomeerinä — esimerkiksi aminohapot ovat pääasiassa L-muodossa ja sokereista monet D-muodossa.
- Kiraalisuus voi esiintyä myös ilman selviä stereokeskuksia: esimerkiksi aksiaalinen kiraalisuus (kuten biaryylirakenteissa) ja planarinen kiraalisuus.
Yhteenveto
Kiraalisuus on laaja ilmiö, joka koskee sekä arkisia esineitä että molekyylejä. Sen ydinasia on, että kaksi peilikuvamuotoa eivät ole superimponoituvia. Tämä vaikuttaa käytännössä siihen, miten aineet reagoivat ja toimivat, erityisesti biologisissa järjestelmissä ja lääkekehityksessä. Pienillä avaruudellisilla eroilla voi olla suuria vaikutuksia, joten kiraalisuuden ymmärtäminen ja hallinta on monella alalla tärkeää.