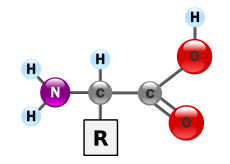
Aminohapot ovat proteiinien rakennusaineita. Eukaryooteissa on 20 tavallista aminohappoa, joista lähes kaikki proteiinit koostuvat.
Biokemiassa aminohappo on mikä tahansa molekyyli, jossa on sekä amiini- (NH2+R) että karboksyyliryhmiä (C=O). Biokemiassa tämä termi viittaa alfa-aminohappoihin, joiden yleinen kaava on H2NCHRCOOH, jossa R on yksi monista sivuryhmistä (ks. kaavio). Alfa-aminohapossa amiini- ja karboksyyliryhmät ovat kiinnittyneinä samaan hiileen (alfa-hiileen), minkä vuoksi ne muodostavat rakennuspalikan proteiinisynteesissä.
Monimuotoisuus ja luokittelu
Aminohappoja tunnetaan luonnossa noin 500, mutta ihmisessä ja useimmissa muissa organismeissa proteiinien muodostukseen käytetään tavallisimmin samoja 20 kanonista aminohappoa. Nämä 20 voidaan jakaa luokkiin kemiallisten ominaisuuksien mukaan, esimerkiksi:
- Ei-polaariset (hydrofobiset) — esim. alaniini, valiini, leusiini, isoleusiini, fenyylialaniini, metioniini, proliini
- Polaariset, varauksettomat — esim. seriini, treoniini, aspariagiini, glutamiini, tyrosiini
- Happamat (negatiivisesti varautuneet) — aspartaatti, glutamaatti
- Emäksiset (positiivisesti varautuneet) — lysiini, arginiini, histidiini
- Aromaatit ja rikkiä sisältävät — fenyylialaniini, tyrosiini, tryptofaani, metioniini, kysteiini
Proteiinien rakenne ja toiminta
Aminohapot yhdistyvät peptidisidoksin muodostaen pitkiä ketjuja eli polypeptidejä. Proteiinin toiminta perustuu sen kolmija neljäänulotteiseen rakenteeseen: primaarirakenne (järjestys), sekundaarirakenne (alpha-kierrokset ja beeta-laskokset), tertiäärirakenne (kolmiulotteinen muoto) ja kvaternäärirakenne (useamman alayksikön muodostama rakenne). Pieni muutos yksittäisessä aminohapossa voi muuttaa koko proteiinin muodon ja toiminnan — tästä esimerkkinä perinnölliset sairaudet, joissa mutaatiot johtavat väärin toimiviin proteiineihin.
Välttämättömät ja ehdollisesti välttämättömät aminohapot
Ihmiselle yhdeksän 20:stä tavanomaisesta aminohaposta on välttämättömiä, eli elimistö ei osaa syntetisoida niitä riittävästi ja ne on saatava ravinnosta. Nämä yhdeksän ovat:
- histidiini
- isoleusiini
- leusiini
- lysiini
- metioniini
- fenyylialaniini
- treoniini
- tryptofaani
- valiini
Lisäksi jotkut aminohapot ovat ehdollisesti välttämättömiä tietyissä tilanteissa, kuten kasvussa, sairaudessa tai kajoavassa aineenvaihdunnan tilassa. Esimerkiksi arginiini voi olla välttämätön imeväisillä ja taudin aikana, ja kysteiini sekä tyrosiini voidaan syntetisoida muista aminohapoista mutta ne saattavat olla puutteellisia tietyissä olosuhteissa.
Ravinto, proteiinin laatu ja eri lähteet
Eläinperäiset proteiinit (liha, kala, maitotuotteet, kananmunat) sisältävät yleensä kaikki välttämättömät aminohapot täydellisinä yhdistelminä. Kasvipohjaiset proteiinit voivat joissain tapauksissa olla puutteellisempia yhdessä tai useammassa välttämättömässä aminohapossa, mutta eri kasviproteiineja yhdistämällä (esim. viljat + palkokasvit) saa usein kattavan aminohappoprofiilin. Tämän vuoksi monipuolinen kasvisruokavalio voi kattaa kaikki välttämättömät aminohapot ilman eläintuotteita.
Kasvinsyöjien kohdalla ravinnon koostumus on erityisen tärkeä, ja märehtijöillä, kuten lehmillä, osa aminohapoista muodostetaan ruoansulatuskanavan mikrobi-elinympäristössä (mikrobien avulla) ennen kuin ne imeytyvät isäntäeläimen käyttöön.
Terveydellinen merkitys ja lääketieteelliset näkökohdat
Aminohapoilla on useita elintärkeitä tehtäviä elimistössä:
- rakentavat proteiineja ja kudoksia, ylläpitävät lihasmassaa
- toimivat esiasteina hormonien ja välittäjäaineiden synteesissä (esim. tyrosiinista syntyvät kilpirauhashormonit ja dopamiini, tryptofaanista serotoniini)
- osallistuvat aineenvaihduntaan ja energian tuottoon (esimerkiksi keto- ja glukogeeniset aminohapot)
- toimivat entsyymien ja kuljetusproteiinien osina
- osallistuvat immuunijärjestelmän toimintaan ja haavojen paranemiseen
Lisäksi monet biologisesti aktiiviset yhdisteet ovat aminohappojohdannaisia: esimerkiksi typpioksidi syntetisoidaan arginiinista, kreatiini syntetisoidaan glysiinistä ja arginiinista, ja glutationi on tripeptidi, joka sisältää kysteeniä ja toimii solujen tärkeänä antioksidanttina.
Sairauksien näkökulmasta on olemassa aminohappoaineenvaihdunnan perinnöllisiä häiriöitä, kuten fenyliketonuria (PKU), jossa fenyylialaniinin metabolia on häiriintynyt ja jonka seurauksena fenyylialaniini kertyy elimistöön aiheuttaen hermostollisia ongelmia ilman hoitoa. Myös haaraketjuisten aminohappojen aineenvaihdunnan häiriöt (BCKD-taudit) ovat kliinisesti merkittäviä.
Aminohappolisät ja ruokavalion vaikutukset
Aminohappolisiä (esim. haaraketjuiset aminohapot BCAA:t eli leusiini, isoleusiini, valiini) käytetään urheilussa lihasmassan ja palautumisen tukena. Useimmille terveille ihmisille monipuolinen ruokavalio kattaa tarvittavat aminohapot, mutta lisien käytössä tulee huomioida annostus ja mahdolliset yhteisvaikutukset lääkkeiden kanssa. Erityisesti munuaissairauksissa tai aineenvaihdunnan poikkeavuuksissa suuria aminohappo- tai proteiinimäärien muutoksia tulee välttää ja hoitaa lääkärin ohjeistuksella.
Yhteenvetona: aminohapot ovat monipuolisia ja välttämättömiä molekyylejä, jotka muodostavat proteiinit, toimivat monien tärkeiden biologisten yhdisteiden lähtöaineina ja vaikuttavat ravitsemukseen sekä terveyteen eri tavoin. Tasapainoinen ja monipuolinen ruokavalio takaa yleensä riittävän aminohappojen saannin, mutta erityisolosuhteissa (kasvukaudet, sairaudet, ruokavaliorajoitukset) tarkempi seuranta voi olla tarpeen.