CRISPR on termi DNA-tutkimuksessa. Se on lyhenne sanoista clustered regularly-interspaced short palindromic repeats. Nämä ovat osa prokaryoottien geneettistä koodia: useimmilla bakteereilla ja arkeologeilla on niitä. CRISPR toimii näiden mikro-organismien puolustautumiskeinona virusten eli bakteriofagien hyökkäyksiä vastaan. Sen rakenne ja toiminta alettiin tunnistaa 2000-luvulla, ja 2010-luvulla CRISPR-järjestelmän muokkaamisesta tuli perustavanlaatuinen työkalu geenitekniikkaan.
Mikä CRISPR on käytännössä?
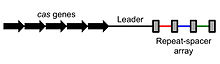
CRISPR-locus koostuu peräkkäisistä toistuvista DNA-sekvensseistä ja niiden väleissä olevista lyhyistä “spacereista”, jotka ovat peräisin aiemmista virustartunnoista. Spacerit toimivat eräänlaisena muistina: ne kertovat, millaisia vieraita DNA-paloja solun tulee tunnistaa. Spacereita ja toistuvia sekvenssejä ympäröivät usein cas-geenit, jotka koodaavat CRISPR-järjestelmän toiminnalle välttämättömiä proteiineja, kuten Cas9-entsyymiä.
Miten CRISPR suojaa bakteereja — kolme päävaihetta
- Adaptaatio (tunnistus ja näytteenotto): Kun bakteriootti altistuu uudelle virukselle, se voi tallentaa osan viruksen DNA:sta spaceriksi CRISPR-locusiin.
- Ilmentyminen ja prosessointi: CRISPR-locus transkriptoidaan RNA-molekyyleiksi, jotka leikataan lyhyiksi crRNA-janiksi. Näihin voi liittyä myös muita RNA-komponentteja (esim. tracrRNA), jotka muodostavat yhdessä ladatun opas-RNA:n.
- Interferenssi (tapahtuman estäminen): crRNA opastaa Cas-proteiinin tunnistamaan ja leikkaamaan vastaavaa vieraan DNA- tai RNA-sekvenssiä. Leikkaus voi katkaista viruksen perimän ja estää infektion etenemisen.
CRISPR-tyypit ja Cas-proteiinit
On olemassa erilaisia CRISPR-järjestelmiä (luokiteltu useisiin tyyppeihin), joiden avainproteiinit eroavat. Tunnetuimpia ovat:
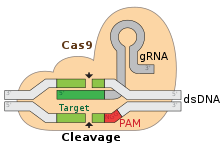
- Cas9 (esim. Streptococcus pyogenes Cas9): leikkaa kaksijuosteista DNA:ta opas-RNA:n avulla. Edellyttää usein viereistä lyhyttä tunnussekvenssiä (PAM), jotta leikkaus tapahtuu oikeassa kohdassa.
- Cas12: myös DNA:ta kohdistava mutta käyttäytyy eri tavalla ja voi tuottaa yksijuosteista leikkausta sekä indusoida laajempaa DNA-hajoitusta in vitro.
- Cas13: tunnistaa ja pilkkoo RNA:ta, ja sitä käytetään mm. virus-RNA:n havaitsemiseen ja mahdollisesti sen estämiseen.
CRISPR geenieditoinnissa
CRISPR–Cas9-järjestelmästä tuli nopeasti tutkimusyhteisön suosituin työkalu, koska se on suhteellisen yksinkertainen, tehokas ja helposti ohjattavissa muuttamalla opas-RNA:n sekvenssiä. Perusperiaate geenieditoinnissa on seuraava:
- opas-RNA ohjaa Cas-entsyymiä haluttuun kohtaan genomissa,
- Cas-entsyymi leikkaa DNA:n,
- solun oma korjausjärjestelmä joko liittää rikkoutuneen kohdan yhteen (usein aiheuttaen insertioita tai deletointeja) tai, kun tarjotaan korjauseksonia, mahdollistaa tarkemman geenin korjauksen tai lisäyksen.
Sovellukset
- Perustutkimus: nopeasti ja tehokkaasti tehtävät geenin “poistot” tai merkkaukset auttavat selvittämään geenien toimintoja.
- Lääketiede: geeniterapia, jossa pyritään korjaamaan tai estämään sairautta aiheuttavia mutaatioita — sekä kantasolutason että somaalisen hoidon tutkimukset etenevät.
- Maatalous: kasvien ja eläinten ominaisuuksien parantaminen, tautiresistenssin lisääminen ja tuottavuuden kehittäminen (geenimuuntelu ja muut menetelmät).
- Diagnostiikka: CRISPR-pohjaisia testejä kehitetään nopeaan ja herkään tautien tunnistukseen (esim. SHERLOCK ja DETECTR -menetelmät).
- Biotekniikka ja teollisuus: mikrobien muokkaus tuotantomäärien ja uusien biotuotteiden synteesin tehostamiseksi.
- Mahdollinen virusvastainen käyttö: tutkimuksessa selvitetään myös, miten CRISPR-pohjaisia lähestymistapoja voisi käyttää virusten torjuntaan ihmisissä.
Rajoitukset, riskit ja eettiset kysymykset
Vaikka CRISPR on voimakas työkalu, sillä on rajoituksia ja riskejä:
- Off-target»-vaikutukset: Cas-entsyymi voi toisinaan leikata myös ei-toivotuissa paikoissa genomissa, mikä voi aiheuttaa haitallisia muutoksia.
- Toimitusongelmat: turvallinen ja tehokas tapa toimittaa CRISPR-komponentit oikeisiin soluihin tai kudoksiin (esim. virusvektoreilla, lipidinanopartikkeleilla) on keskeinen haaste.
- Immuneettiset vasteet: ihmisillä voi olla ennestään immuunivaste Cas-proteiinien kantajabakteereita vastaan.
- Eettiset kysymykset: erityisesti periytyvien (germline) muokkausten tekeminen herättää vakavia eettisiä ja yhteiskunnallisia kysymyksiä, ja monissa maissa niitä rajoitetaan tai kiellettään.
Lyhyt historia ja tulevaisuus
CRISPR-järjestelmän biologista merkitystä alettiin ymmärtää 2000-luvun alkupuolella, ja 2012–2013 tutkijat osoittivat, että CRISPR–Cas9:ää voidaan käyttää täsmälliseen geenieditoimiseen eukaryoottisoluissa. Tutkijat Emmanuelle Charpentier ja Jennifer Doudna saivat tästä työstä Nobel-palkinnon kemiassa vuonna 2020. Nykyään tutkimus keskittyy turvallisuuden parantamiseen, uusiin Cas-variantoihin, RNA-kohteisiin ratkaisuihin ja kliinisiin sovelluksiin.
Yhteenveto
CRISPR on luonnollinen bakteerien ja arkeonien puolustusjärjestelmä, joka on muuttunut vallankumoukselliseksi työkaluksi geenieditoinnissa. Sen sovellukset ulottuvat perustutkimuksesta lääketieteeseen, maatalouteen ja diagnostiikkaan. Samalla se herättää tärkeitä teknisiä, turvallisuus- ja eettisiä kysymyksiä, jotka vaativat huolellista arviointia jatkokehityksen aikana.