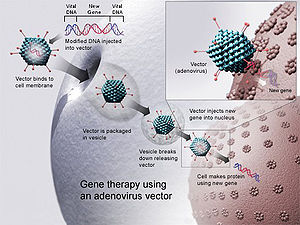
Geeniterapia tarkoittaa toimivan geenin syöttämistä henkilölle, jolla on vaurioitunut geeni. Euroopan komissio on hyväksynyt tämän menetelmän yhtä tiettyä hoitoa varten. Glybera-tuotteen hoidossa käytetään virusta, jolla lihassolut infektoidaan toimivalla geenikopiolla. Euroopan komissio on antanut Glyberalle myyntiluvan, mikä tarkoittaa, että sitä voidaan myydä koko EU:n alueella.
Geeniterapian tavoitteena on korvata, lisätä tai muokata sairastavaa geenitoimintaa. Lääkinnällisessä käytössä puhutaan yleensä somaattisesta geeniterapiasta, jossa muutetaan potilaan elimistön soluja — toisin kuin sukusolu- tai alkion geenimuutoksissa, joita ei nykyisin sallita kliinisessä hoidossa. Geenin voi tuoda soluihin useilla eri tavoilla: suoraan paikallisin injektioin, systeemisesti verenkierrossa tai ensin solut erotellen (ex vivo) ja sitten takaisin potilaaseen.
Yhdellä miljoonasta ihmisestä on vaurioitunut kopio rasvan hajottamiseen tarvittavasta lipaasigeenistä. Rasvaa kertyy heidän vereensä, mikä johtaa kipuun ja haimatulehdukseen (haimatulehdus). Se on hengenvaarallinen. Tähän mennessä ainoa tapa hoitaa sairautta on hyvin vähärasvainen ruokavalio, ja toistuvat vaikeat haimatulehduksen jaksot voivat vaatia sairaalahoitoa. Geeniterapia on kehitetty nimenomaan vähentämään haimatulehduskohtauksia ja parantamaan lipaasin puutoksen aiheuttamaa aineenvaihduntaongelmaa.
Näin käytettynä virus on vektori. Se tarkoittaa, että se on kantaja; geeni on lisätty viruksen genomiin, ja virus siirtää sen ihmissoluihin. Glybera käytti adeno‑associated virus -tyyppiä (AAV1) lihassoluihin annettavana vektorina. AAV‑vektorit ovat usein suhteellisen turvallisia, eivät aiheuta voimakasta akuutia taudinoiretta ja yleensä säilyvät solussa episomaalisena (eli eivät integroi usein isäntägenomiin), mikä pienentää integroitumiseen liittyvää riskia.
On olemassa erilaisia virusvektoreita, joilla on omat ominaisuutensa:
- AAV (adeno-associated virus) – matala immunogeenisyys, useita serotyyppejä, käytetty monissa paikallisissa terapioissa kuten lihakseen annettaessa;
- Adenovirus – aiheuttaa voimakkaamman immuunivasteen ja usein vain tilapäisen geeniekspression;
- Lenti‑ ja retrovirukset – integroituvat isäntägenomiin, joten niitä käytetään usein ex vivo -menetelmissä (esim. kantasolut tai solut, jotka käsitellään laboratorioissa) ja pitkäaikaisen ilmentymän saavuttamiseen.
Tekniikoista käytetyt termit kannattaa erottaa: virusvektorien kautta tapahtuva geenin siirto kutsutaan yleensä transduktioksi. Sana transfektioksi käytetään yleensä ei-virusperäisestä DNA:n tai RNA:n siirrosta soluihin (esim. lipidipartikkeleilla tai sähköpulssilla). Toinen eri menetelmä on geenin inaktivointi tai korjaus (esimerkiksi työnttäminen pois toiminnasta tai CRISPR-perusteinen korjaus), ja se eroaa suoraan geenin toiminnallisen kopion lisäämisestä.
Glybera (alipogene tiparvovec) annettiin potilaille lihakseen monesta paikasta annettavina injektioina, ja käsitteenä oli kertakäyttöinen hoito, jonka tarkoitus oli tuottaa toimivaa lipaasientsyymiä paikallisesti. Kliinisissä tutkimuksissa hoito vähensi joidenkin potilaiden haimatulehdusjaksoja ja paransi rasvan aineenvaihduntaa, mutta potilasmäärät olivat pieniä, ja vaikuttavuuden laajuus vaihteli. Tuotteen korkeat kustannukset (raportoidusti noin miljoona euroa potilasta kohti), harvinaisen taudin pieni hoidon tarve ja rajallinen näyttö johtivat siihen, ettei hoitoa käytetty laajalti, ja sen markkinointi lopetettiin myöhemmin.
Geeniterapioihin liittyy riskejä ja haasteita:
- immuunivasteita — potilailla voi kehittyä vasta‑aineita vektoria vastaan tai kohdeproteiinin yliherkkyyttä;
- paikalliset reaktiot ja tulehdus injektiokohdassa;
- geeniekspression kesto voi olla rajallinen (riippuen vektorista ja kohdekudoksesta);
- integraatio‑ ja mutageenisuusriski — erityisesti integroituvien vektorien kohdalla, vaikka AAV:n integroitumisriski on yleensä matalampi;
- valmistuksen monimutkaisuus ja korkeat kustannukset.
Yleisesti ottaen geneettinen lääketiede kehittyy nopeasti: vectoritekniikkaa on parannettu, turvallisuusseuranta on tiukentunut ja uusia lähestymistapoja (kuten geenin korjaus CRISPR‑menetelmillä, parannetut vektorit ja tarkemmat kohdistusstrategiat) tutkitaan laajalti. Vaikka Glybera oli merkittävä askel harvinaiseen sairauteen suunnatussa geeniterapiassa, sen käytännön vaikutukset ja markkinointi olivat rajoitettuja, ja alan kehitys on sittemmin jatkunut monilla muilla tavoilla.