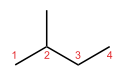Rakenteellinen isomeria (IUPAC kutsuu tätä konstitutionaaliseksi isomeriaksi) on eräänlainen isomeria. Tässä isomeriassa kahdella kemikaalilla on sama molekyylikaava, mutta molekyylit eroavat toisistaan siinä, miten atomit ovat sitoutuneet toisiinsa — eli niiden sidokset (connectivity) ovat erilaiset. Tämä ero johtaa usein merkittäviin eroihin aineiden fysikaalisissa ja kemiallisissa ominaisuuksissa. Rakenteellisen isomerian vastakohta on stereoisomeria, jossa atomien liittymisjärjestys on sama mutta avaruudellinen järjestys eroaa (esim. cis/trans- ja enantiomeerit).
Rakenteellisen isomerian päätyypit
Konstitutionaalisia isomeerejä voidaan luokitella useaan ryhmään. Yleisimmät tyypit ovat:
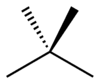
- Luurankoisomeerit (ketjusomeerit) — sama molekyylikaava mutta eri hiiliketjun rakenne: suora ketju vs haarautunut ketju. Esimerkkinä C4H10: n-butan (suora) ja 2-metyyli-propaani (isobutaani, haarautunut).
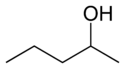
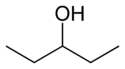
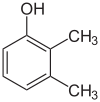
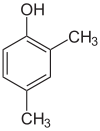
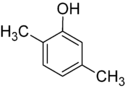
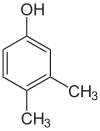
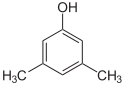
- Asemoisomeerit (positional/regioisomeerit) — funktionaalinen ryhmä tai kaksoissidos sijaitsee eri kohdassa samaa runkoa. Esimerkkejä: 1-butanoli vs 2-butanoli, tai orto-, meta- ja para-xyleenit (sameaniliini-ydin, eri asentoihin liittyneet metyyli‑ryhmät). Asemoisomeerejä kutsutaan usein myös regioisomeereiksi.
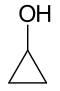
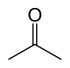
- Funktionaaliset isomeerit — molekyylikaava on sama mutta funktionaalinen ryhmä on erilainen, jolloin aineilla on eri funktionaalinen luokka. Tunnettu esimerkki on C2H6O: etanoli (alkoholi) ja dimetyylieetteri (eetteri). Toinen esimerkki C3H6O: propanali (aldehydi) ja propanoni (ketooni, asetonin).
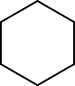
Edellä mainittujen lisäksi voidaan huomioida mm. rengas–ketju-isomeria (esim. C6H12: sykloheksaani vs heks-1-eeni) ja muita alatyyppejä, jotka perustuvat samaan ajatukseen: sama summakaava, erilainen rakenne.
Tautomeriat — erityistapa funktionaalisista isomeereistä
Tautomeria on erikoistapaus funktionaalisesta isomeriasta, jossa kaksi isomeeria liittyy toisiinsa nopeasti kemiallisten reaktioiden (yleensä protoninsiirron) avulla ja ne ovat tasapainossa keskenään. Yleisimmät tautomeriat ovat keto–enoli-tautomeria (esim. keto‑muoto vs enolimuoto). Tautomeriat eroavat usein vain protonin paikasta ja kaksoissidoksen sijainnista, mutta niillä voi olla hyvin erilainen reaktiivisuus.
Miten rakenteelliset isomeerit eroavat käytännössä?
- Fysikaaliset ominaisuudet: kiehumispisteet, sulamispisteet, tiheys ja liukoisuudet voivat poiketa paljonkin. Esimerkiksi etanoli (C2H6O, alkoholi) kiehuu noin 78 °C kun taas dimetyylieetterin kiehumispiste on noin −25 °C — sama summakaava mutta hyvin erilaiset ominaisuudet.
- Kemiallinen reaktiivisuus: funktionaalisen ryhmän tyyppi ja sijainti määräävät, millaisia reaktioita yhdiste käy läpi ja kuinka helposti. Esimerkiksi aldehydit reagoivat eri tavoilla kuin ketonit.
- Analyyttinen erottelu: rakenteelliset isomeerit voidaan erottaa ja tunnistaa mm. NMR‑, IR‑ ja massaspektrometrialla sekä kromatografisilla menetelmillä.
Yhteenveto
Rakenteellinen (konstitutionaalinen) isomeria tarkoittaa sitä, että samankokuisilla molekyyleillä on erilainen atomien sitoutumisjärjestys. Päätyyppejä ovat luurankoisomeerit, asemoisomeerit (regioisomeerit) ja funktionaaliset isomeerit; tautomeria on eräs erityistapa funktionaalisista isomeereistä. Näillä isomeereillä voi olla selvästi erottuvat fysikaaliset ja kemialliset ominaisuudet, joten niiden tunnistus ja luokittelu on tärkeää kemiallisessa tutkimuksessa ja käytännön sovelluksissa.