Kemiassa molekyyliorbitaali (tai MO) kuvaa sitä, mitä tapahtuu elektroneille, kun atomit liittyvät yhteen molekyylissä. MO on kvanttimekaaninen matemaattinen funktio, joka kuvaa elektronin aaltomaista käyttäytymistä ja jonka neliö kertoo todennäköisyyden löytää elektroni tietyltä alueelta molekyylin ympäriltä. Kemistit ja teoreettiset tutkijat käyttävät näitä funktioita ennustaakseen ja selittääkseen kemiallisia ja fysikaalisia ominaisuuksia, kuten sidosten muotoa, elektronitiheyttä, spektriä tai magneettisuutta.
Kuinka molekyyliorbitaalit muodostuvat
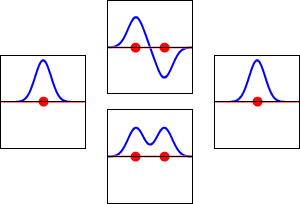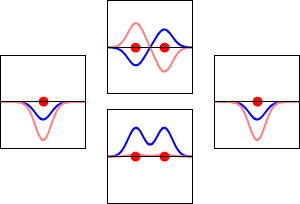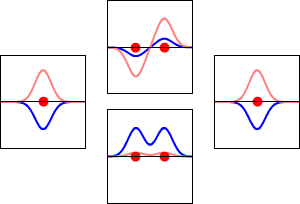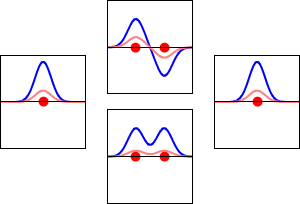
Kemistit rakentavat usein matemaattisia molekyyliorbitaalimalleja yhdistämällä atomiorbitaaleja (LCAO‑menetelmä, linear combination of atomic orbitals). Kahdesta tai useammasta atomiorbitaalista muodostuu lineaarikombinaatioita, joista osa on konstruktivisia (sidosorbitaaleja) ja osa destruktivisia (antidi‑sidosorbitaaleja). Sidosorbitaalissa aaltofunktioilla on sama etumerkki ja elektronitiheys atomeja yhdistävällä alueella kasvaa, mikä stabiloi järjestelmää. Antisidoksisessa orbitaalissa esiintyy solmuja (nodal plane), ja yhteisenergia on korkeampi.
Orbitaalien energiajärjestys määräytyy alkuperäisten atomiorbitaalien energioista ja niiden lomittumisesta (overlap). Lähempänä toisiaan olevat ja hyvin lomittuvat orbitaalit muodostavat voimakkaamman sidoksen. Myös atomien hybridiorbitaaleja tai laajempia delokalisoituneita MOita voidaan käyttää kuvaamaan monimutkaisempia järjestelmiä.
Keskeiset käsitteet ja ominaisuudet
- Sidos- ja antisiidosorbitaalit: sidosorbitaalit (bonding) alentavat järjestelmän energiaa, antisiidosorbitaalit (antibonding, merkitty usein tähti‑merkinnällä kuten σ* tai π*) nostavat sitä.
- Sigma (σ) ja pi (π) orbitallit: σ‑orbitaalit ovat symmetrisiä atomitason akselin ympäri, π‑orbitaalit syntyvät sivittaisten päällekkäisyyksien kautta ja voivat johtaa delokalisoituneisiin π‑järjestelmiin (esim. alkeenit, aromaattiset yhdisteet).
- HOMO ja LUMO: korkein täytetty molekyyliorbitaali (Highest Occupied Molecular Orbital) ja matalin tyhjä (Lowest Unoccupied Molecular Orbital) määräävät usein kemiallisen reaktiivisuuden ja elektronisiirtymien todennäköisyyden.
- Elektronien täyttö: MO‑tasot täytetään Pauli‑periaatteen ja Aufbau‑periaatteen mukaisesti; Hundin sääntö koskee degeneraattisten orbitaalien elektronien sijoittumista.
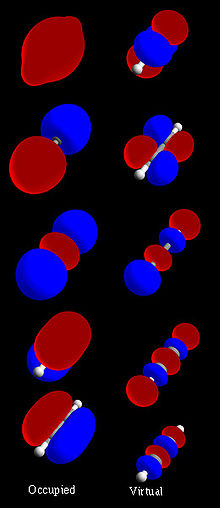
- Todennäköisyys ja tiheys: MO on aaltofunktio ψ; elektronin löytämisen todennäköisyys on |ψ|2. Visualisoinnissa käytetään usein isopintatasoja (isosurfaces) näyttämään, missä elektronitiheys on merkittävää.
- Symmetria ja ryhmäteoria: molekyylin symmetria rajoittaa, mitkä atomiorbitaaleista voivat lomittua; ryhmäteoria auttaa MO‑nimityksissä ja energioiden ennustamisessa.
Esimerkkejä ja ilmiöitä
Yksinkertainen esimerkki on vetymolekyyli H2: kahden H‑1s‑orbitaalin yhdistyessä syntyy yksi sidosorbitaali (σ1s) ja yksi antisiidosorbitaali (σ1s*). Kaksi elektronia täyttävät sidosorbitaalin ja muodostavat yksinkertaisen kovalenttisen sidoksen. Toisaalta happimolekyyli O2 selittyy MO‑teorialla siten, että siinä on kaksi paritonta elektronia π*‑antisiidosorbitaaleissa, mikä selittää O2:n paramagnetisuuden — ilmiö, jota yksinkertainen sidosteoria ei kuvaa yhtä sujuvasti.
Laajemmissa π‑järjestelmissä, kuten bentseenissä, MO‑teoria selittää elektronien delokalisaation ja aromaattisuuden: π‑elektronit jakautuvat koko renkaan yli ja muodostavat energialtaan eriytyneitä delokalisoituneita orbitaaleja.
Kvanttimekaniikka, laskennalliset menetelmät ja rajoitukset
Molekyyliorbitaalit perustuvat kvanttimekaniikkaan; käytännön laskennassa sovelletaan erilaisia approksimaatioita. LCAO on yleinen lähestymistapa, ja sen päälle rakennetaan menetelmiä kuten Hartree‑Fock, Density Functional Theory (DFT) tai monielektronimenetelmät (post‑Hartree‑Fock), jotka ottavat huomioon elektronikorrelaation eri tavoin. Laskutoimituksissa käytetään myös basis‑joukkoja (esim. STO‑3G, 6‑31G*), jotka määrittelevät, millaisista funktioista MOit koostetaan.
MO‑mallit tarjoavat usein selkeän ja matemaattisesti käsiteltävän kuvan, mutta niillä on rajoituksensa: hyvin korreloituneissa järjestelmissä yksinkertainen Hartree‑Fock ei riitä, ja lokaalit kemialliset ilmiöt voivat joskus hahmottua paremmin valence bond ‑käsitteellä. Usein paras käytäntö on yhdistää eri lähestymistapoja ja vertailla laskennallisia tuloksia kokeelliseen dataan.
Käytännön havaintoja ja visualisointi
Tietokoneet pystyvät nykyään laskemaan MOita ja visualisoimaan ne kolmiulotteisina pintamuotoina; tällaiset kuvat näyttävät, missä elektronit todennäköisesti sijaitsevat ja miten orbitaalit lomittuvat. MO‑kuvat ja energiadia‑grammit auttavat keskustelemaan sidosten vahvuudesta, elektronisiirtymistä (esim. UV‑VIS‑spektrit) ja reaktiivisuudesta (HOMO/LUMO‑tulkinta).
Yhteenvetona: molekyyliorbitaalit ovat kvanttimekaaninen työkalu, joka yhdistää atomiorbitaalit ja selittää monia molekyylien sähköisiä ja kemiallisia ominaisuuksia. Ne tarjoavat selkeän tavan ymmärtää sidoksia, elektronien jakautumista ja reaktioalttiutta, kun käytetään sopivia laskennallisia menetelmiä ja huomioidaan niiden rajoitukset.