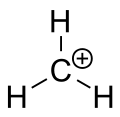
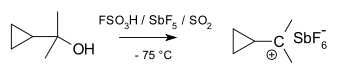
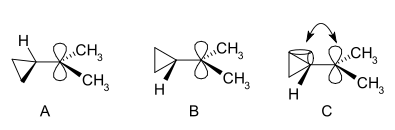
Karbokationi on ioni, jossa on positiivisesti varautunut hiiliatomi. Karbokationin varautunut hiiliatomi muodostaa niin sanotun "sekstetin" eli sillä on vain kuusi elektronia ulommassa valenssikuoressaan kahdeksan valenssielektronin sijasta. Hiiliatomeilla, joilla on kahdeksan valenssielektronia, on yleensä suurempi stabiilisuus (oktettisääntö), minkä vuoksi karbokationit ovat elektroni- ja oktettivajaita sekä usein kemiallisesti hyvin reaktiivisia: ne pyrkivät täyttämään valenssikuorensa ja palauttamaan neutraalin varauksen.
Hybridisaatio ja geometria
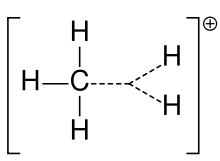
Intuitiotasolla voisi ajatella karbokationin liittyvän 3sp-hybridisaatioon, koska positiivinen varaus liittyy "tyhjyyteen". Kuitenkin kokeellinen ja teoreettinen näyttö osoittaa, että tyypillinen karbokation on sp²-hybridisoitunut: kaksi sp²-hybridiorbitaalia muodostavat sigma-sidokset kahteen substituenttiin ja jäljelle jäävä tyhjä p-orbitaali (p) on kohtisuorassa tasoa vastaan. Tämän vuoksi karbokationin rakenne on yleensä trigonaalinen tasomainen (trigonal planar) eikä tetraedrinen.
Stabiilisuus – mikä vaikuttaa karbokationin elinkaareen
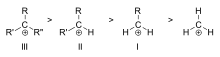
- Alkyylinen konjugaatio ja hyperkonjugaatio: alkyyliryhmät stabiloivat karbokationia hyperkonjugaatiossa ja induktiivisesti siirtämällä elektronitiheyttä positiiviselle hiilelle. Näin tertiääriset karbokationit ovat stabillimpia kuin sekundääriset, jotka taas ovat stabillimpia kuin primääriset ja metyylikarbokationit.
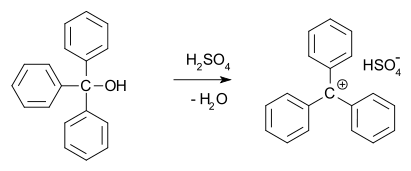
- Resonanssi: karbokationi, jonka positiivinen varaus voidaan delokalisoida kaksoissidoksen (allyyli) tai aromaattisen järjestelmän (bentsyyli) kautta, on huomattavasti stabiilimpi kuin paikallisoitunut karbokationi.
- Vallitseva liuotin ja vastaimen vaikutus: polaariset liuottimet ja stabiloivat vastaimet (esim. konjugaattihapot ja superhapot) voivat pidentää karbokationin elinaikaa.
- Elektronisia tekijöitä: elektronivetävät substituentit heikentävät, elektronidoonorit vahvistavat stabiilisuutta.
Reaktiivisuus ja yleiset reaktiot
- Nukleofiilinen additio/korvaus: tyhjä p-orbitaali tekee karbokationista vahvan elektrofiilin; se reagoi helposti nukleofiilien (esim. vesimolekyylit, alkoholit, halidit) kanssa muodostaen uusia sidoksia. Monet SN1-reaktiot kulkevat karbokationivälituotteen kautta.
- Eliminaatio: karbokation voi menettää protonin muodostuakseen alkeeniksi (E1-mekanismi).
- Uudelleenjärjestelyt: hydride- tai alkylisiirtymät (hydride shift, alkyl shift) voivat tapahtua, kun siirtymä johtaa stabiilimpaan karbokationiin (esim. primäärisestä sekundääriseen tai sekundäärisestä tertiääriseen).
- Delokalisoituneet reaktiot: allyyli- ja bentsyylikarbokationit osallistuvat reaktioihin, joissa varausta voidaan delokalisoida, mikä muuttaa niiden reaktioalttiutta ja selektiivisyyttä.
Esimerkkejä ja käytännön merkitys
- Metyylikarbokationi (CH3+) on hyvin epästabiili ja harvoin havaittavissa vapaana välituotteena tavanomaisissa olosuhteissa.
- Sekundääriset ja tertiääriset karbokationit syntyvät helposti heterolyyttisessä kloorin tai bromin lähtöryhmän lähdössä solvolyyseissä (SN1/E1).
- Allyyli- ja bentsyylikarbokationit ovat huomattavasti stabiilimpia resonanssin vuoksi; tästä seuraa tyypillinen reaktiivisuus esimerkiksi Friedel–Crafts-alkyloinnissa tai kiehumistilanteissa.
- Karboniumit ja paljon stabiloidut karbokationityypit voidaan havaita ja tutkia superhapoissa ja matriiseissa; Nobel-palkittu tutkimus kemiassa (esim. G. A. Olahin työ) laajensi ymmärrystämme karbokationien olemassaolosta ja stabiilisuudesta.
Tiivistelmä
Karbokationi on positiivinen hiili-ioni, joka on elektronivajainen ja siksi yleensä hyvin reaktiivinen. Vaikka intuitio saattaa viitata johonkin muuhun hybridisaatioon, useimmat karbokationit ovat sp²-hybridisoituneita ja trigonaalisesti tasomaisia, ja niiden stabiliteetti riippuu hyperkonjugaatiosta, resonanssista, induktiivisista vaikutuksista ja ympäristöstä. Näiden ominaisuuksien tunteminen selittää monia orgaanisen kemian reaktiomekanismeja ja reaktiotuotteiden muodostumista.