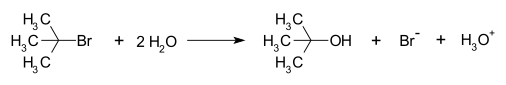
NS1-reaktio on orgaanisen kemian substituutioreaktio, jossa "SN" tarkoittaa nukleofiilistä substituutiota ja "1" sitä, että nopeuden määräävään vaiheeseen osallistuu vain yksi reaktiokomponentti (yksimolekyylinen). Reaktio etenee tyypillisesti kahdessa vaiheessa ja siihen liittyy stabiili karbokationivälituote (karbokationi), minkä vuoksi tätä mekanismia kutsutaan myös dissosiatiiviseksi mekanismiksi. Christopher Ingold et al. ehdottivat reaktiomekanismia ensimmäisen kerran vuonna 1940.
Mekanismi ja kinetiikka
SN1-reaktio etenee tyypillisesti kahdessa pääaskeleessa:
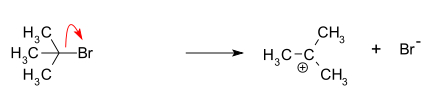
- Ionisaatio (nopeuden määräävä vaihe): lähtöaineesta irtoaa hyvä lähtöryhmä muodostaen karbokationin ja lähtevän ryhmän anionin. Tämän vaiheen hidasnessa tapahtumassa määrääntyy reaktion nopeus. Kinetiikka on ensimmäisen kertaluvun: rate = k[lähtöaine].
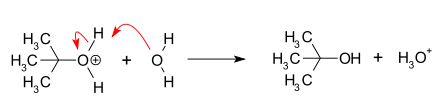
- Nukleofiilinen hyökkäys: vapaan karbokationin planaariseen hiileen nukleofiili liittyy nopeasti, muodostaen substituution lopputuotteen.
Tämän vuoksi reaktion nopeuteen vaikuttaa pääasiassa lähtöaineen kyky muodostaa stabiili karbokationi (sekundaarinen, tertiäärinen tai resonanssistabiloitu, kuten benzyylinen tai allyylinen). Nukleofiilin konsentraatio on yleensä vähäisempi tekijä verrattuna SN2-reaktioihin.
Tekijät, jotka suosivat SN1-reaktiota
- Substraatin stabiilisuus: tertiääriset > sekundaariset. Poikkeuksena ovat resonanssistabiloidut primaariset karbokationit (esim. benzyylinen, allyylinen), jotka voivat reagoida SN1-mekanismin kautta.
- Lähtöryhmän laatu: hyvä lähtöryhmä (esim. halidit, tosylaatit) helpottaa ionisaatiota.
- Liukenne: polaariset protiset liuottimet (vesi, alkoholijohdannaiset) stabiloivat ioneja ja suosivat SN1-reaktioita.
- Nukleofiilin heikkous: SN1-reaktioissa nukleofiilin voimakkuus on usein vähemmän ratkaiseva, koska nukleofiili hyökkää vasta karbokationin muodostumisen jälkeen.
- Happamuus tai emäksisyys: tietyissä olosuhteissa (esim. vahvasti hapan) alkoholit voivat protonoitua ja lähtöryhmästä tulee parempi lähtijä, jolloin sekundaariset tai tertiääriset alkoholit voivat käydä SN1-tyyppisesti substuutioreaktioita. Vastaavasti joissain emäksisissä olosuhteissa tietyt substraatit käyttäytyvät SN1-tyyppisesti.
Stereokemia ja ioniparit
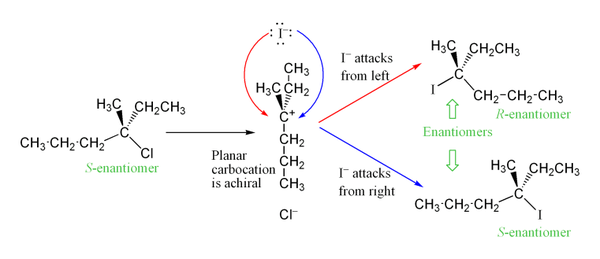
Karbokationi on planaarinen ja nukleofiili voi hyökätä kummalta tahansa puolelta, minkä vuoksi SN1-reaktio johtaa yleensä rasemisaatioon (sekä retention että inversion sekoitus). Käytännössä täydellinen racemisointi voi jäädä puutteelliseksi, koska välillä syntyy ns. kontakti- tai intimii-ioni-pareja, joissa lähtevä anioni pysyy lähellä karbokationia ja estää vapaan hyökkäyksen toiselta puolelta.
Karbokationin rearranget
Karbokationivälituote voi käydä reorganisoitumisia (esim. hydride- tai alkylisiirtoja) muodostaakseen entistä stabiilimman karbokationin. Tällaiset rearranget johtavat usein odottamattomiin tuotteisiin ja ovat tyypillisiä sekundaaristen karbokationien kohdalla, jotka voivat siirtyä tertiarymuotoon.
Esimerkkejä
- Tert-amyylikloridin hydrolyysi vedessä (solvolyysi) johtaa tertiääriseen alkoholiin. Esimerkiksi tert-butyylikloridin reaktio veden kanssa on tunnettu SN1-esimerkki.
- Benzyylikloridi (primaarinen) voi reagoida SN1-mekanismilla, koska benzyylinen karbokationi on resonanssistabiloitu.
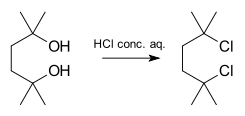
- Sekundaaristen alkoholien protonointi happamassa ympäristössä voi johtaa veden lähtemiseen ja karbokationin muodostumiseen, jolloin nukleofiili (esim. vesi tai muu liuotin) liittyy nopeasti.
- Rearrangeerausesimerkkinä 2-butanolin protonointi ja vedenlähtö voi muodostaa sekundaarisen karbokationin, joka voi siirtyä hydride-siirrolla tertiääriseksi karbokationiksi ja näin muuttaa lopputuotetta.
Vertailu SN2-reaktioon
- Kinetiikka: SN1 on ensimmäisen kertaluvun (rate = k[substrate]); SN2 on toisen kertaluvun (rate = k[substrate][nukleofiili]).
- Stereokemia: SN1 yleensä racemisaatio, SN2 antaa inversiota (Waldenin inversio).
- Substraatti: SN1 suosii tertiäärisiä ja resonanssistabiloituja substraatteja; SN2 suosii primaarisia ja steriilitön substraatti.
- Liuotin: SN1 hyötyy polaarisista protisista liuottimista, kun taas SN2 sujuu usein paremmin polaarisissa aprotisissa liuottimissa.
Yhteenvetona: SN1-reaktio on tärkeä mekanismi orgaanisessa kemiassa, jossa lähtöaineen kyky muodostaa stabiili karbokationi, hyvä lähtöryhmä ja liuotinolosuhteet määrittävät reaktion todennäköisyyden ja nopeuden. SN1-reaktioihin liittyy usein karbokationin rearrangeeraukset ja stereokemialliset muutokset, jotka on syytä huomioida reaktiota suunniteltaessa.