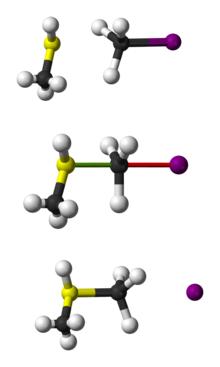
SN 2 -reaktio (tunnetaan myös nimellä bimolekulaarinen nukleofiilinen substituutio) on orgaanisen kemian substituutioreaktio. Se on eräänlainen nukleofiilinen substituutio, jossa nukleofiilin yksinäinen pari hyökkää elektronipuutteiseen elektrofiiliseen keskukseen ja sitoutuu siihen. Tällöin toinen ryhmä, jota kutsutaan "poistuvaksi ryhmäksi", poistuu. Tuleva ryhmä korvaa siis lähtevän ryhmän yhdessä vaiheessa. Koska kaksi reagoivaa lajia osallistuu reaktion hitaaseen, nopeuden määräävään vaiheeseen, tästä käytetään nimitystä bimolekulaarinen nukleofiilinen substituutio tai SN 2. Epäorgaanisten kemistien keskuudessa SN 2 -reaktio tunnetaan usein vaihtomekanismina.
Perusmekanismi ja siirtymätila
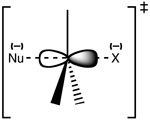
SN 2 on konsertoitu eli yksiaskelinen mekanismi: nukleofiili hyökkää samaan aikaan kun poistuva ryhmä irtoaa. Hyökkäys tapahtuu yleensä reaktion substraatin vastakkaiselta puolelta (backside attack), jolloin johtuu tyypillisesti Waldenin inversiosta eli stereokemiallisesta kääntymisestä karbokationin ympärillä olevien substituenttien järjestyksessä. Siirtymätilassa hiileen on osittaiset sidokset sekä nukleofiiliin että lähtevään ryhmään; tätä tilaa kuvataan usein pentakoordinaation kaltaisena tilana, jossa hiili on "puoliksi" sitoutunut molempiin.
Kinetiikka
- SN 2 -reaktion nopeus riippuu sekä substraatin että nukleofiilin konsentraatioista: rate = k[substrate][nukleofiili]. Tämä tekee reaktiosta toisen kertaluvun (bimolekulaarisen) kinetiikan.
- Nopeuteen vaikuttaa myös lämpötila ja liuotin, ja aktivaatiovaikutus kuvataan Arrheniuksen yhtälöllä.
Tekijät, jotka vaikuttavat SN 2 -reaktion kulkuun
- Substraatin steriikka: vähemmän sterisesti hindered substraatit reagoivat nopeammin (methyl > 1° > 2°; 3° on yleensä hyvin hidas tai estynyt).
- Poistuvan ryhmän laatu: hyvä poistuva ryhmä (esim. I−, Br−, tosylaatti) helpottaa reaktiota; huono poistuva ryhmä hidastaa sitä.
- Nukleofiilin perusyys ja varaus: vahva, negatiivisesti varautunut nukleofiili on yleensä reaktiivisempi (esim. OH−, RS−, CN−). Kuitenkin liuotin ja paritusionit voivat muuttaa aktiivisuutta.
- Liuotin: polar aprotic -liuottimet (esim. DMSO, DMF, acetonitrile) suosivat SN 2-reaktioita, koska ne eivät koordinoidu voimakkaasti anioneihin ja jättävät nukleofiilin "vapaimmaksi". Protisissa liuottimissa (vety sidos) nukleofiili saattaa heikentyä solvaation vuoksi.
- Konjugaatio ja elektroniset tekijät: allyyli- ja benzyyli-substraatit reagoivat usein helposti SN 2 -tyyppisesti, koska siirtymätilaa stabiloi delokalisaatio.
Stereokemia
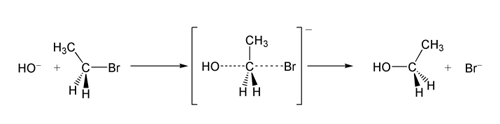
SN 2-iskun seurauksena tapahtuu tyypillisesti täydellinen Waldenin inversio eli konfiguraation kääntyminen. Tämä on tärkeä ominaisuus synteesissä, kun halutaan kontrolloida tuotteen stereokemiaa. Jos substraatti on optisesti aktiivinen ja nukleofiili hyökkää ainoastaan takapuolelta, tuote on peilikuvansa (invertoitunut) asema suhteessa lähtöaineeseen.
Esimerkkejä ja sovelluksia
- Williamsonin eetterisynteesi (alkoholaatin hyökkäys alkyylihalidiin) on klassinen SN 2 -reaktio.
- Halogeenin vaihtuminen hydroksyyliryhmään tai päinvastoin (esim. R–Br + OH− → R–OH + Br−) tapahtuu usein SN 2-mekanismilla, jos substraatti ei ole liiaksi sumeeraantunut.
- CN−-ionin lisääminen alkyylihalidiin antaa nitrilejä ja on yleinen tapa muodostaa hiili-hiili- kolmoissidoksia jatkokemian lähtöaineeksi.
Rajoitukset ja kilpailuprosessit
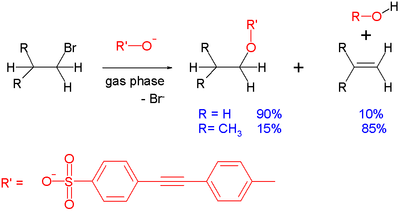
SN 2 ei ole ainoa mahdollinen reaktioreitti. Erityisesti substraateilla, joissa on suuri sterinen este tai jotka muodostavat stabiilin karbokationin, SN1-mekanismi voi kilpailla tai ylittää SN 2:n. Lisäksi E2-eliminaatio voi kilpailla SN 2:n kanssa, erityisesti vahvojen peräkkäisten emästen ja heikosti haluttujen poistuvien ryhmien yhteydessä; E2 johtaa alkeenin muodostumiseen eikä substituutioon.
Käytännön vinkkejä laboratoriossa
- Valitse polar aprotic -liuotin, kun tavoitteena on SN 2 ja nukleofiili on anioninen.
- Vältä liian sterisesti hindered substraatteja, jos haluat tehokkaan SN 2:sen.
- Käytä hyvää poistuvaa ryhmää (esim. tosylation ennen SN 2:tä huonon poistuvan ryhmän parantamiseksi).
- Optimoi lämpötila ja konsentraatiot; suurempi nukleofiilikonsentraatio yleensä nopeuttaa reaktiota.
Yhteenvetona SN 2 on nopeasti ymmärrettävä ja käytännöllinen mekanismi orgaanisessa synteesissä silloin, kun halutaan suoraviivaista substituutiota, selkeä stereokemian hallinta ja kun substraatti sekä reaktioolosuhteet suosivat konsertoitua, takaa hyökkäystä sisältävää kulkua.